Clear Sky Science · it
Varianti di snRNA U1 contribuiscono al controllo del ciclo cellulare e della differenziazione delle cellule iPS umane
Perché piccoli frammenti di RNA contano per le cellule staminali
Le cellule staminali affascinano medici e ingegneri perché possono trasformarsi in quasi qualsiasi cellula del corpo. Questa promessa dipende da un controllo interno molto rigoroso. Questo studio esamina un gruppo trascurato di minuscole molecole di RNA nelle cellule staminali pluripotenti indotte (iPS) umane e mostra che esse contribuiscono silenziosamente a decidere la velocità di divisione delle staminali e il loro grado di prontezza a diventare cellule specializzate.
Piccoli aiutanti nella fabbrica dei messaggi cellulari
All'interno di ogni cellula, i geni vengono prima copiati in messaggi di RNA, che vengono poi rifiniti e cuciti insieme prima di essere letti come istruzioni per produrre proteine. Una parte chiave di questo macchinario di rifinitura usa piccoli RNA chiamati U1. Per anni, copie extra di RNA simili a U1 sono state considerate avanzi privi di funzione. Gli autori si concentrano su due di questi sosia, chiamati varianti U1, che sono particolarmente attive nei tessuti umani precoci e nelle cellule staminali. Poiché le loro sequenze differiscono leggermente dall'U1 principale, potrebbero riconoscere siti di taglio diversi nell'RNA e modificare sottilmente quali versioni proteiche una cellula può produrre.
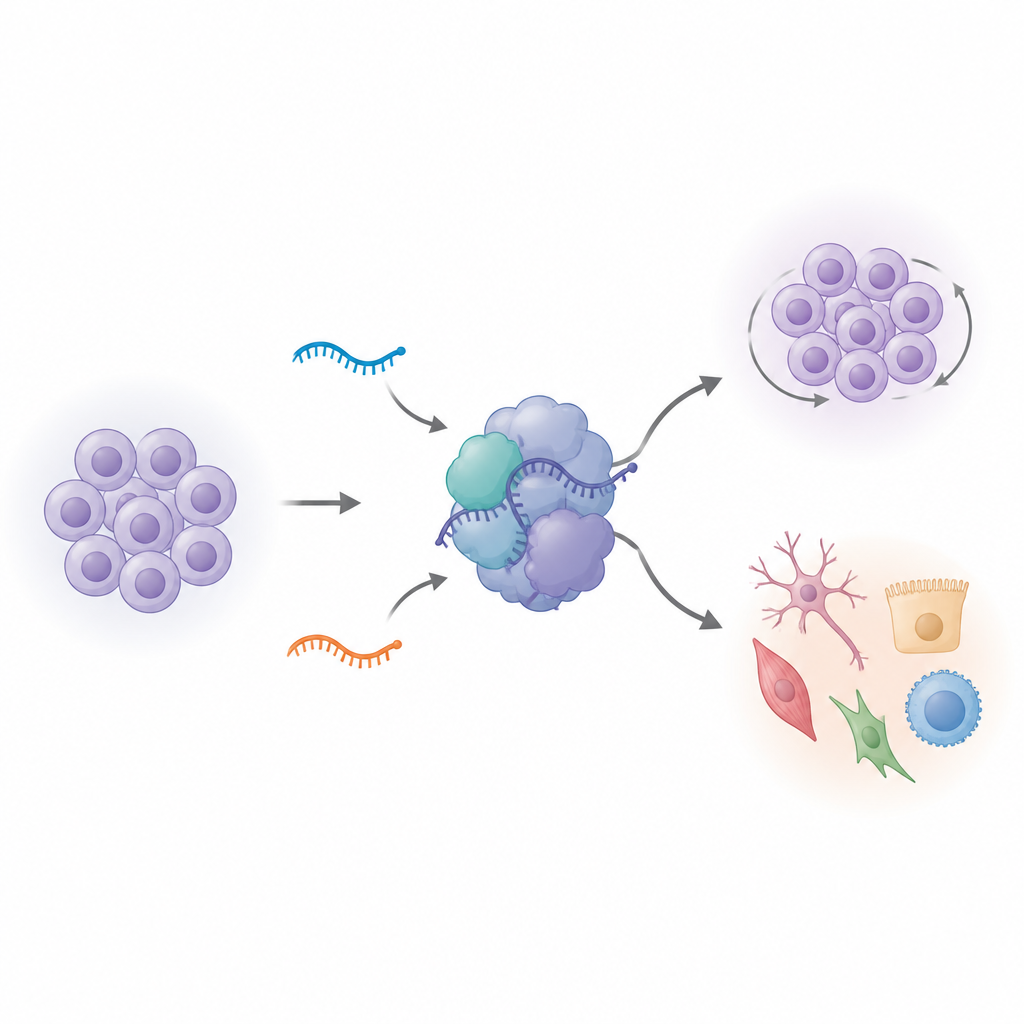
Spegnere le varianti di RNA rimodella il comportamento delle staminali
Per capire cosa fanno realmente queste varianti U1, il gruppo ha usato l'editing genomico per eliminare ciascuna delle due varianti in cellule iPS umane. A prima vista le cellule modificate sembravano normali. Ma quando i ricercatori hanno misurato quali geni erano attivi o spenti, hanno osservato cambiamenti diffusi, in particolare dopo la cancellazione di una variante, vU1.8. Centinaia di geni coinvolti nella divisione cellulare e nell'identità delle staminali hanno modificato la loro attività. Anche gli orologi interni delle cellule sono cambiati: più cellule si sono accumulate in una fase tardiva del ciclo cellulare e i tassi di crescita complessivi sono aumentati quando le cellule sono state spinte a iniziare la differenziazione. I geni che di solito marcano la staminalità e lo sviluppo cerebrale precoce non hanno più seguito i loro schemi normali, suggerendo che questi piccoli RNA aiutano a mantenere le cellule staminali in uno stato ben calibrato tra auto-rinnovamento e specializzazione.
Modificare i messaggi tagliando e ricongiungendo
Lo studio ha quindi analizzato in dettaglio come le varianti U1 influenzano la rifinitura dei messaggi di RNA. Molti geni umani possono essere tagliati e ricongiunti in modi diversi, producendo varianti proteiche che differiscono per stabilità, localizzazione o attività. Confrontando cellule staminali normali e modificate, gli autori hanno scoperto migliaia di cambiamenti nello splicing dell'RNA. Alcuni messaggi hanno perso sezioni codificanti importanti e hanno prodotto versioni accorciate o non codificanti. Una variante favoriva cambiamenti all'inizio e alla fine dei messaggi, accorciando le regioni terminali che possono controllare la durata di vita di un RNA e quando viene utilizzato. I geni legati alla divisione cellulare e allo sviluppo neurale sono stati particolarmente colpiti, collegando questi piccoli RNA a processi centrali sia per la crescita sana sia per la formazione del cervello.
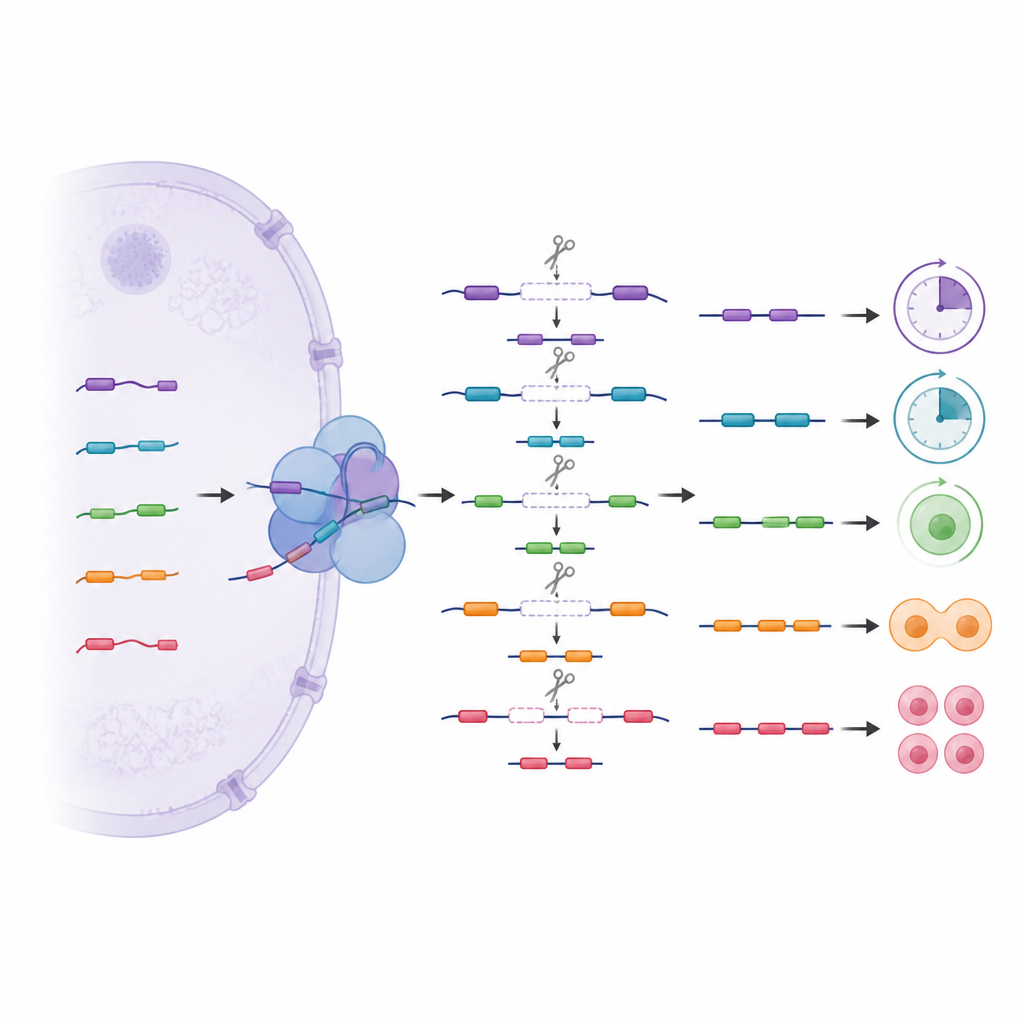
Uno strato nascosto di tagli passo-passo
Oltre allo splicing ordinario, il team ha esplorato un modello più complesso chiamato splicing ricorsivo, in cui lunghi segmenti genici vengono rimossi in più passaggi usando siti di taglio interni nascosti. Questi tagli stepwise erano più comuni nelle cellule dello sviluppo precoce e nei geni che gestiscono DNA, RNA e segnali cellulari. Tracciando la frequenza di utilizzo di siti specifici nelle cellule normali e modificate, gli autori hanno trovato che le varianti U1 aiutano a scegliere quali siti interni vengono riconosciuti. La perdita di una variante ha fatto sì che alcuni siti venissero saltati e altri usati più spesso, modificando di conseguenza i pezzi di messaggio vicini. Alcuni di questi segmenti nascosti si comportano come mini-esoni criptici che di solito sono esclusi dai messaggi finali ma possono inserirsi quando il controllo viene perso, portando potenzialmente a RNA instabili o degradati.
Cosa significa per la ricerca sulle staminali e le malattie
Nel complesso, il lavoro rivela che queste varianti di U1 non sono osservatrici silenziose. Influenzano se le cellule staminali si dividono, quali versioni proteiche possono produrre e quanto durano i loro messaggi di RNA. Guidando sia lo splicing ordinario sia quello stepwise, aggiungono un livello di fine regolazione alle reti di controllo genico che sostengono le cellule staminali pluripotenti umane e guidano i loro primi passi verso la trasformazione in neuroni e altri tipi cellulari. Poiché i geni che contengono questi siti di splicing speciali ospitano anche varianti genetiche associate a disturbi umani, comprendere come funzionano le varianti U1 potrebbe infine aiutare a spiegare perché alcune modifiche nel DNA non codificante contribuiscono a malattie dello sviluppo e neurologiche.
Citazione: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
Parole chiave: cellule staminali, splicing dell'RNA, ciclo cellulare, pluripotenza, sviluppo neurologico