Clear Sky Science · pt
snRNAs variante U1 contribuem ao controle do ciclo celular e da diferenciação de células iPS humanas
Por que trechos minúsculos de RNA importam para células-tronco
Células-tronco fascinam médicos e engenheiros porque podem se transformar em quase qualquer tipo celular do corpo. Essa promessa depende de controles internos muito rígidos. Este estudo examina um grupo pouco observado de pequenas moléculas de RNA em células-tronco pluripotentes induzidas humanas e mostra que elas silenciosamente ajudam a decidir com que rapidez as células-tronco se dividem e quão prontas estão para se tornar células especializadas.
Pequenos auxiliares na fábrica de mensagens da célula
Dentro de cada célula, os genes são primeiro copiados em mensagens de RNA, que são então aparadas e costuradas antes de serem lidas como instruções para fabricar proteínas. Uma parte chave dessa maquinaria de processamento usa pequenos RNAs chamados U1. Por anos, cópias extras de RNAs semelhantes ao U1 foram consideradas sobras inúteis. Os autores focam em dois desses sósias, chamados U1 variantes, que são especialmente ativos em tecidos humanos iniciais e em células-tronco. Como suas sequências diferem ligeiramente do U1 principal, eles podem reconhecer locais de corte diferentes no RNA e alterar sutilmente quais versões de proteína a célula pode produzir.
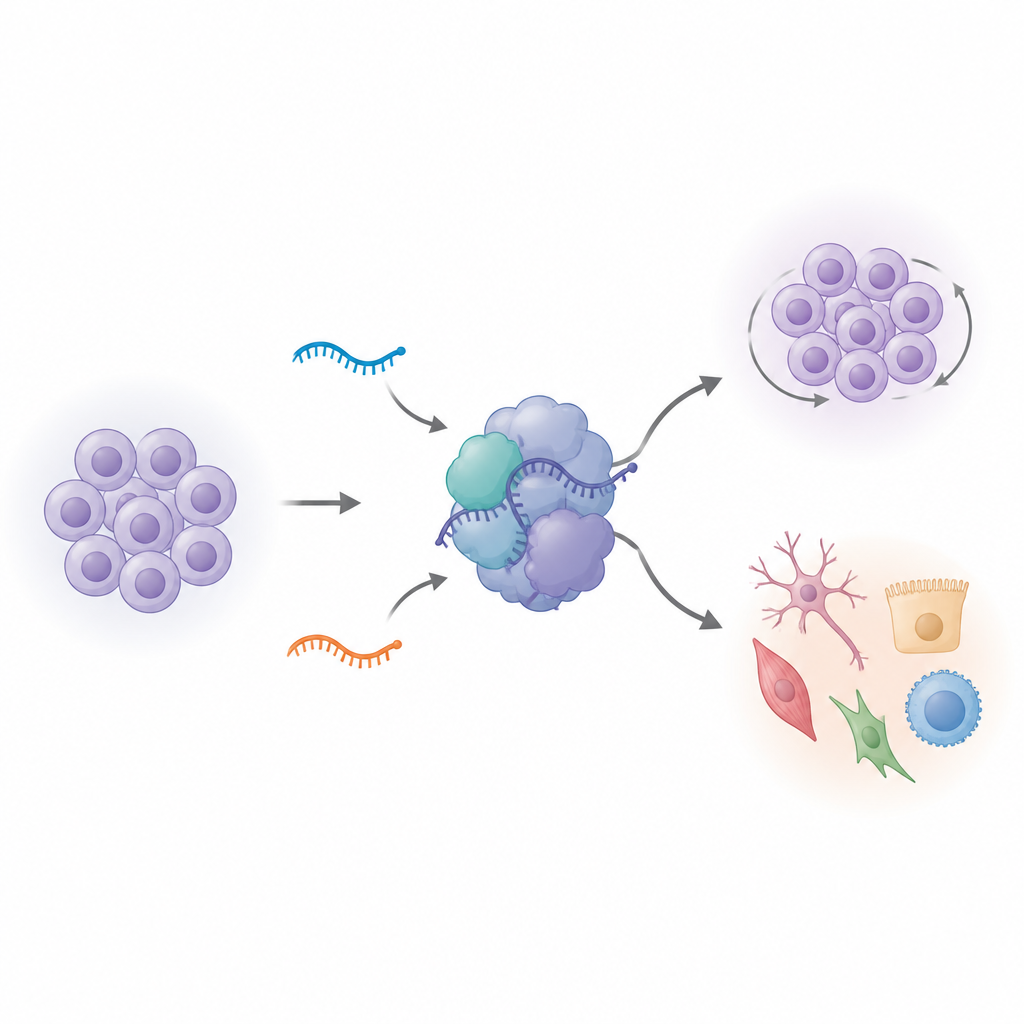
Desligar RNAs variantes remodela o comportamento das células-tronco
Para ver o que essas U1 variantes realmente fazem, a equipe usou edição genômica para remover cada uma das duas variantes em células iPS humanas. À primeira vista, as células editadas pareciam normais. Mas quando os pesquisadores mediram quais genes estavam ligados ou desligados, encontraram mudanças amplas, especialmente quando uma variante, vU1.8, foi deletada. Centenas de genes ligados à divisão celular e à identidade de células-tronco mudaram sua atividade. Os relógios internos das células também mudaram: mais células se acumularam em uma fase posterior do ciclo celular, e as taxas de crescimento aumentaram quando as células foram empurradas a iniciar a diferenciação. Genes que normalmente marcam a pluripotência e o desenvolvimento cerebral inicial deixaram de seguir seus padrões usuais, sugerindo que esses pequenos RNAs ajudam a manter as células-tronco em um estado bem ajustado entre autorrenovação e especialização.
Editando mensagens por corte e religação
O estudo então se aprofundou em como as U1 variantes influenciam o processamento detalhado das mensagens de RNA. Muitos genes humanos podem ser cortados e religados de maneiras diferentes, produzindo variantes de proteínas que diferem em estabilidade, localização ou atividade. Ao comparar células-tronco normais e editadas, os autores descobriram milhares de mudanças em como os RNAs eram emendados. Algumas mensagens perderam trechos codificadores importantes e passaram a produzir versões encurtadas ou não codificantes. Uma das variantes favoreceu alterações no início e no fim das mensagens, aparando as regiões de cauda que podem controlar quanto tempo um RNA sobrevive e quando é usado. Genes ligados à divisão celular e ao desenvolvimento neural foram especialmente afetados, ligando esses pequenos RNAs a processos centrais tanto para o crescimento saudável quanto para a formação do cérebro.
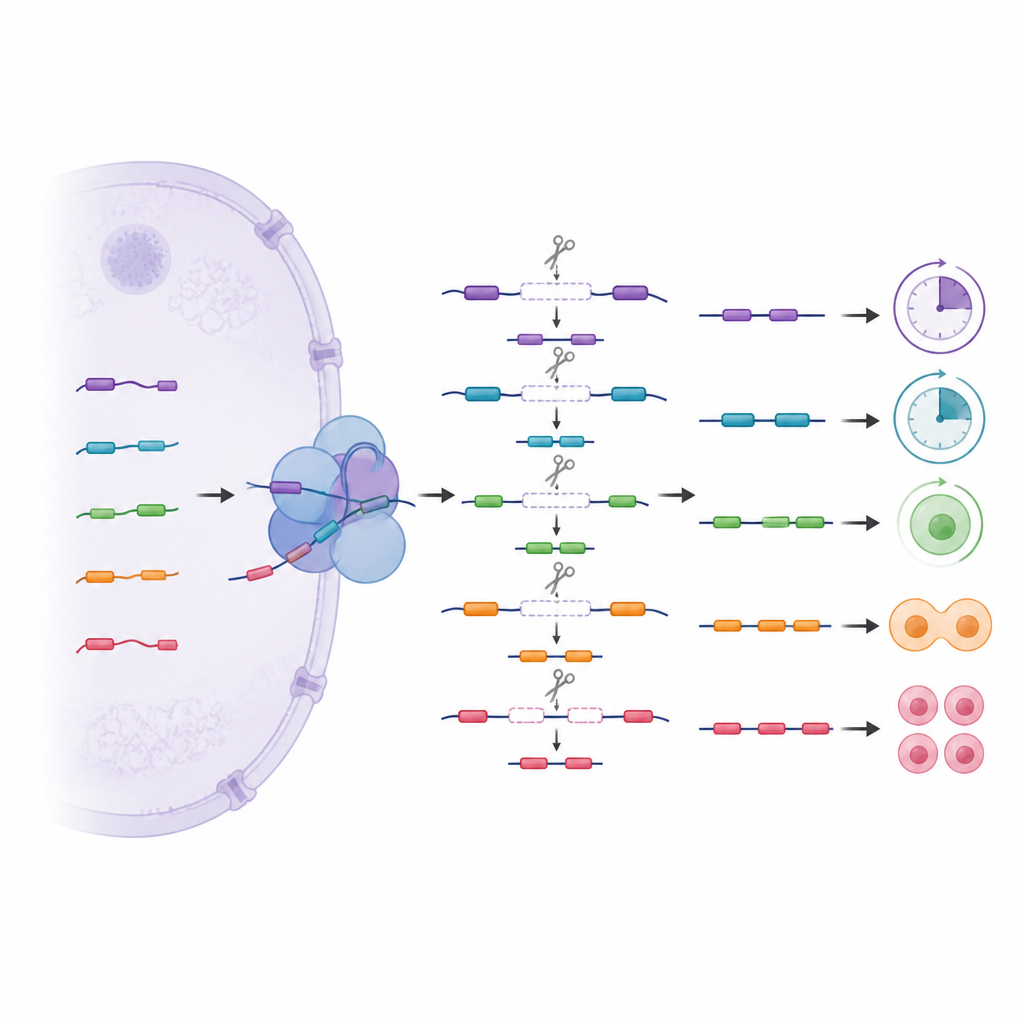
Uma camada oculta de cortes em etapas
Além do emendemento comum, a equipe explorou um padrão mais complexo chamado emendemento recursivo, no qual longos segmentos genômicos são removidos em vários passos usando pontos de corte internos ocultos. Esses cortes em etapas foram mais comuns em células de desenvolvimento inicial e em genes que gerenciam DNA, RNA e sinalização celular. Ao rastrear com que frequência sítios específicos eram usados em células normais e editadas, os autores descobriram que as U1 variantes ajudam a escolher quais sítios internos ocultos são reconhecidos. A perda de uma variante fez com que alguns sítios fossem pulados e outros usados com mais frequência, o que por sua vez alterou trechos de mensagens próximos. Alguns desses segmentos ocultos se comportam como mini-exons crípticos que normalmente ficam fora das mensagens finais, mas podem se inserir quando o controle é perdido, potencialmente levando a RNAs instáveis ou degradados.
O que isso significa para a ciência das células-tronco e para doenças
No conjunto, o trabalho revela que essas U1 variantes não são espectadores silenciosos. Elas influenciam se as células-tronco se dividem, quais versões de proteína podem produzir e quanto tempo suas mensagens de RNA duram. Ao direcionar tanto o emendemento comum quanto o em passos, elas adicionam uma camada de ajuste fino às redes de controle gênico que sustentam células-tronco pluripotentes humanas e orientam seus primeiros passos rumo a neurônios e outros tipos celulares. Como genes que contêm esses sítios de emendemento especiais também abrigam variantes genéticas associadas a distúrbios humanos, entender como as U1 variantes funcionam pode, eventualmente, ajudar a explicar por que certas alterações no DNA não codificante contribuem para doenças do desenvolvimento e neurológicas.
Citação: Zhu, Y., Sofiadis, K., Mizi, A. et al. Variant U1 snRNAs contribute to cell cycle and differentiation control of human iPS cells. Nat Commun 17, 4334 (2026). https://doi.org/10.1038/s41467-026-73121-0
Palavras-chave: células-tronco, emendemento de RNA, ciclo celular, pluripotência, neurodesenvolvimento