Clear Sky Science · zh
肠道代谢的瞬时重塑支持果蝇的幼年生长与成年适应性
生长中的肠道如何塑造整个人生
童年是快速生长的时期,这对果蝇和人类同样适用。本研究探讨了幼体的肠道如何在短期内进入“高档运行”,为最后一波生长冲刺提供能量——以及这种短暂改变如何对成年期健康留下持久印记。通过追踪果蝇(Drosophila)的发育,作者发现肠道代谢在幼年阶段出现暂时性增强,帮助幼虫快速生长、储存能量、抵御恶劣环境,并在成年后成功繁殖。
短暂生命中的突发冲刺
果蝇在蜕变成成虫前经历三个幼虫期。研究人员追踪了各期的体型和生物化学指标,发现生长并非平稳进行。相反,在幼虫生命中期,即最后一个阶段L3,生长速率显著加快。在短短几天内,幼虫体积以及蛋白质、糖类和脂肪等关键构建材料成倍增加,表明出现了需要大量燃料支持的强烈生长冲刺。
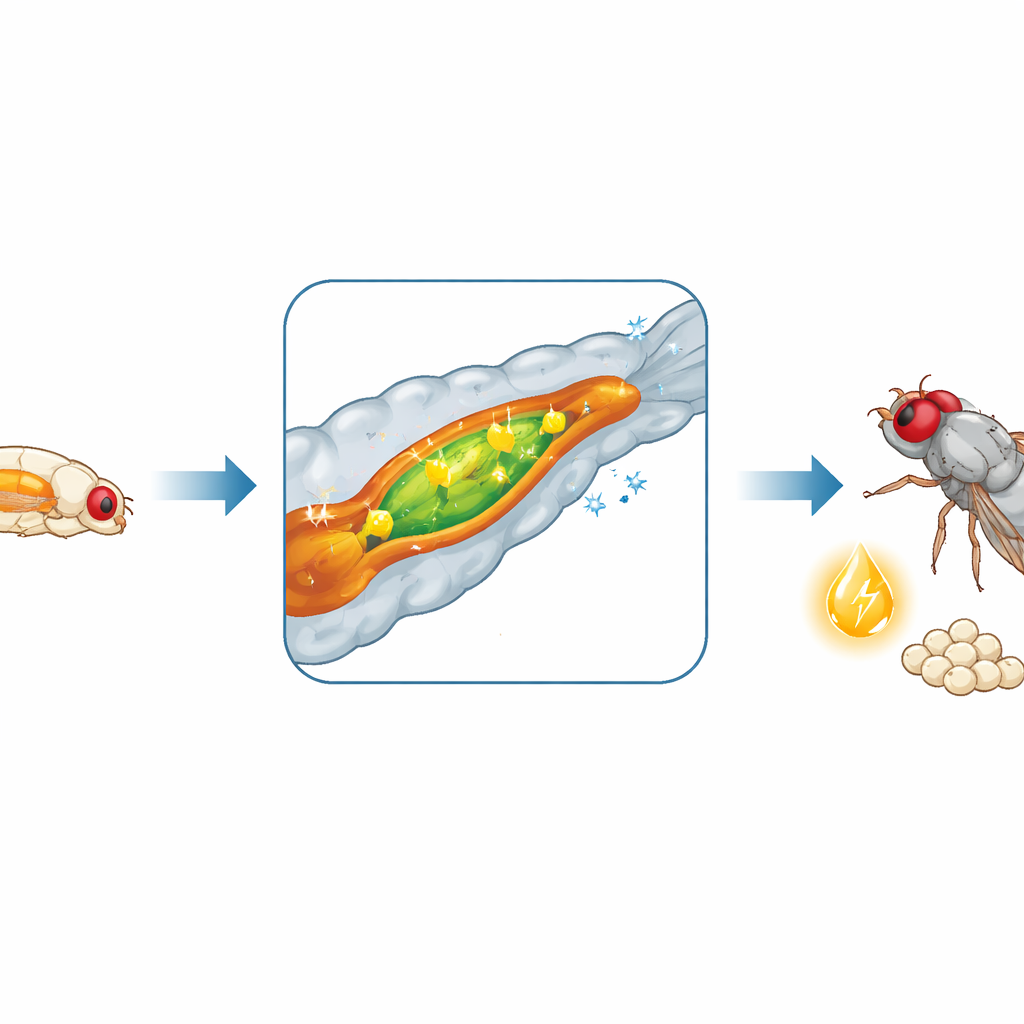
肠道变身为脂肪处理工厂
既然生长依赖食物,团队检查了肠道在这一关键时期是否改变了功能。通过对中肠(相当于哺乳动物的小肠)进行信使RNA测序,他们发现当幼虫进入L3期时基因活性发生了广泛重编程。数百个基因被开启或关闭,尤其是与膳食脂质分解和处理相关的基因。脂肪消化酶含量增加,肠细胞增强了燃烧、储存并至关重要的将脂质输出到全身的能力。对肠道酶和代谢产物的测量证实,L3期脂质消化和动员增强,而血样般的体液中循环脂质水平也相应上升。碳水化合物消化同样加快,进一步为这一能量激增提供燃料。
告诉肠道何时换档的激素
这种肠道改造的时机并非随机。两种核受体——对激素信号做出反应以开启或关闭基因的蛋白——在其中发挥核心作用。一种是类固醇激素蜕皮激素(ecdysone)的受体,负责协调蜕皮和变态等发育转变;另一种是HNF4,一种保守的脂质代谢调控因子。在L3期肠道中,蜕皮激素信号在脂质处理基因被诱导时同步开启。当研究者特异性抑制肠道细胞中的蜕皮激素功能时,脂质代谢基因的正常上调未能发生。脂肪在肠内堆积,而循环中的脂质水平下降,表明肠道无法有效输出脂质。
促进生长与能量储备的协作
HNF4被证实是这一过程中的关键搭档。它在富含脂质的幼虫肠道区域活性上升,近一半在L3期上调的脂质代谢基因的完全诱导依赖于HNF4。在肠道中沉默HNF4会出现与干扰蜕皮激素信号相同的模式:脂肪被困在肠细胞内,循环脂质下降,L3期之后的整体体脂减少。数据表明蜕皮激素提升HNF4水平,而HNF4又激活一整套基因,将肠道改造为高效的膳食脂质传输通道,优先将脂质输出到身体其他部位而非局部储存。然而,如果蜕皮激素被阻断,单靠HNF4无法完全补偿,说明多个激素驱动的通路共同塑造这一代谢开关。
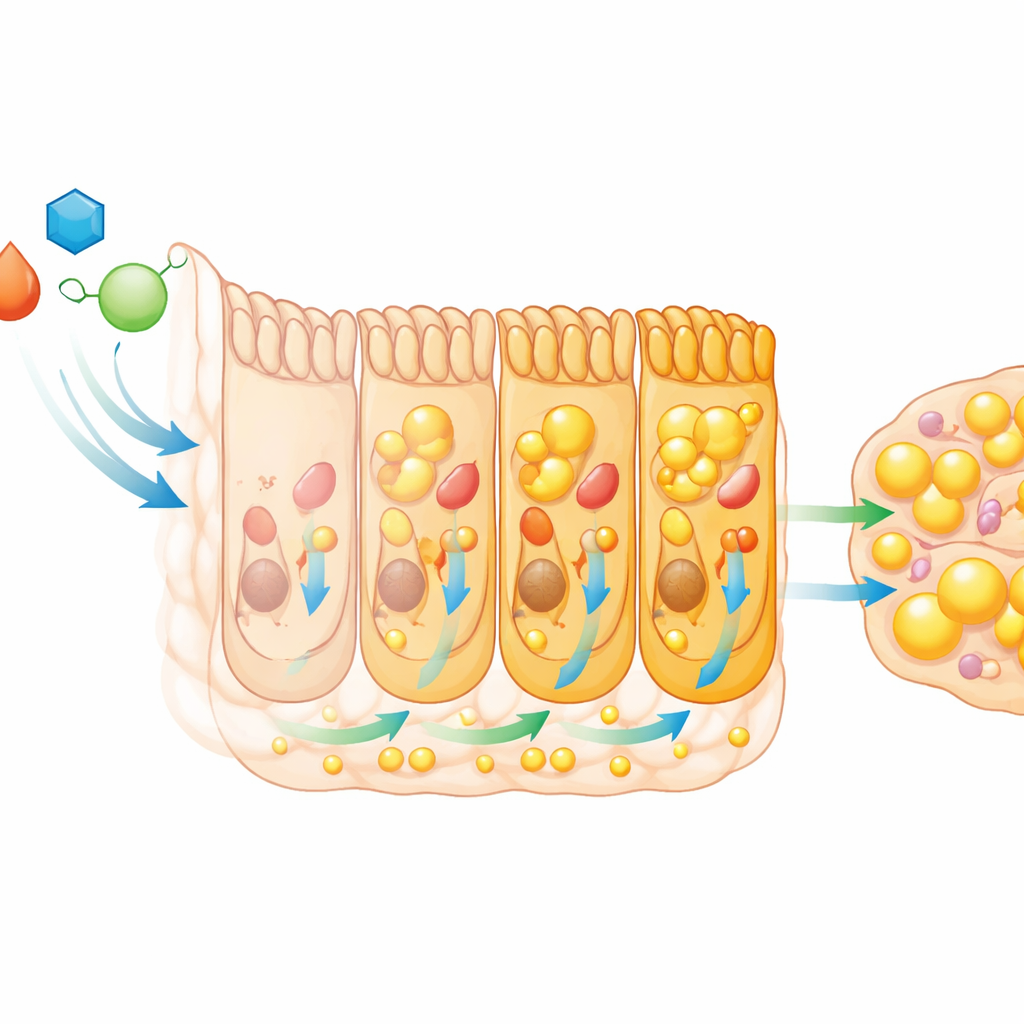
从幼年肠道到成年成功
这段短暂的肠道程序的后果远超幼虫期。当肠道中的蜕皮激素或HNF4受损时,幼虫在L3期生长变慢,蛋白质积累减少,达到变态所需体型的时间被推迟,从而延迟了转变。由缺乏适当肠道重塑的幼虫发育而成的成虫体型更小、偏瘦且脂肪储备减少。这些成虫更容易脱水,雌性个体的卵巢更小,早期产卵量也减少。因此,青年期那一短暂的肠道代谢增强期为机体储存了构建强健成体、抵抗环境压力并迅速繁殖所需的物质。
为何这超越了果蝇本身的重要性
这项工作表明,早期发育中单一器官的短暂变化能够影响生长、类青春期转变的时机以及后期的适应性。在果蝇中,受激素引导的肠道活动在狭窄的发育窗口内爆发,推动最后的生长冲刺并补充能量储备,后来这些储备有助于体表防水和产卵。鉴于许多相同的分子参与者和肠道功能在哺乳动物(包括人类)中具有保守性,这些发现强调了儿童期营养和代谢的暂时性变化可能对终身健康和疾病风险产生长期影响。
引用: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
关键词: 果蝇发育, 肠道代谢, 脂质消化, 类固醇激素, 幼年生长