Clear Sky Science · it
Rimodellamento transitorio del metabolismo intestinale sostiene la crescita giovanile e la fitness adulta in Drosophila
Come gli intestini in crescita plasmano un’intera vita
L’infanzia è un periodo di crescita rapida, e questo vale tanto per le mosche della frutta quanto per gli esseri umani. Questo studio esplora come l’intestino di un animale giovane entri brevemente in “alta marcia” per alimentare un’ultima impennata di crescita — e come questo cambiamento di breve durata lasci tracce durature sulla salute adulta. Seguendo lo sviluppo nella mosca Drosophila, gli autori rivelano un potenziamento temporaneo del metabolismo intestinale che aiuta i giovani a crescere velocemente, immagazzinare energia, resistere ad ambienti avversi e riprodursi con successo da adulti.
Uno sprint improvviso in una vita breve
Le mosche della frutta attraversano tre stadi larvali prima di trasformarsi in adulte. I ricercatori hanno seguito dimensione corporea e chimica corporea attraverso questi stadi e hanno scoperto che la crescita non è costante. Al contrario, accelera drammaticamente a metà della vita larvale, nell’ultimo stadio noto come L3. In appena un paio di giorni il volume larvale e i mattoni fondamentali come proteine, zuccheri e grassi si moltiplicano molte volte, segnalando un’intensa impennata di crescita che richiede grandi quantità di carburante.
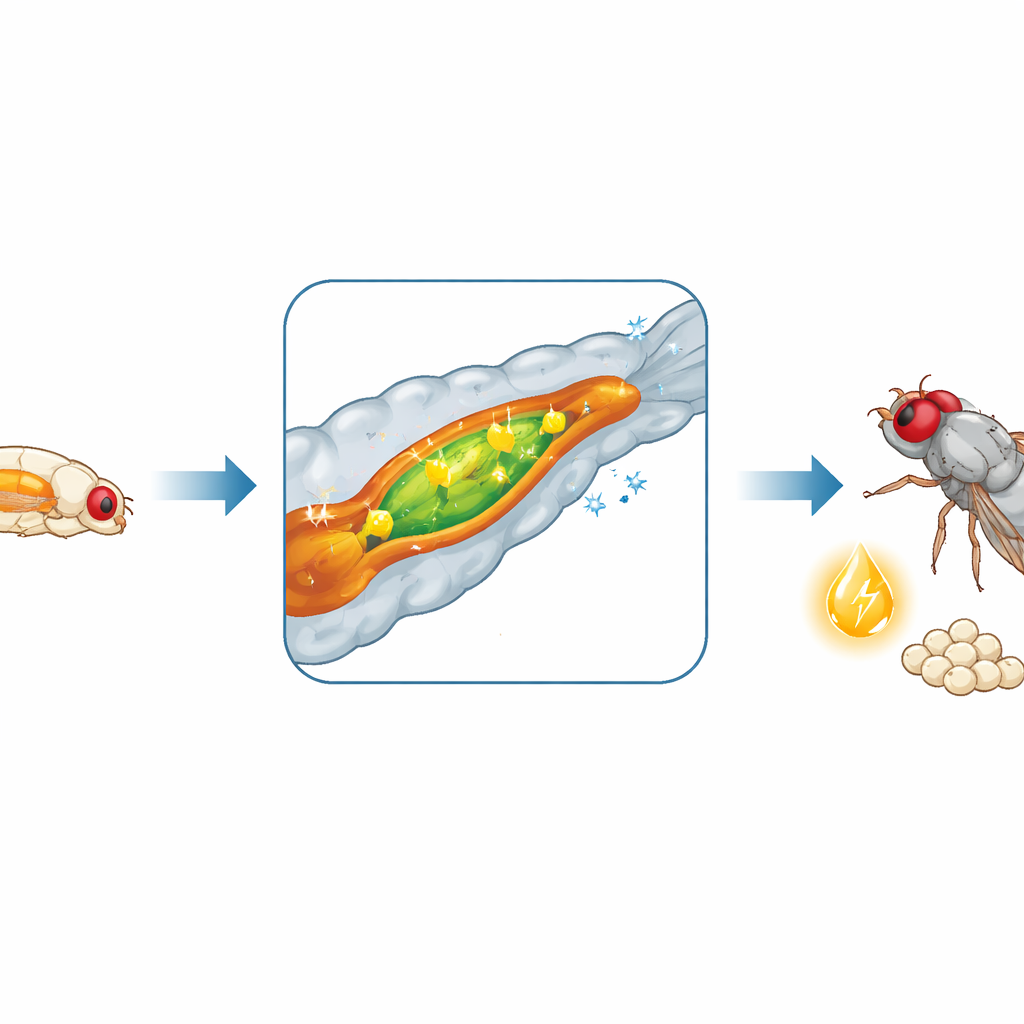
L’intestino si trasforma in una fabbrica di trattamento dei grassi
Poiché la crescita dipende dal cibo, il gruppo ha esaminato se l’intestino modificasse il proprio comportamento in questo momento critico. Sequenziando l’RNA messaggero dal midgut — l’equivalente nell’insetto dell’intestino tenue — hanno scoperto un’ampia riprogrammazione dell’attività genica all’ingresso nello stadio L3. Centinaia di geni si attivano o si spengono, in particolare quelli coinvolti nella degradazione e nella gestione dei grassi alimentari. Le enzimi che digeriscono i lipidi diventano più abbondanti e le cellule intestinali aumentano la capacità di bruciare, immagazzinare e, cosa cruciale, esportare i grassi al resto del corpo. Misure di enzimi intestinali e metaboliti hanno confermato che la digestione e la mobilizzazione dei grassi si intensificano nelle larve L3, e i lipidi circolanti nel fluido simile al sangue aumentano di conseguenza. Anche la digestione dei carboidrati accelera, alimentando ulteriormente questo picco energetico.
Ormoni che dicono all’intestino quando cambiare marcia
Il momento di questo rimodellamento intestinale non è casuale. Due recettori nucleari — proteine che accendono o spengono geni in risposta a segnali ormonali — svolgono ruoli chiave. Uno è il recettore per l’ormone steroideo ecdysone, che coordina transizioni dello sviluppo come la muta e la metamorfosi. L’altro è HNF4, un regolatore conservato del metabolismo lipidico. Nell’intestino L3 la segnalazione di ecdysone si attiva proprio mentre i geni di gestione dei lipidi vengono indotti. Quando i ricercatori hanno bloccato la funzione di ecdysone specificamente nelle cellule intestinali, il normale aumento dei geni del metabolismo lipidico non si è verificato. I grassi si sono accumulati all’interno dell’intestino mentre i livelli circolanti diminuivano, dimostrando che l’intestino non riusciva più a esportare i lipidi in modo efficiente.
Una partnership per crescita e immagazzinamento energetico
HNF4 emerge come partner chiave in questo processo. La sua attività aumenta nelle regioni dell’intestino larvale ricche di lipidi, e quasi la metà dei geni del metabolismo lipidico che aumentano in L3 dipendono da HNF4 per la piena induzione. Silenziare HNF4 nell’intestino ha portato allo stesso schema osservato con la segnalazione di ecdysone compromessa: i grassi rimanevano intrappolati nelle cellule intestinali, i lipidi circolanti calavano e il grasso corporeo complessivo dopo lo stadio L3 risultava ridotto. I dati suggeriscono che l’ecdysone aumenta i livelli di HNF4, che a sua volta attiva una batteria di geni che trasformano l’intestino in un potente condotto per i grassi alimentari, dando priorità all’esportazione verso il resto del corpo rispetto all’immagazzinamento locale. Tuttavia, HNF4 da solo non può compensare completamente se l’ecdysone è bloccato, indicando che più vie guidate da ormoni collaborano a plasmare questo interruttore metabolico.
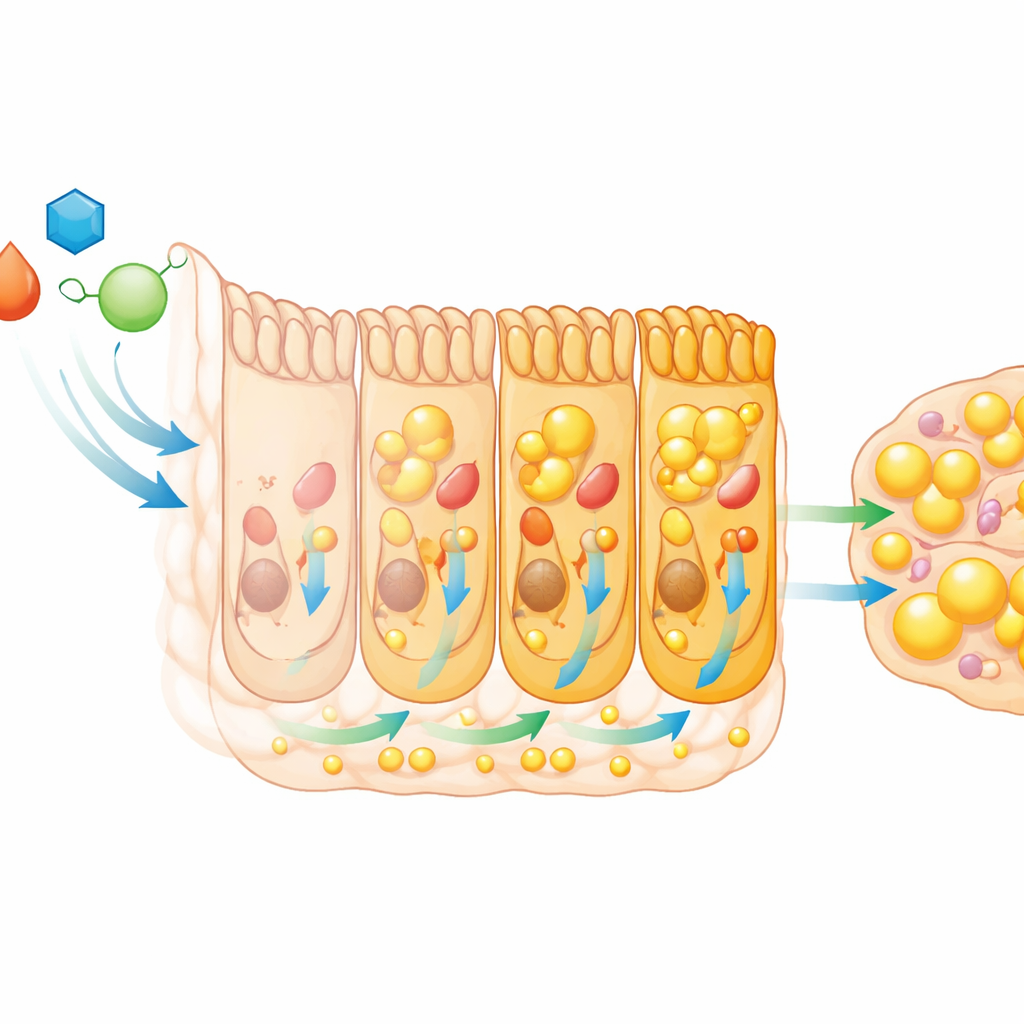
Dall’intestino giovanile al successo adulto
Le conseguenze di questo programma intestinale effimero si estendono ben oltre lo stadio larvale. Quando ecdysone o HNF4 erano compromessi nell’intestino, le larve crescevano più lentamente durante L3, accumulavano meno proteine e raggiungevano più tardi la dimensione necessaria per la metamorfosi, ritardando la trasformazione. Gli adulti derivati da larve prive di un corretto rimodellamento intestinale emergevano più piccoli, più magri e con riserve di grasso ridotte. Questi adulti erano più sensibili alla disidratazione e, nelle femmine, avevano ovaie più piccole e producevano meno uova nella vita precoce. Così, una breve finestra di metabolismo intestinale potenziato in giovinezza fornisce al corpo il materiale necessario per costruire un adulto robusto, resistere allo stress ambientale e riprodursi rapidamente.
Perché questo importa oltre le mosche della frutta
Questo lavoro mostra che cambiamenti precoci in un singolo organo possono plasmare la crescita, il timing di transizioni simili alla pubertà e la fitness successiva. In Drosophila, un’esplosione guidata dagli ormoni dell’attività intestinale durante una finestra di sviluppo ristretta alimenta un’ultima impennata di crescita e riempie le riserve energetiche che in seguito supportano l’impermeabilizzazione del corpo e la produzione di uova. Poiché molti degli stessi attori molecolari e comportamenti intestinali sono conservati nei mammiferi, compresi gli esseri umani, questi risultati evidenziano come spostamenti temporanei nella nutrizione e nel metabolismo durante l’infanzia possano avere conseguenze a lungo termine per la salute e il rischio di malattie nel corso della vita.
Citazione: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
Parole chiave: Sviluppo di Drosophila, metabolismo intestinale, digestione dei lipidi, ormoni steroidei, crescita giovanile