Clear Sky Science · de
Vorübergehende Umgestaltung des Darmstoffwechsels unterstützt juveniles Wachstum und Fitness im Adultstadium bei Drosophila
Wie wachsende Därme ein ganzes Leben formen
Die Kindheit ist eine Zeit schnellen Wachstums, und das gilt für Fruchtfliegen ebenso wie für Menschen. Diese Studie untersucht, wie der Darm eines jungen Tiers vorübergehend in einen „höheren Gang“ schaltet, um einen letzten Wachstumsschub zu befeuern – und wie diese kurzlebige Umstellung bleibende Spuren auf die Gesundheit im Erwachsenenalter hinterlässt. Anhand der Entwicklungsverfolgung bei der Fruchtfliege Drosophila zeigen die Autorinnen und Autoren einen temporären Anstieg des intestinalen Stoffwechsels, der Jungtiere beim schnellen Wachstum, bei der Energiespeicherung, beim Überstehen rauer Umgebungen und beim späteren Fortpflanzungserfolg unterstützt.
Ein plötzlicher Sprint in einem kurzen Leben
Fruchtfliegen durchlaufen drei Larvenstadien, bevor sie sich in Erwachsene verwandeln. Die Forschenden verfolgten Körpergröße und Körperchemie über diese Stadien hinweg und stellten fest, dass das Wachstum nicht gleichmäßig verläuft. Stattdessen beschleunigt es sich auf dramatische Weise in der Mitte der Larvenzeit, im letzten Stadium, bekannt als L3. Innerhalb nur weniger Tage vervielfachen sich Larvenvolumen und zentrale Baustoffe wie Proteine, Zucker und Fette, was auf einen intensiven Wachstumsschub hinweist, der große Mengen an Treibstoff erfordert.
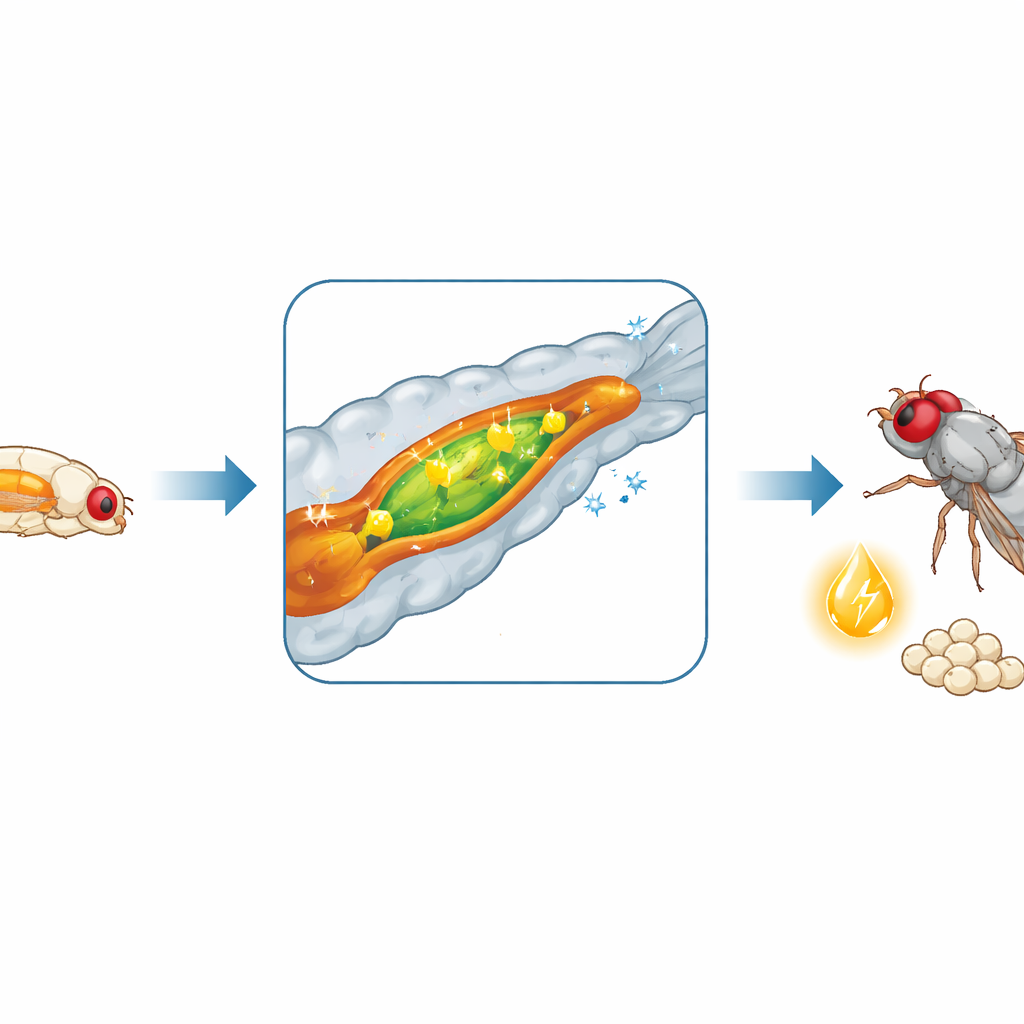
Der Darm verwandelt sich in eine Fettverarbeitungsfabrik
Da Wachstum von Nahrung abhängt, untersuchte das Team, ob sich das Verhalten des Darms zu diesem kritischen Zeitpunkt ändert. Durch Sequenzierung von Boten-RNA aus dem Mitteldarm – dem Gegenstück des Dünndarms bei Fliegen – entdeckten sie eine weitreichende Umprogrammierung der Genaktivität, wenn die Larven in das L3-Stadium eintreten. Hunderte Gene werden an- oder abgeschaltet, besonders solche, die am Abbau und an der Handhabung von Nahrungsfetten beteiligt sind. Enzyme, die Fette verdauen, werden häufiger, und Darmzellen steigern ihre Fähigkeit, Fett zu verbrennen, zu speichern und, entscheidend, Fett an den Rest des Körpers zu exportieren. Messungen von Darmenzymen und Metaboliten bestätigten, dass Fettverdauung und -mobilisierung in L3-Larven intensiviert werden, und zirkulierende Fettanteile in der blutähnlichen Flüssigkeit steigen entsprechend an. Auch die Kohlenhydratverdauung nimmt zu und nährt so diesen Energieschub zusätzlich.
Hormone, die dem Darm sagen, wann er den Gang wechseln soll
Das Timing dieses intestinalen Umbaus ist nicht zufällig. Zwei nukleäre Rezeptoren – Proteine, die Gene als Reaktion auf hormonelle Signale an- oder abschalten – spielen zentrale Rollen. Der eine ist der Rezeptor für das Steroidhormon Ecdysone, das Entwicklungsübergänge wie Häutung und Metamorphose koordiniert. Der andere ist HNF4, ein konservierter Regulator des Fettstoffwechsels. Im L3-Darm wird die Ecdysone-Signalgebung aktiviert, genau in dem Moment, in dem die Gene für Fettverarbeitung hochgefahren werden. Wenn die Forschenden die Ecdysone-Funktion gezielt in Darmzellen blockierten, trat der normale Anstieg der Gene des Lipidstoffwechsels nicht auf. Fett sammelte sich im Darm an, während die Werte im Kreislauf sanken, was zeigte, dass der Darm Lipide nicht mehr effizient exportieren konnte.
Eine Partnerschaft für Wachstum und Energiespeicherung
HNF4 erweist sich als wichtiger Partner in diesem Prozess. Seine Aktivität steigt in Darmregionen der Larve, die fettreich sind, und nahezu die Hälfte der Fettstoffwechselgene, die in L3 ansteigen, sind für ihre volle Induktion auf HNF4 angewiesen. Das Stummschalten von HNF4 im Darm führte zum gleichen Muster wie bei gestörter Ecdysone-Signalgebung: Fett blieb in den intestinalen Zellen gefangen, zirkulierende Lipide sanken, und der gesamte Körperfettgehalt nach dem L3-Stadium war reduziert. Die Daten legen nahe, dass Ecdysone HNF4-Level erhöht, welches wiederum eine Reihe von Genen aktiviert, die den Darm in einen leistungsstarken Kanal für Nahrungsfett verwandeln und den Export an den Rest des Körpers gegenüber lokaler Speicherung priorisieren. Allein HNF4 kann jedoch nicht vollständig kompensieren, wenn Ecdysone blockiert ist, was darauf hindeutet, dass mehrere hormongetriebene Wege gemeinsam diesen metabolischen Umschaltpunkt gestalten.
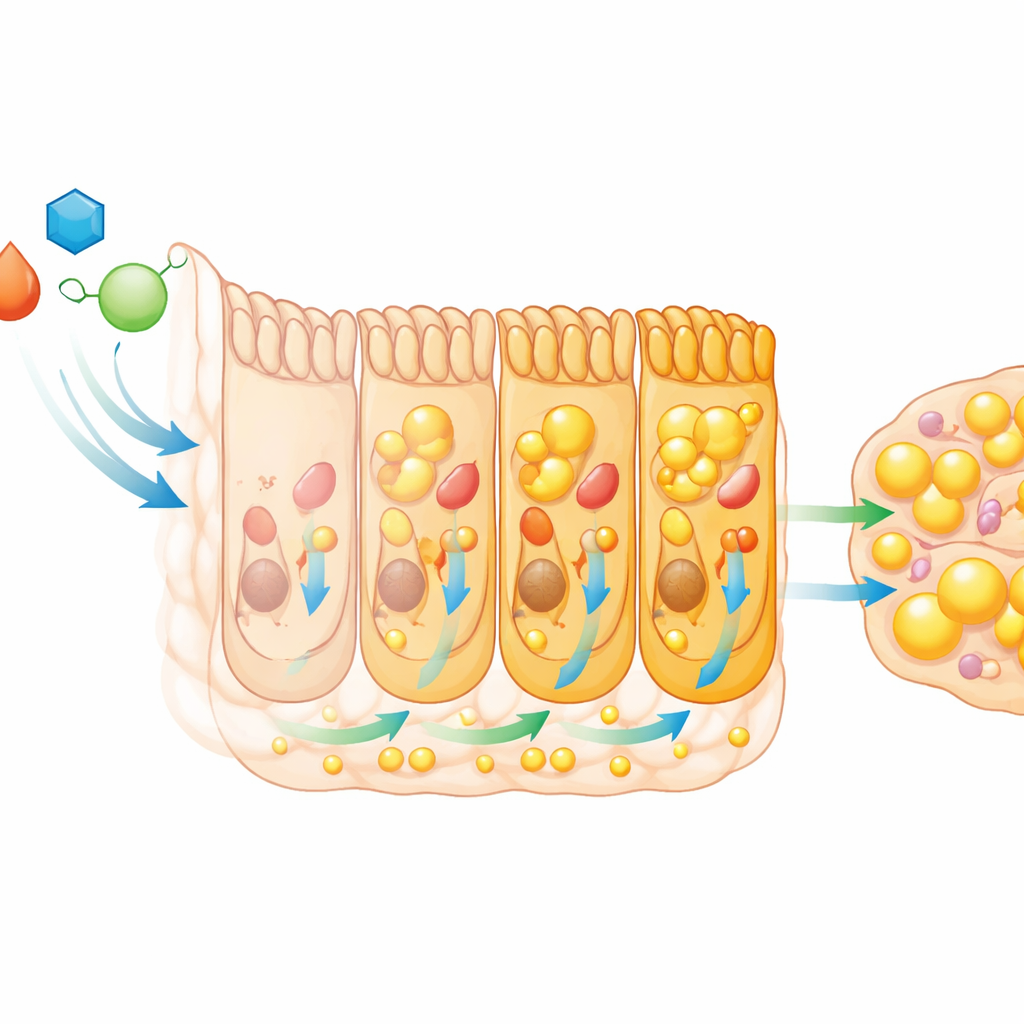
Vom juvenilen Darm zum Erfolg im Erwachsenenalter
Die Folgen dieses flüchtigen intestinalen Programms reichen weit über das Larvenstadium hinaus. Wenn Ecdysone oder HNF4 im Darm beeinträchtigt waren, wuchsen die Larven in L3 langsamer, akkumulierten weniger Protein und erreichten die für die Metamorphose erforderliche Größe später, wodurch ihre Verwandlung verzögert wurde. Erwachsene, die aus Larven ohne angemessene Darmumgestaltung hervorgingen, schlüpften kleiner, schlanker und mit reduzierten Fettreserven. Diese Erwachsenen waren empfindlicher gegenüber Austrocknung und hatten bei Weibchen kleinere Ovarien und produzierten in der frühen Lebensphase weniger Eier. Somit füllt ein kurzes Zeitfenster gesteigerten Darmstoffwechsels in der Jugend den Körper mit den Materialien, die nötig sind, um einen robusten Erwachsenen aufzubauen, Umweltstress zu widerstehen und sich schnell fortzupflanzen.
Warum das über Fruchtfliegen hinaus wichtig ist
Die Arbeit zeigt, dass frühzeitige Veränderungen in einem einzelnen Organ Wachstum, das Timing von pubertätsähnlichen Übergängen und die spätere Fitness prägen können. Bei Drosophila treibt ein hormongeführter Schub der Darmaktivität während eines engen Entwicklungsfensters einen letzten Wachstumsschub an und füllt Energiespeicher, die später die Wasserdichtigkeit des Körpers und die Eiproduktion unterstützen. Da viele derselben molekularen Akteure und Darmfunktionen bei Säugetieren, einschließlich des Menschen, konserviert sind, unterstreichen diese Befunde, wie vorübergehende Verschiebungen in Ernährung und Stoffwechsel während der Kindheit langfristige Folgen für Gesundheit und Krankheitsrisiken über die Lebensspanne hinweg haben könnten.
Zitation: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
Schlüsselwörter: Entwicklung von Drosophila, Darmstoffwechsel, Fettverdauung, Steroidhormone, jugendliches Wachstum