Clear Sky Science · nl
Tijdelijke herprogrammering van darmmetabolisme ondersteunt juveniele groei en volwassen fitheid in Drosophila
Hoe groeiende darmen een heel leven vormen
De kindertijd is een periode van snelle groei, en dat geldt voor fruitvliegjes net zo goed als voor mensen. Deze studie onderzoekt hoe de darm van een jong dier kortstondig in een "hoge versnelling" schakelt om een laatste groeispurt van brandstof te voorzien — en hoe die kortdurende verandering blijvende sporen nalaat in de gezondheid van volwassenen. Door de ontwikkeling bij de fruitvlieg Drosophila te volgen, laten de auteurs een tijdelijke stimulans van het intestinale metabolisme zien die juvenielen helpt snel te groeien, energie op te slaan, harde omgevingen te doorstaan en zich later succesvol voort te planten.
Een plotselinge sprint in een kort leven
Fruitvliegen doorlopen drie larvale stadia voordat ze zich omvormen tot volwassenen. De onderzoekers volgden lichaamsgrootte en lichaamschemie gedurende deze stadia en ontdekten dat de groei niet gelijkmatig verloopt. In plaats daarvan versnelt ze dramatisch halverwege het larvale leven, in het laatste stadium dat bekendstaat als L3. Binnen slechts een paar dagen nemen larvaire volume en belangrijke bouwstenen zoals eiwit, suikers en vetten vele malen toe, wat duidt op een intense groeispurt die grote hoeveelheden brandstof vereist.
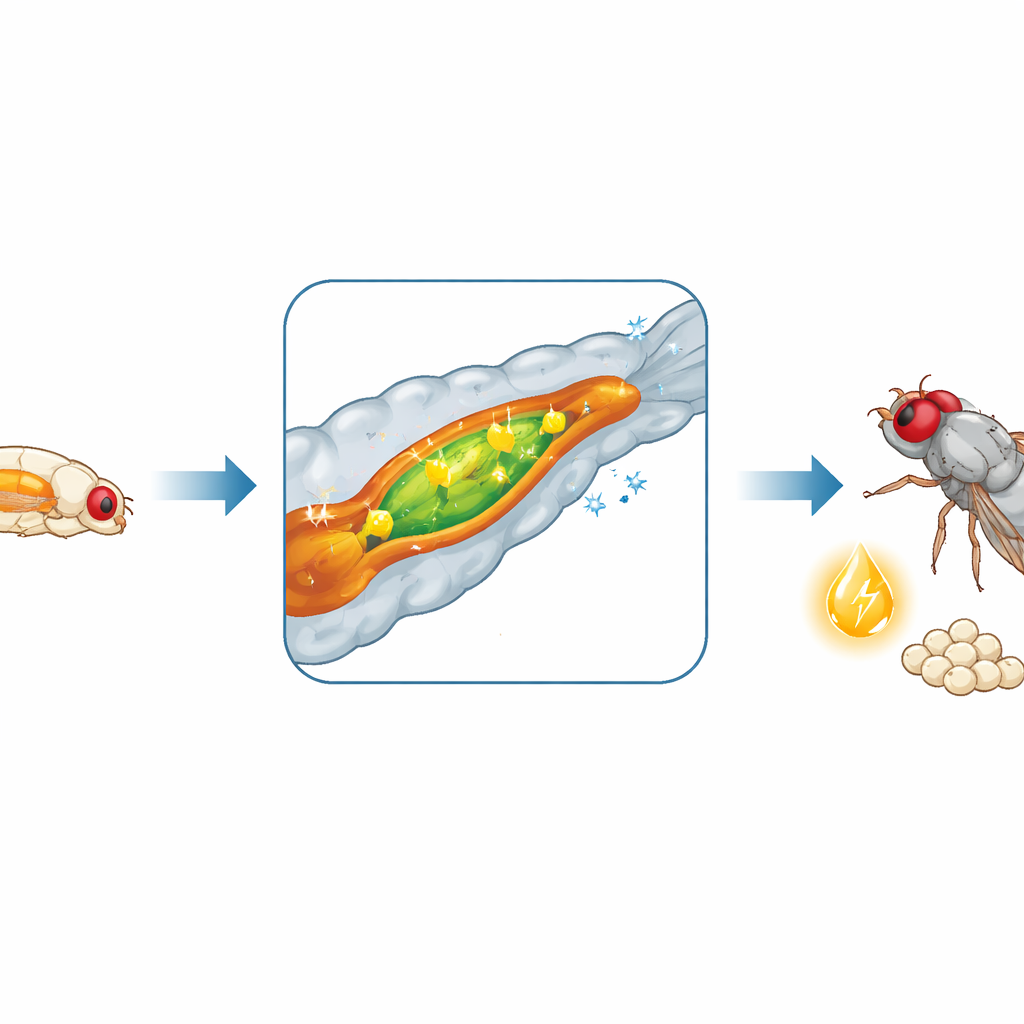
De darm verandert in een vetverwerkende fabriek
Aangezien groei afhankelijk is van voedsel, onderzocht het team of de darm zich op dit kritieke moment anders gedraagt. Door boodschapper-RNA van het midden-darm — het vlieg-equivalent van de dunne darm — te sequencen, ontdekten ze een ingrijpende herprogrammering van genactiviteit bij intrede in stadium L3. Honderden genen worden aan- of uitgezet, vooral die betrokken bij het afbreken en verwerken van voedingsvetten. Enzymen die vet verteren worden overvloediger en darmcellen vergroten hun vermogen om vet te verbranden, op te slaan en, cruciaal, naar de rest van het lichaam te exporteren. Metingen van darmenzymen en metabolieten bevestigden dat vetvertering en -mobilisatie toenemen in L3-larven, en circulerend vet in de bloedachtige vloeistof stijgt overeenkomstig. Ook de koolhydraatvertering neemt toe, wat deze energietoename verder voedt.
Hormonen die de darm vertellen wanneer te schakelen
De timing van deze intestinale make-over is niet willekeurig. Twee nucleaire receptoren — eiwitten die genen aan- of uitzetten als reactie op hormonale signalen — spelen centrale rollen. De ene is de receptor voor het steroïde hormoon ecdysone, dat ontwikkelingsovergangen zoals vervelling en metamorfose coördineert. De andere is HNF4, een geconserveerde regulator van vetmetabolisme. In de L3-darm wordt ecdysone-signaalvoering aangezet juist wanneer de vetverwerkende genen geïnduceerd worden. Wanneer de onderzoekers ecdysonefunctie specifiek in intestinale cellen blokkeerden, trad de normale stijging van genen voor lipidemetabolisme niet op. Vet stapelde zich op in de darm terwijl de niveaus in de circulatie daalden, wat aantoonde dat de darm lipiden niet langer efficiënt naar buiten kon exporteren.
Een partnerschap voor groei en energieopslag
HNF4 komt naar voren als een sleutelpartner in dit proces. De activiteit neemt toe in darmregio's van de larve die rijk zijn aan lipiden, en bijna de helft van de vetmetabolismegenen die in L3 stijgen zijn afhankelijk van HNF4 voor volledige inductie. Het stilleggen van HNF4 in de darm leidde tot hetzelfde patroon als bij verstoorde ecdysone-signaling: vet werd gevangen in intestinale cellen, circulerende lipiden daalden, en de totale lichaamsvetreserve na het L3-stadium nam af. De gegevens suggereren dat ecdysone HNF4-niveaus verhoogt, die op hun beurt een batterij van genen activeert die de darm transformeren tot een krachtig kanaal voor dieetvet, waarbij export naar de rest van het lichaam prioriteit krijgt boven lokale opslag. Toch kan HNF4 alleen onvoldoende compenseren als ecdysone geblokkeerd is, wat aangeeft dat meerdere hormoongestuurde routes gezamenlijk deze metabole schakelaar vormgeven.
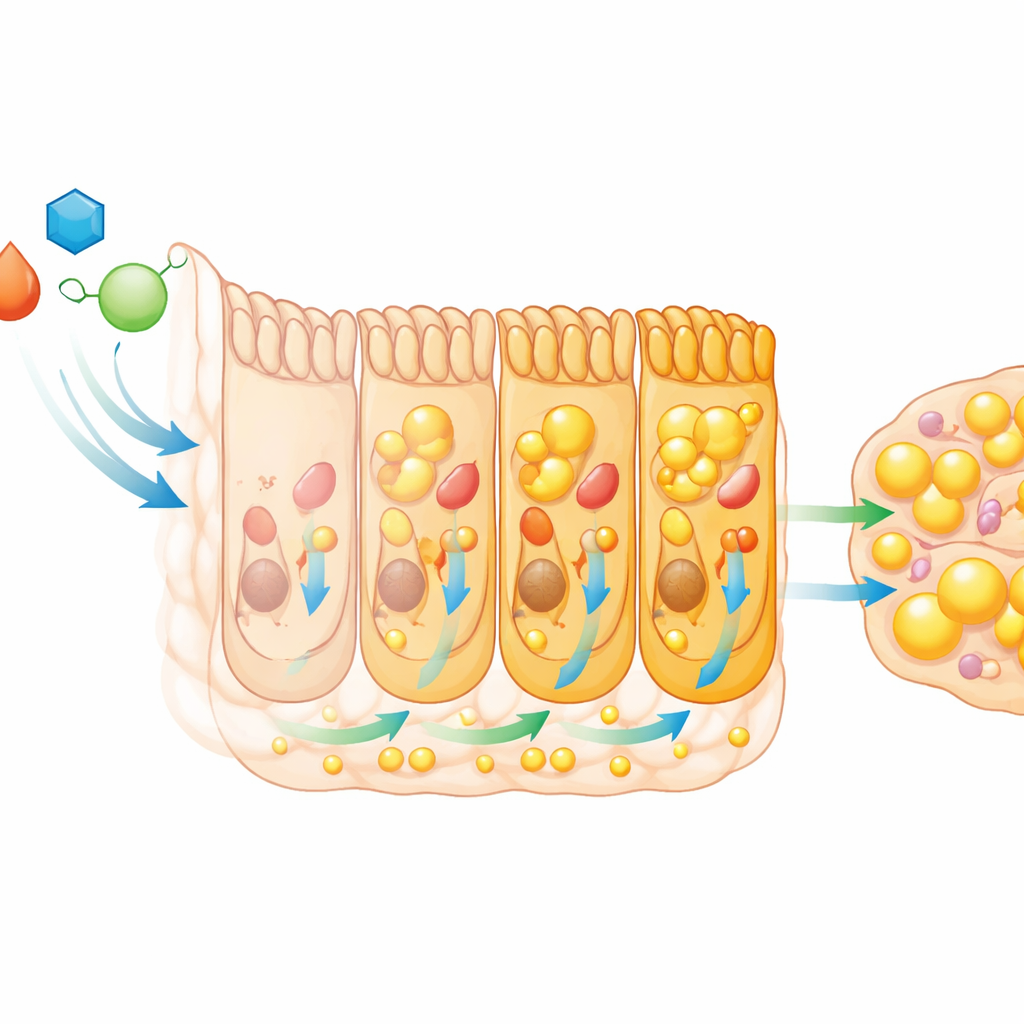
Van juveniele darm naar volwassen succes
De gevolgen van dit vluchtige intestinale programma reiken veel verder dan het larvale stadium. Wanneer ecdysone of HNF4 in de darm waren aangetast, groeiden larven trager tijdens L3, stapelden zich minder eiwit op en bereikten ze later de grootte die nodig is voor metamorfose, waardoor hun transformatie werd vertraagd. Volwassenen die uit larven met gebrekkige darmhermodellering voortkwamen, kwamen tevoorschijn als kleiner, magerder en met verminderde vetreserves. Deze volwassenen waren gevoeliger voor uitdroging en hadden bij vrouwtjes kleinere eierstokken en produceerden in het vroege leven minder eieren. Zo voorziet een korte periode van verhoogd darmmetabolisme in de jeugd het lichaam van het materiaal dat nodig is om een robuuste volwassene te bouwen, om milieu-stress te weerstaan en zich snel voort te planten.
Waarom dit belang heeft buiten fruitvliegen
Dit werk laat zien dat vroeg-leven veranderingen in een enkel orgaan groei, de timing van puberteitsachtige overgangen en fitheid later in het leven kunnen vormgeven. In Drosophila drijft een hormoon-gestuurde uitbarsting van darmactiviteit tijdens een nauwe ontwikkelingsvenster een laatste groeispurt aan en vult energievoorraden die later de waterdichtheid van het lichaam en de eiproductie ondersteunen. Omdat veel van dezelfde moleculaire spelers en darmgedragingen bewaard zijn in zoogdieren, inclusief mensen, benadrukken deze bevindingen hoe tijdelijke verschuivingen in voeding en metabolisme tijdens de kindertijd langdurige gevolgen kunnen hebben voor gezondheid en ziektegevoeligheid gedurende het leven.
Bronvermelding: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
Trefwoorden: Ontwikkeling van Drosophila, darmmetabolisme, vetvertering, steroïde hormonen, juveniele groei