Clear Sky Science · fr
Remodelage transitoire du métabolisme intestinal soutient la croissance juvénile et la forme adulte chez Drosophila
Comment des intestins en croissance façonnent toute une vie
L’enfance est une période de croissance rapide, et cela vaut pour les mouches des fruits autant que pour les humains. Cette étude explore comment l’intestin d’un jeune animal passe brièvement en « haute vitesse » pour alimenter un dernier pic de croissance — et comment ce changement éphémère laisse des traces durables sur la santé à l’âge adulte. En suivant le développement chez la mouche du vinaigre Drosophila, les auteurs révèlent un renforcement temporaire du métabolisme intestinal qui aide les juvéniles à croître rapidement, stocker de l’énergie, résister à des environnements hostiles et se reproduire avec succès à l’âge adulte.
Un sprint soudain dans une vie brève
Les mouches passent par trois stades larvaires avant de se transformer en adultes. Les chercheurs ont suivi la taille corporelle et la composition chimique au cours de ces stades et ont constaté que la croissance n’est pas régulière. Elle s’accélère de façon spectaculaire à mi-parcours de la vie larvaire, lors du dernier stade appelé L3. En l’espace de quelques jours seulement, le volume larvaire et des éléments constitutifs clés comme les protéines, les sucres et les lipides se multiplient, signalant un pic de croissance intense qui exige d’importantes quantités de carburant.
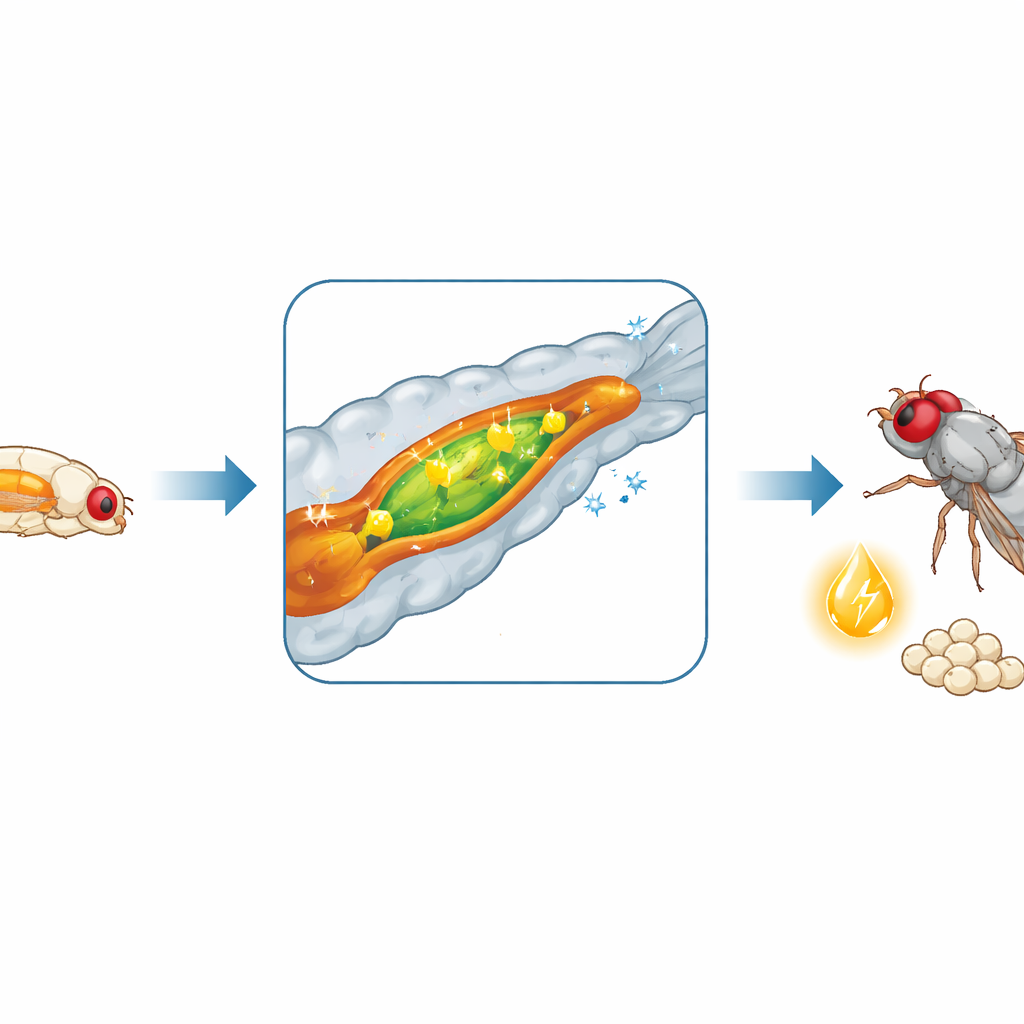
L’intestin se transforme en usine de traitement des graisses
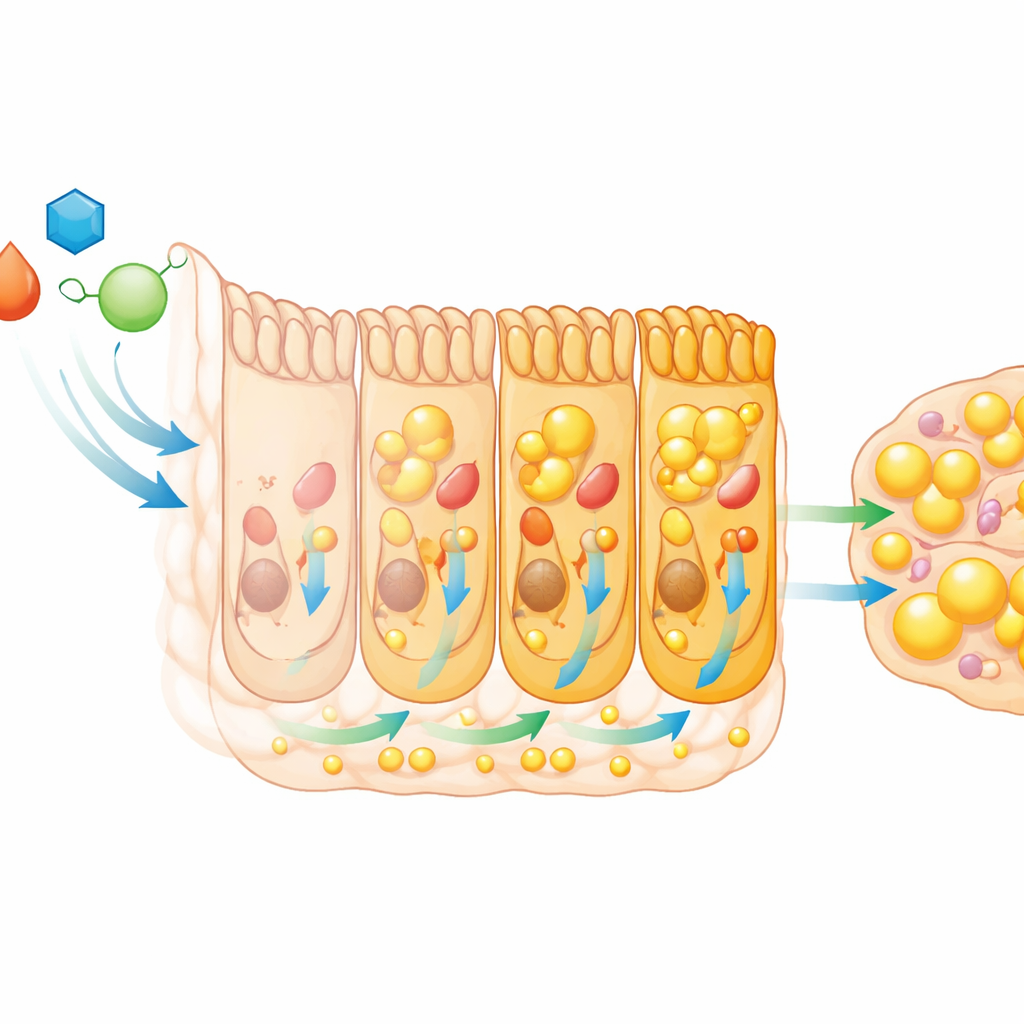
Parce que la croissance dépend de l’alimentation, l’équipe a examiné si l’intestin modifie son comportement à ce moment critique. En séquençant l’ARN messager du mésentère — l’équivalent chez la mouche de l’intestin grêle — ils ont découvert une reprogrammation massive de l’activité génique à l’entrée en stade L3. Des centaines de gènes s’activent ou s’éteignent, en particulier ceux impliqués dans la dégradation et la gestion des lipides alimentaires. Les enzymes digestives des graisses deviennent plus abondantes, et les cellules intestinales augmentent leur capacité à brûler, stocker et, surtout, exporter les lipides vers le reste du corps. Des mesures des enzymes et des métabolites intestinaux ont confirmé que la digestion et la mobilisation des graisses s’intensifient chez les larves L3, et que les lipides circulants dans le fluide analogue au sang augmentent en conséquence. La digestion des glucides s’amplifie également, alimentant davantage cette poussée d’énergie.
Des hormones qui indiquent à l’intestin quand changer de vitesse
Le moment de cette métamorphose intestinale n’est pas aléatoire. Deux récepteurs nucléaires — des protéines qui activent ou répriment des gènes en réponse à des signaux hormonaux — jouent des rôles centraux. L’un est le récepteur de l’hormone stéroïde ecdysone, qui coordonne les transitions développementales comme la mue et la métamorphose. L’autre est HNF4, un régulateur conservé du métabolisme lipidique. Dans l’intestin L3, la signalisation par l’ecdysone s’active au même moment que l’induction des gènes de gestion des lipides. Lorsque les chercheurs ont bloqué spécifiquement la fonction de l’ecdysone dans les cellules intestinales, la montée normale des gènes du métabolisme lipidique n’a pas eu lieu. Les graisses s’accumulaient dans l’intestin tandis que les niveaux circulants chutaient, montrant que l’intestin ne pouvait plus exporter les lipides efficacement.
Un partenariat pour la croissance et le stockage d’énergie
HNF4 apparaît comme un partenaire clé de ce processus. Son activité augmente dans des régions de l’intestin larvaire riches en lipides, et près de la moitié des gènes du métabolisme lipidique induits en L3 dépendent d’HNF4 pour leur induction complète. L’inhibition d’HNF4 dans l’intestin a conduit au même profil observé lors de la perturbation de la signalisation par l’ecdysone : les graisses restaient piégées dans les cellules intestinales, les lipides circulants diminuaient et la masse grasse corporelle après le stade L3 était réduite. Les données suggèrent que l’ecdysone augmente les niveaux d’HNF4, qui active à son tour un ensemble de gènes transformant l’intestin en un conduit puissant pour les lipides alimentaires, priorisant leur exportation vers le reste du corps plutôt que leur stockage local. Pourtant, HNF4 seul ne peut pas compenser entièrement si l’ecdysone est bloquée, ce qui indique que plusieurs voies hormonales conjuguées façonnent ce basculement métabolique.
De l’intestin juvénile au succès adulte
Les conséquences de ce programme intestinal éphémère vont bien au-delà du stade larvaire. Lorsque l’ecdysone ou HNF4 étaient altérés dans l’intestin, les larves croissaient plus lentement pendant le stade L3, accumulaient moins de protéines et atteignaient plus tard la taille requise pour la métamorphose, retardant leur transformation. Les adultes issus de larves dépourvues du remodelage intestinal adéquat apparaissaient plus petits, plus maigres et avec des réserves de graisse réduites. Ces adultes étaient plus sensibles à la dessiccation et, chez les femelles, avaient des ovaires plus petits et produisaient moins d’œufs en début de vie. Ainsi, une fenêtre brève d’un métabolisme intestinal renforcé chez les jeunes approvisionne l’organisme en matériaux nécessaires pour construire un adulte robuste, résister aux stress environnementaux et se reproduire rapidement.
Pourquoi cela importe au-delà des mouches des fruits
Ce travail montre que des changements en début de vie dans un seul organe peuvent façonner la croissance, le calendrier des transitions similaires à la puberté et la forme physique ultérieure. Chez Drosophila, une poussée d’activité intestinale guidée par des hormones durant une fenêtre développementale étroite alimente un dernier pic de croissance et remplit les réserves énergétiques qui soutiendront plus tard l’imperméabilisation du corps et la production d’œufs. Parce que beaucoup des mêmes acteurs moléculaires et comportements intestinaux sont conservés chez les mammifères, y compris les humains, ces résultats soulignent comment des variations temporaires de la nutrition et du métabolisme pendant l’enfance pourraient avoir des conséquences à long terme pour la santé et le risque de maladie au cours de la vie.
Citation: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
Mots-clés: développement de Drosophila, métabolisme intestinal, digestion des lipides, hormones stéroïdes, croissance juvénile