Clear Sky Science · ru
Преходная перестройка метаболизма кишечника поддерживает ювенильный рост и взрослую приспособленность у Drosophila
Как растущий кишечник формирует всю жизнь
Детство — время стремительного роста, и это так же верно для плодовых мух, как и для людей. В этом исследовании изучают, как кишечник молодого животного на короткое время включается на «высшую передачу», чтобы обеспечить завершающий скачок роста — и как это кратковременное изменение оставляет долговременные следы на здоровье взрослой особи. Отслеживая развитие у плодовой мухи Drosophila, авторы выявили временное усиление кишечного метаболизма, которое помогает молодым особям быстро расти, запасать энергию, выдерживать суровые условия и успешно размножаться во взрослом возрасте.
Внезапный спринт в короткой жизни
Плодовые мухи проходят три личиночных стадии, прежде чем превратиться во взрослую особь. Исследователи отслеживали размер тела и состав тела на протяжении этих стадий и обнаружили, что рост не равномерный. Вместо этого он резко ускоряется примерно в середине личиночной жизни, на последней стадии, известной как L3. В течение всего нескольких дней объем личинки и ключевые строительные блоки — белки, сахара и жиры — увеличиваются в разы, что указывает на интенсивный скачок роста, требующий больших объемов топлива.
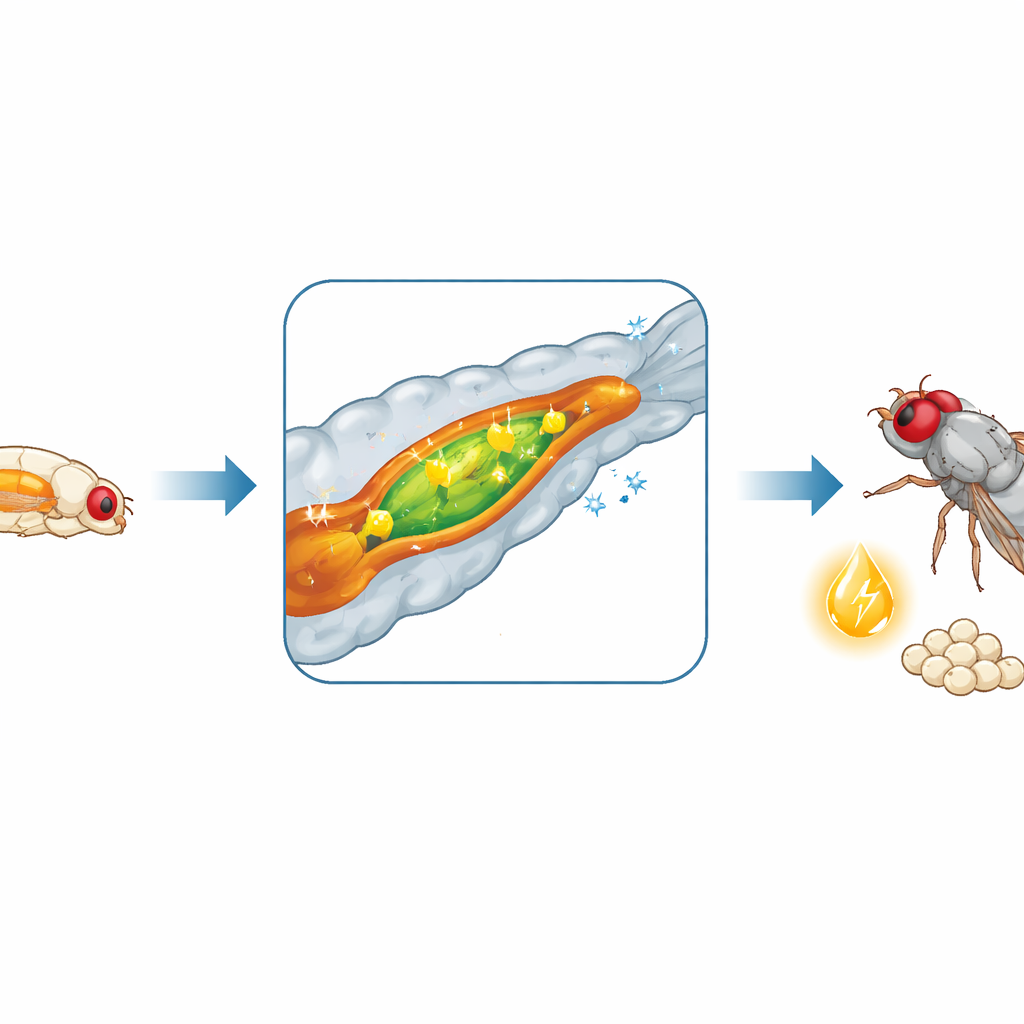
Кишечник превращается в фабрику по переработке жиров
Поскольку рост зависит от пищи, команда проверила, меняется ли поведение кишечника в это критическое время. Секвенируя матричную РНК из средней кишки — эквивалента тонкой кишки у мух — они обнаружили масштабную перепрограммировку активности генов при переходе личинок в стадию L3. Сотни генов включаются или выключаются, особенно те, которые участвуют в расщеплении и обработке пищевых жиров. Ферменты, переваривающие жиры, становятся более многочисленными, и клетки кишечника увеличивают способность окислять, запасать и, что важно, экспортировать жиры в остальное тело. Измерения активности кишечных ферментов и метаболитов подтвердили, что переваривание и мобилизация жиров усиливаются у личинок L3, а уровень циркулирующих липидов в гемолимфе возрастает соответственно. Переваривание углеводов также усиливается, дополнительно подпитывая этот энергетический всплеск.
Гормоны, которые подсказывают кишечнику, когда менять передачу
Время этой кишечной перестройки не случайно. Две ядерные рецепторные белковые молекулы — белки, которые включают или выключают гены в ответ на гормональные сигналы — играют центральную роль. Один из них — рецептор для стероидного гормона экдизона, который координирует переходы развития, такие как линька и метаморфоз. Другой — HNF4, консервативный регулятор липидного метаболизма. В кишечнике на стадии L3 сигнализация экдизона включается как раз в тот момент, когда индуцируются гены обработки жиров. Когда исследователи блокировали функцию экдизона специфически в кишечных клетках, нормальный подъём генов липидного метаболизма не происходил. Жир накапливался внутри кишечника, а уровни в циркуляции падали, что показало, что кишечник больше не мог эффективно экспортировать липиды.
Партнёрство для роста и накопления энергии
HNF4 выступает ключевым партнёром в этом процессе. Его активность повышается в областях личиночного кишечника, богатых липидами, и почти половина генов липидного метаболизма, которые увеличиваются в L3, зависит от HNF4 для полного индукционного ответа. Подавление HNF4 в кишечнике приводило к той же картине, что и при нарушенной сигнализации экдизона: жир оставался захваченным в клетках кишечника, циркулирующие липиды снижались, а общий уровень жира в теле после стадии L3 уменьшался. Данные предполагают, что экдизон повышает уровни HNF4, который, в свою очередь, активирует набор генов, превращающих кишечник в мощный канал для диетических жиров, отдающий приоритет их экспорту в остальное тело над местным накоплением. Тем не менее HNF4 сам по себе не может полностью компенсировать блокировку экдизона, что указывает на то, что несколько гормонально регулируемых путей совместно формируют этот метаболический переключатель.
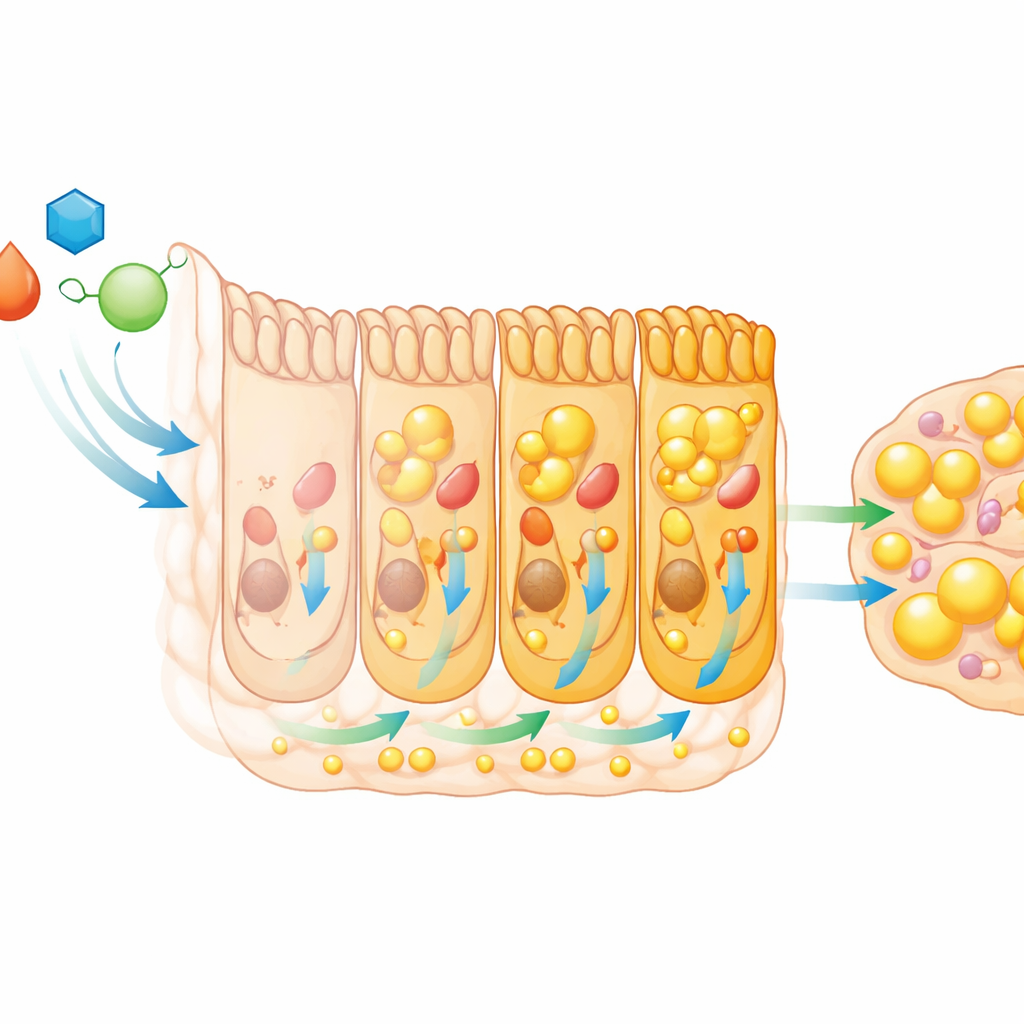
От ювенильного кишечника к взрослому успеху
Последствия этой мимолётной кишечной программы простираются далеко за пределы личиночной стадии. Когда экдизон или HNF4 были нарушены в кишечнике, личинки росли медленнее в течение L3, накапливали меньше белка и достигали размера, необходимого для метаморфоза, позже, задерживая превращение. Взрослые особи, развившиеся из личинок с нарушенной кишечной перестройкой, вылуплялись меньшими, более худыми и с уменьшенными жировыми резервами. Эти взрослые были более чувствительны к высыханию, а у самок отмечались меньшие яичники и уменьшенное число откладываемых яиц в ранней жизни. Таким образом, короткое окно усиленного кишечного метаболизма в молодости наполняет организм материалом, необходимым для построения крепкой взрослой особи, сопротивления экологическому стрессу и быстрого размножения.
Почему это важно не только для плодовых мух
Эта работа показывает, что изменения в одном органе на раннем этапе жизни могут определять рост, время переходов, похожих на половое созревание, и приспособленность в будущем. У Drosophila гормонально управляемый всплеск активности кишечника в узком окне развития обеспечивает завершающий скачок роста и наполняет энергетические запасы, которые позже поддерживают водонепроницаемость тела и продукцию яиц. Поскольку многие те же молекулярные участники и поведенческие реакции кишечника сохраняются у млекопитающих, включая человека, эти результаты подчёркивают, как временные сдвиги в питании и метаболизме в детстве могут иметь долгосрочные последствия для здоровья и риска заболеваний на протяжении жизни.
Цитирование: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
Ключевые слова: развитие Drosophila, метаболизм кишечника, переваривание липидов, стероидные гормоны, ювенильный рост