Clear Sky Science · es
Remodelado transitorio del metabolismo intestinal que sostiene el crecimiento juvenil y la aptitud adulta en Drosophila
Cómo los intestinos en crecimiento moldean toda una vida
La infancia es una etapa de crecimiento rápido, y eso es tan cierto para las moscas de la fruta como para los humanos. Este estudio analiza cómo el intestino de un animal joven cambia brevemente a una “marcha alta” para impulsar un último estirón de crecimiento —y cómo ese cambio de corta duración deja huellas duraderas en la salud adulta. Mediante el seguimiento del desarrollo en la mosca Drosophila, los autores revelan un aumento temporal del metabolismo intestinal que ayuda a los juveniles a crecer rápido, almacenar energía, resistir ambientes adversos y reproducirse con éxito en la edad adulta.
Una carrera repentina en una vida breve
Las moscas de la fruta atraviesan tres estadios larvales antes de transformarse en adultas. Los investigadores siguieron el tamaño corporal y la química del cuerpo a lo largo de estos estadios y hallaron que el crecimiento no es constante. En lugar de eso, se acelera de forma dramática a mitad de la vida larval, en el último estadio conocido como L3. En apenas un par de días, el volumen larval y bloques constructores clave como proteínas, azúcares y grasas se multiplican muchas veces, lo que señala un estallido de crecimiento intenso que requiere grandes cantidades de combustible.
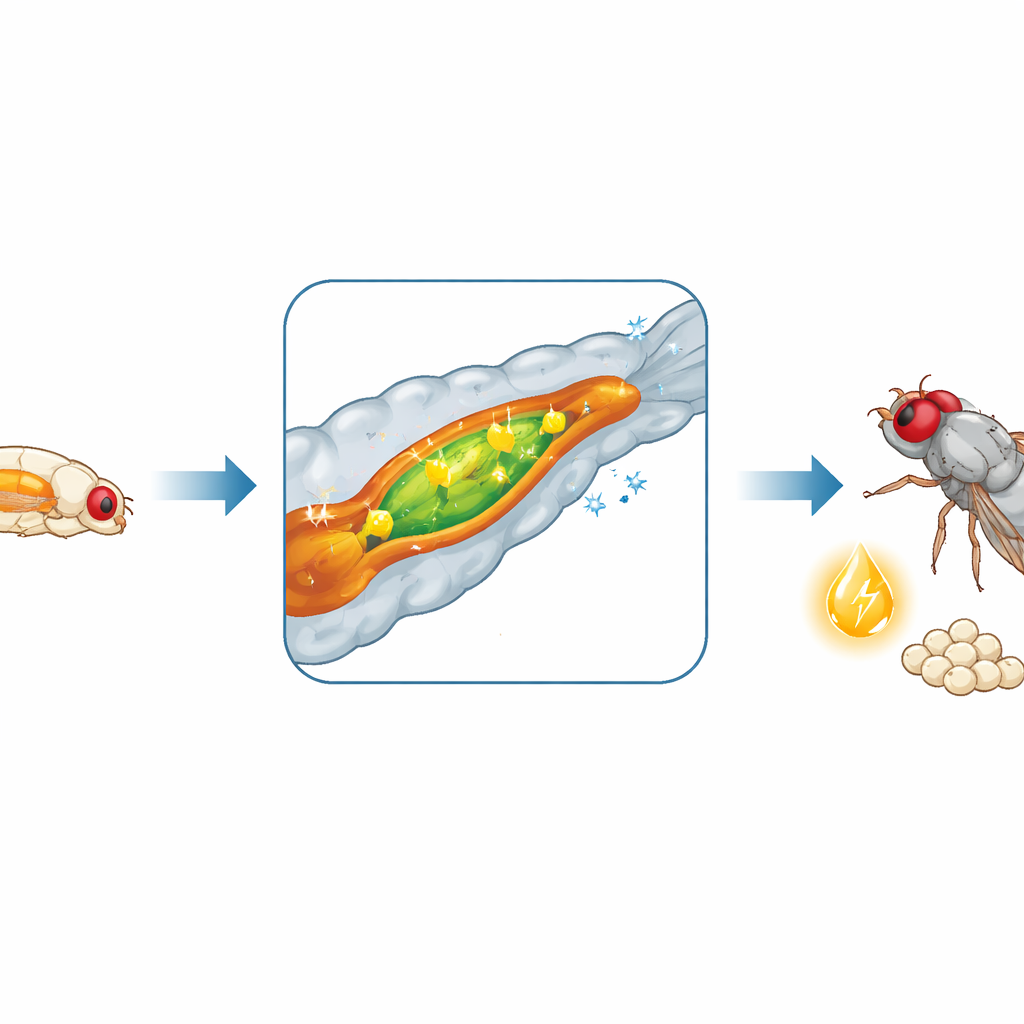
El intestino se convierte en una fábrica de procesamiento de grasas
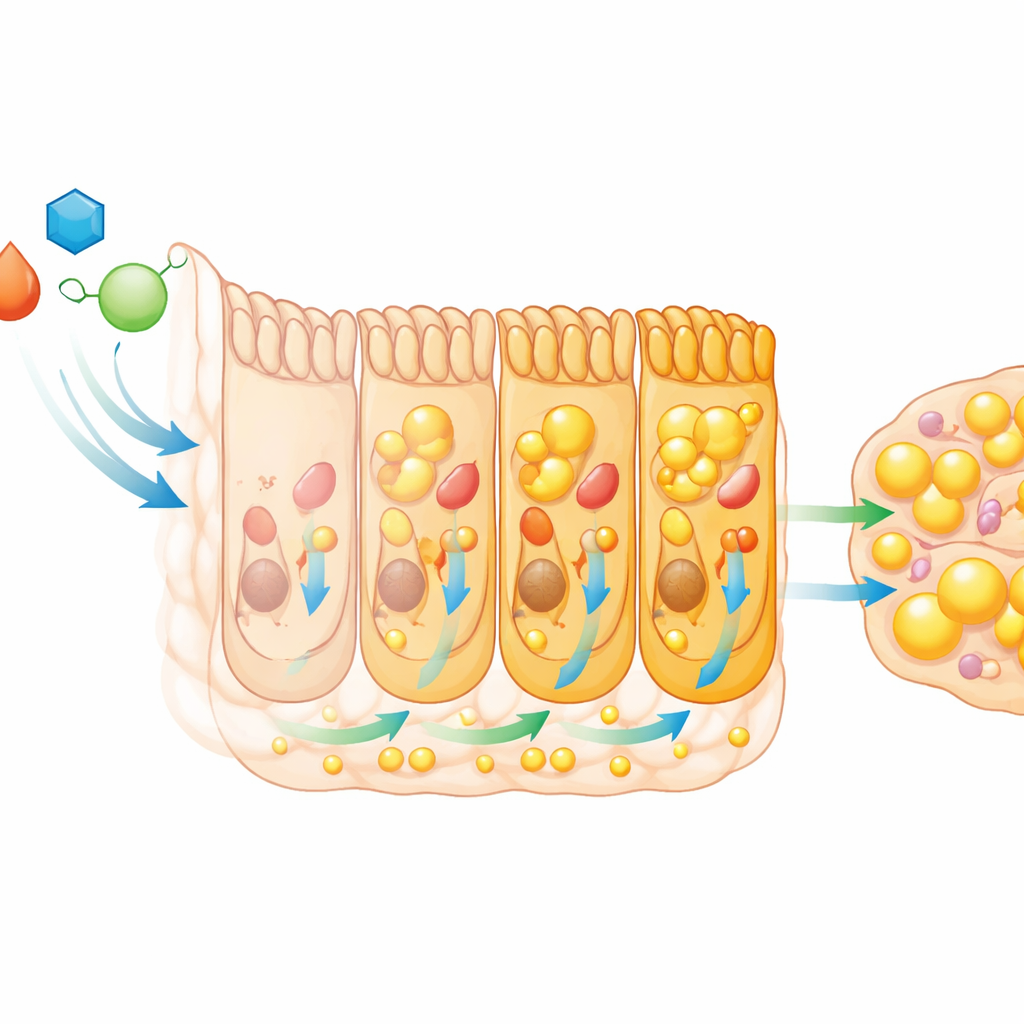
Dado que el crecimiento depende de la comida, el equipo examinó si el intestino cambia su comportamiento en este momento crítico. Al secuenciar ARN mensajero del intestino medio —el equivalente al intestino delgado en la mosca— descubrieron una reprogramación extensa de la actividad génica cuando las larvas entran en L3. Cientos de genes se activan o se apagan, especialmente aquellos implicados en descomponer y manejar las grasas dietéticas. Las enzimas que digieren grasas se vuelven más abundantes, y las células intestinales aumentan su capacidad para quemar, almacenar y, crucialmente, exportar grasas al resto del cuerpo. Las mediciones de enzimas y metabolitos intestinales confirmaron que la digestión y movilización de lípidos se intensifican en las larvas L3, y las grasas circulantes en el fluido similar a la sangre aumentan en consecuencia. La digestión de carbohidratos también se incrementa, alimentando aún más este impulso energético.
Hormonas que le dicen al intestino cuándo cambiar de marcha
El momento de esta remodelación intestinal no es aleatorio. Dos receptores nucleares —proteínas que encienden o apagan genes en respuesta a señales hormonales— desempeñan papeles centrales. Uno es el receptor de la hormona esteroide ecdysone, que coordina transiciones del desarrollo como la muda y la metamorfosis. El otro es HNF4, un regulador conservado del metabolismo lipídico. En el intestino L3, la señalización por ecdysone se activa justo cuando se inducen los genes de manejo de grasas. Cuando los investigadores bloquearon la función de ecdysone específicamente en las células intestinales, el aumento normal de los genes de metabolismo lipídico no se produjo. La grasa se acumuló dentro del intestino mientras que los niveles en la circulación cayeron, mostrando que el intestino ya no podía exportar lípidos de forma eficiente.
Una asociación para el crecimiento y el almacenamiento de energía
HNF4 surge como un socio clave en este proceso. Su actividad aumenta en regiones del intestino larval ricas en lípidos, y casi la mitad de los genes de metabolismo lipídico que se elevan en L3 dependen de HNF4 para su inducción completa. Silenciar HNF4 en el intestino condujo al mismo patrón observado con la señalización de ecdysone alterada: la grasa quedó atrapada en las células intestinales, las lipoproteínas circulantes descendieron y la grasa corporal total después del estadio L3 se redujo. Los datos sugieren que ecdysone aumenta los niveles de HNF4, que a su vez activa una batería de genes que transforman el intestino en un potente conducto para la grasa dietética, priorizando la exportación al resto del cuerpo sobre el almacenamiento local. Sin embargo, HNF4 por sí solo no puede compensar completamente si ecdysone está bloqueada, lo que indica que múltiples vías dirigidas por hormonas configuran conjuntamente este cambio metabólico.
Del intestino juvenil al éxito adulto
Las consecuencias de este programa intestinal fugaz se extienden mucho más allá del estadio larval. Cuando ecdysone o HNF4 se vieron afectados en el intestino, las larvas crecieron más despacio durante L3, acumularon menos proteína y alcanzaron el tamaño necesario para la metamorfosis más tarde, retrasando su transformación. Los adultos que se desarrollaron a partir de larvas sin una remodelación intestinal adecuada emergieron más pequeños, delgados y con reservas de grasa reducidas. Estos adultos fueron más sensibles a la desecación y, en las hembras, tuvieron ovarios más pequeños y produjeron menos huevos en la vida temprana. Así, una ventana breve de metabolismo intestinal potenciado en la juventud provee al cuerpo del material necesario para construir un adulto robusto, resistir el estrés ambiental y reproducirse rápidamente.
Por qué esto importa más allá de las moscas de la fruta
Este trabajo muestra que los cambios en la primera etapa de la vida en un solo órgano pueden moldear el crecimiento, el momento de transiciones similares a la pubertad y la aptitud posterior. En Drosophila, un estallido de actividad intestinal guiado por hormonas durante una ventana de desarrollo estrecha impulsa un último estirón de crecimiento y llena las reservas energéticas que luego sostienen la impermeabilización del cuerpo y la producción de huevos. Dado que muchos de los mismos actores moleculares y comportamientos intestinales se conservan en mamíferos, incluidos los humanos, estos hallazgos subrayan cómo los cambios temporales en la nutrición y el metabolismo durante la infancia podrían tener consecuencias a largo plazo para la salud y el riesgo de enfermedad a lo largo de la vida.
Cita: Lefranc, C., Fichant, A. & Storelli, G. Transient remodeling of gut metabolism supports juvenile growth and adult fitness in Drosophila. Nat Commun 17, 3458 (2026). https://doi.org/10.1038/s41467-026-71776-3
Palabras clave: Desarrollo de Drosophila, metabolismo intestinal, digestión de lípidos, hormonas esteroides, crecimiento juvenil