Clear Sky Science · zh
通过单细胞转录组学解析脆弱拟杆菌与噬菌体的相互作用动力学
为何肠道内的微小战斗重要
我们的肠道栖息着无数细菌以及捕食它们的病毒。本研究聚焦于一种常见肠道细菌脆弱拟杆菌与攻击它的噬菌体之间的一场较量。通过同时观察成万计的单个细菌细胞,研究人员揭示了为何一些细菌成为牺牲品而另一些得以幸存并使群体恢复。这些隐藏的生存策略会影响肠道生态系统对病毒攻击的反应,也可能为未来的噬菌体疗法提供参考。
看单个细胞而非混浊的培养物
过去大多数关于细菌与其病毒的研究都在混合试管中进行,数百万个细胞的行为被平均在一起。那种方法掩盖了并非每个细胞都表现相同的事实。在这里,团队使用了一种称为微生物单细胞RNA测序的方法,读取大约5万个脆弱拟杆菌单细胞在暴露于从废水中新分离出的噬菌体后的基因活性。该方法使他们能够在同一培养物中区分被感染与未被感染的细胞,并观察在感染过程中宿主与病毒的活动如何变化。
重构看不见的感染时间线
尽管研究者只拍摄了一个时间点的快照,被感染的细胞却覆盖了疾病的多个不同阶段。通过比较它们的基因活性模式,团队将这些细胞按一个虚拟时间线排序,追踪感染的进程。在早期,病毒促使细菌增强基本的基因转录与蛋白质合成机器。中期时,宿主开启了提供DNA构件的基因,病毒很可能劫持这些构件以复制其基因组。在后期,宿主自身的转录信息大多消失,而用于组装新病毒颗粒和裂解细胞的病毒基因激增,标志着即将出现病毒子代的大量释放。
能够免疫攻击的隐性亚型
暴露于病毒的培养物中并非所有细胞都被感染。有相当一部分细胞保持未受影响,单细胞数据表明这并非偶然。该细菌天然会切换某些DNA开关,产生显示不同糖衣(称为荚膜)和不同表面纤维(或菌毛)的亚群。研究团队发现携带特定荚膜类型的细胞,尤其是标记为PSB和PSG的类型,比带有其他包膜的细胞更不易被感染。另一套由名为Tsr16的DNA开关控制的表面系统在高表达时也显著增强了保护作用,进一步降低了感染概率。
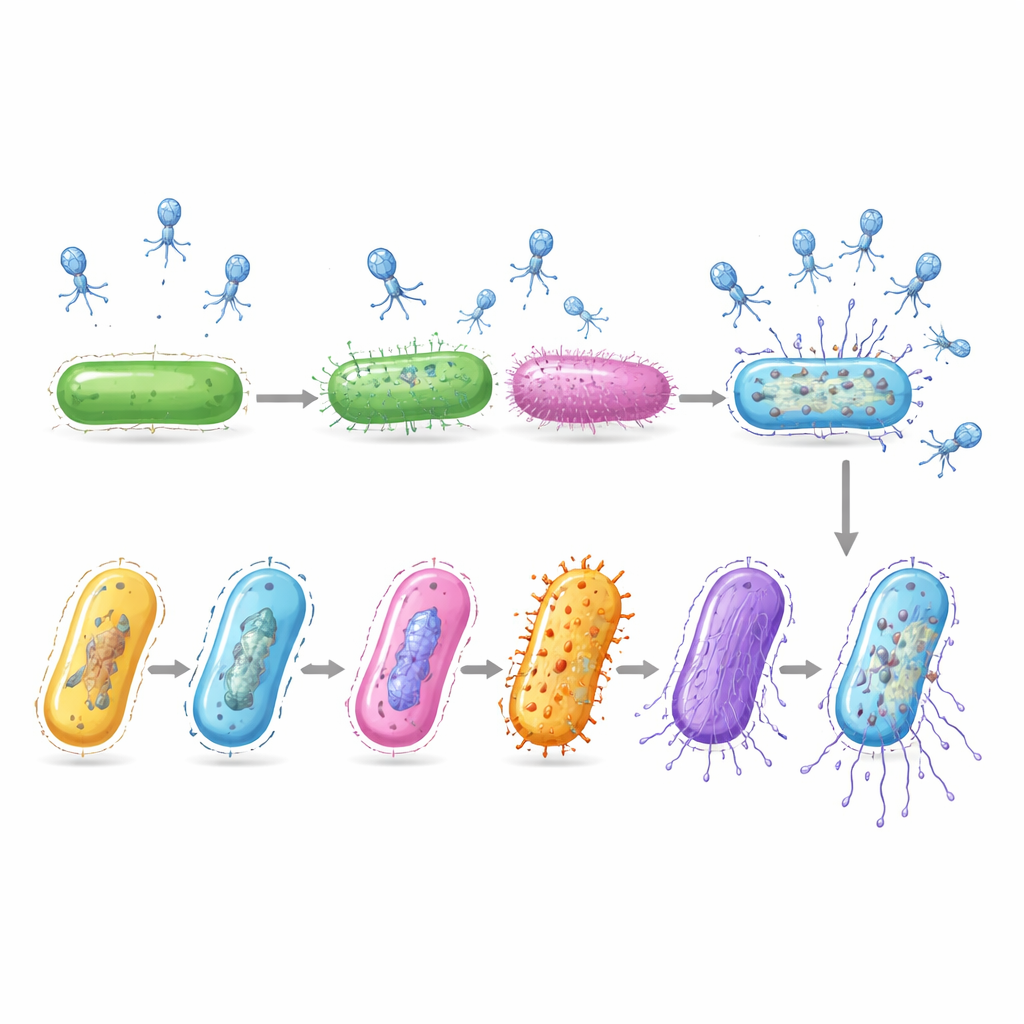
协同作用的多层防御
研究还考察了细菌内部已知的抗病毒工具,例如切割外来DNA的系统或自我牺牲以阻止感染的机制。单独来看,这些防御无法完全解释哪些细胞幸存。但当某些内部防御在同时携带保护性荚膜的细胞中激活时,感染几率几乎降为零。在使用被锁定只产生单一荚膜类型的菌株进行的独立生长实验中,携带PSG包被的细菌抵抗了噬菌体,而具有更脆弱包被的菌株被清除。对幸存细菌的后续DNA测序显示,抗性主要来自对这些已有保护性类型的选择,而非新突变的产生。
对我们的肠道和噬菌体应用的意义
对普通读者而言,主要信息是即使拥有相同基因,肠道细菌也并非长相或行为一致。通过不断混换表面特征与其他防御机制,它们形成了能够在突发病毒攻击中幸存并随后再度繁殖的小型亚群。这种内建的分散风险策略帮助脆弱拟杆菌在人体肠道的动荡环境中持续存在,也表明若要在医学上成功使用噬菌体,必须考虑到这些隐藏且难以消灭的亚群体。
引用: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
关键词: 噬菌体, 肠道微生物组, 脆弱拟杆菌, 单细胞测序, 细菌防御