Clear Sky Science · pt
Dinâmica das interações fago-hospedeiro em Bacteroides fragilis resolvida por transcriptômica de célula única
Por que pequenas batalhas intestinais importam
Nosso intestino abriga incontáveis bactérias e os vírus que as perseguem. Este estudo focaliza um desses duelos entre uma bactéria intestinal comum, Bacteroides fragilis, e um vírus que a infecta. Ao observar simultaneamente dezenas de milhares de células bacterianas individuais, os pesquisadores revelam por que algumas bactérias sucumbem enquanto outras permanecem seguras e permitem que a população se recupere. Esses truques de sobrevivência escondidos moldam como nosso ecossistema intestinal responde a ataques virais e podem ajudar a orientar futuras terapias com fagos.
Olhando para células únicas em vez de caldo turvo
A maior parte do trabalho anterior sobre bactérias e seus vírus foi feita em tubos de ensaio em volume, onde o comportamento de milhões de células é promediado. Essa abordagem oculta o fato de que nem toda célula se comporta da mesma forma. Aqui, a equipe usou um método chamado sequenciamento de RNA microbiano de célula única para ler quais genes estavam ativos em cerca de 50.000 células individuais de B. fragilis após exposição a um vírus recém-isolado de águas residuais. Isso permitiu separar células infectadas das não infectadas na mesma cultura e ver como tanto a atividade do hospedeiro quanto a do vírus mudaram ao longo da infecção.
Reconstruindo uma linha do tempo invisível da infecção
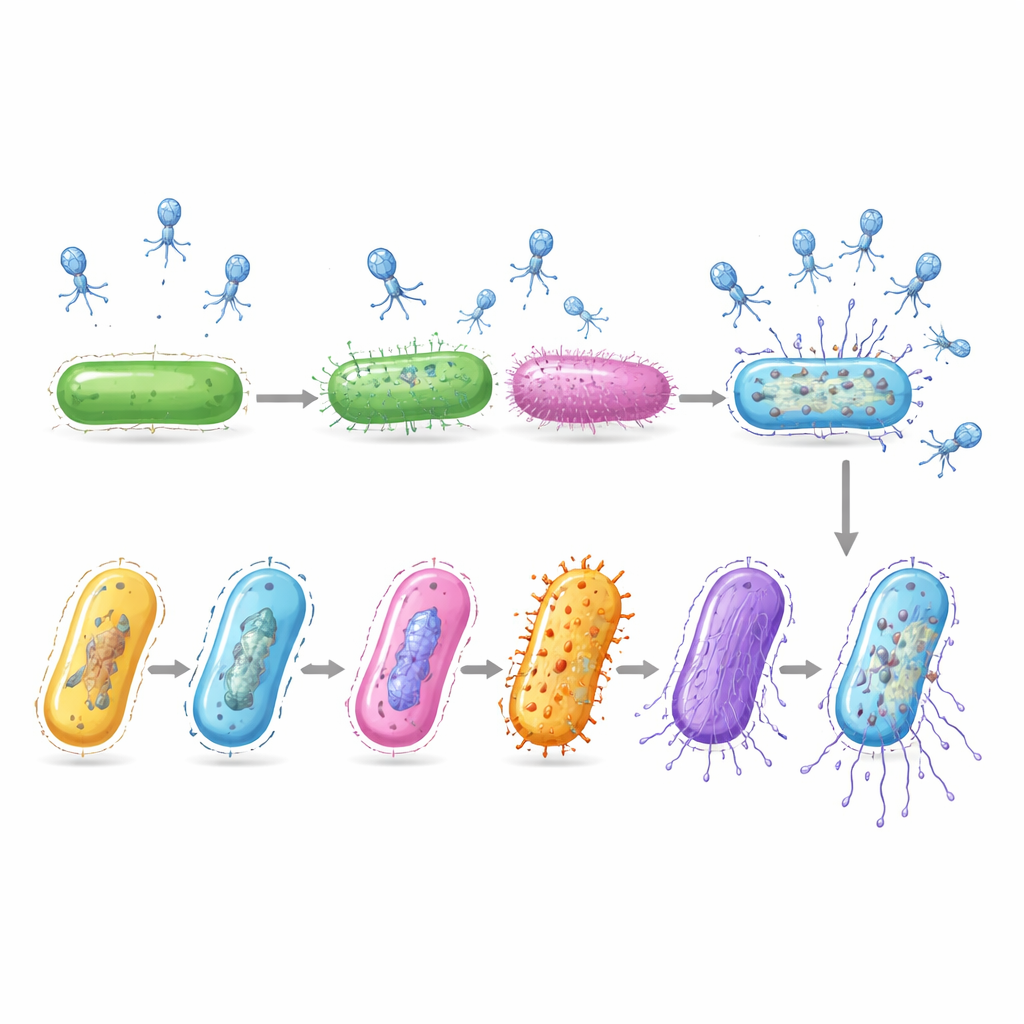
Embora os pesquisadores tenham capturado apenas um instante no tempo, as células infectadas foram encontradas em muitos estágios diferentes da doença. Ao comparar seus padrões de atividade gênica, a equipe ordenou essas células ao longo de uma linha do tempo virtual que acompanha o progresso da infecção. No início, o vírus fez a bactéria aumentar sua maquinaria básica de leitura de genes e síntese de proteínas. Na fase intermediária, o hospedeiro ligou genes que fornecem blocos de construção de DNA, que o vírus provavelmente sequestra para copiar seu genoma. No final do processo, as mensagens do próprio hospedeiro praticamente desapareceram enquanto genes virais para formar novas partículas virais e romper a célula dispararam, sinalizando um iminente estouro de descendentes virais.
Subtipos ocultos que ignoram o ataque
Nem todas as células na cultura exposta ao vírus estavam infectadas. Uma fração considerável permaneceu intocada, e os dados de célula única mostraram que isso não foi apenas sorte. A bactéria embaralha naturalmente certos interruptores de DNA, criando subgrupos que exibem diferentes coberturas de açúcar, chamadas cápsulas, e diferentes fibras de superfície, ou fímbria. A equipe descobriu que células com tipos específicos de cápsula, especialmente aquelas chamadas PSB e PSG, eram muito menos propensas a serem infectadas do que células com outros revestimentos. Outro sistema de superfície, controlado por um interruptor de DNA chamado Tsr16, tornou-se especialmente protetor quando altamente ativo, reduzindo ainda mais as chances de infecção.
Camadas de defesa que trabalham em conjunto
O estudo também examinou mecanismos antivirais conhecidos dentro da bactéria, como sistemas que cortam DNA estranho ou que sacrificam uma célula infectada. Sozinhos, essas defesas não explicaram totalmente quais células sobreviveram. Mas quando certas defesas internas estavam ativas nas mesmas células que possuíam cápsulas protetoras, a chance de infecção caiu para quase zero. Em experimentos de crescimento separados usando linhagens travadas para produzir apenas um tipo de cápsula, bactérias com o revestimento PSG resistiram ao vírus enquanto linhagens com cápsulas mais vulneráveis foram dizimadas. O sequenciamento de DNA das bactérias sobreviventes mostrou que a resistência veio principalmente da seleção desses tipos protetores pré-existentes, em vez de novas mutações.
O que isso significa para nosso intestino e para o uso de fagos
Para um leitor leigo, a mensagem principal é que as bactérias intestinais não são todas iguais em aparência ou comportamento, mesmo quando compartilham os mesmos genes. Ao misturar constantemente suas características de superfície e outras defesas, elas criam pequenos subgrupos que podem sobreviver a ataques virais súbitos e depois repovoar a comunidade. Essa estratégia de proteção embutida ajuda Bacteroides fragilis a persistir no ambiente turbulento do intestino humano e sugere que o uso médico bem-sucedido de fagos precisará levar em conta essas subpopulações ocultas e difíceis de eliminar.
Citação: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
Palavras-chave: bacteriófagos, microbioma intestinal, Bacteroides fragilis, sequenciamento de célula única, defesa bacteriana