Clear Sky Science · ru
Динамика взаимодействий фагов и хозяев у Bacteroides fragilis, восстановленная с помощью транскриптомики одиночных клеток
Почему крошечные битвы в кишечнике важны
В наших кишечниках живут бесчисленные бактерии и вирусы, охотящиеся на них. В этом исследовании внимание сосредоточено на такой дуэли между распространённой кишечной бактерией Bacteroides fragilis и вирусом, поражающим её. Наблюдая одновременно десятки тысяч отдельных бактериальных клеток, исследователи показывают, почему одни бактерии гибнут, а другие остаются невредимыми и позволяют популяции восстановиться. Эти скрытые приёмы выживания формируют ответ нашего кишечного сообщества на вирусные атаки и могут помочь в разработке будущих фаговых терапий.
Смотреть на отдельные клетки, а не на мутную смесь
Большая часть прежних работ по бактериям и их вирусам проводилась в объёмных пробирках, где поведение миллионов клеток усредняется. Такой подход скрывает, что не каждая клетка ведёт себя одинаково. Здесь команда использовала метод микробного одноклеточного секвенирования РНК, чтобы прочитать, какие гены активны примерно в 50 000 отдельных клетках B. fragilis после контакта с недавно выделенным вирусом из сточных вод. Это позволило им отделить заражённые от незаражённых клеток в одной и той же культуре и проследить, как активность хозяина и вируса менялась в ходе инфекции.
Воссоздание невидимой временной линии инфекции
Хотя исследователи сделали лишь один снимок во времени, заражённые клетки оказались пойманными на разных стадиях болезни. Сравнивая их профили активности генов, команда расположила эти клетки вдоль виртуальной временной шкалы, отслеживающей прогресс инфекции. На ранней стадии вирус заставлял бактерию усиливать основные механизмы чтения генов и синтеза белка. В средней фазе хозяин включал гены, обеспечивающие дезоксирибонуклеотидные строительные блоки ДНК, которые вирус, вероятно, присваивает для копирования своего генома. На поздней стадии собственные сообщения хозяина в основном исчезали, тогда как вирусные гены, отвечающие за сборку новых вирионов и разрыв клетки, резко возрастали, предвещая скорый выпуск потомства вируса.
Скрытые подтипы, которые отмахиваются от атаки
Не все клетки в культуре, подвергшейся воздействию вируса, были заражены. Значительная часть осталась нетронутой, и одноклеточные данные показали, что это было не просто везение. Бактерия естественно перемешивает определённые ДНК-переключатели, создавая подгруппы, которые демонстрируют разные сахарные покрытия, называемые капсулами, и разные поверхностные волокна — фимбрии. Команда обнаружила, что клетки с определёнными типами капсул, особенно помеченными как PSB и PSG, гораздо реже подвергались заражению, чем клетки с другими покровами. Ещё одна поверхностная система, контролируемая ДНК-переключателем Tsr16, становилась особенно защитной при высокой активности, дополнительно снижая вероятность инфицирования.
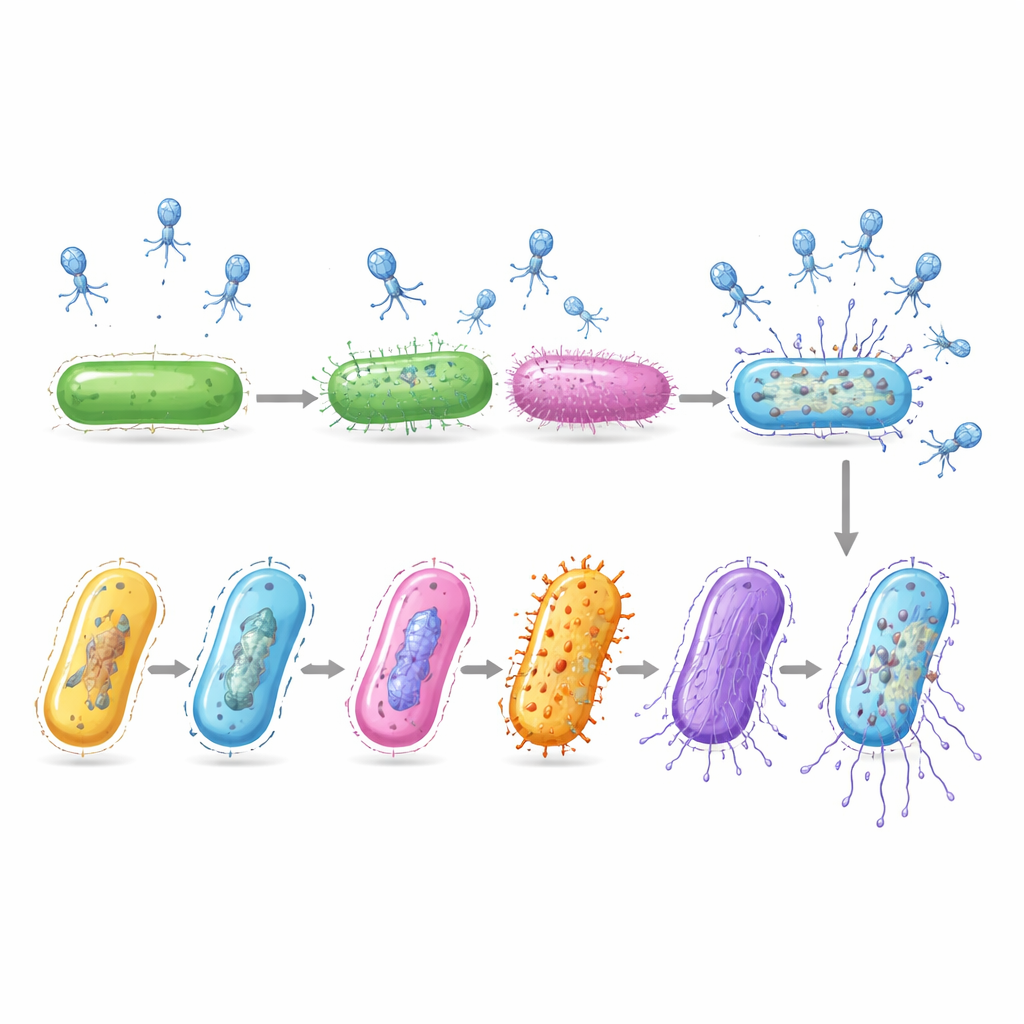
Слои защиты, работающие вместе
Исследование также рассмотрело известные антивирусные механизмы внутри бактерии, такие как системы, разрезающие чужую ДНК, или программы самопожертвования инфицированной клетки. Сами по себе эти защиты не полностью объясняли, какие клетки выживают. Но когда определённые внутренние защиты были активны в тех же клетках, которые несли защитные капсулы, шанс заражения падал почти до нуля. В отдельных опытах роста со штаммами, «запертыми» на производстве только одного типа капсулы, бактерии с покрытием PSG противостояли вирусу, в то время как штаммы с более уязвимыми покровами были уничтожены. Последующее секвенирование ДНК выживших бактерий показало, что устойчивость в основном возникала за счёт отбора этих заранее существующих защитных типов, а не за счёт новых мутаций.
Что это значит для нашего кишечника и применения фагов
Для неспециалиста основной вывод таков: кишечные бактерии не все одинаково выглядят и не ведут себя одинаково, даже если у них одни и те же гены. Постоянно меняя свои поверхностные черты и другие защиты, они создают небольшие подгруппы, которые могут пережить внезапные вирусные атаки и затем вновь населить сообщество. Эта встроенная стратегия распределения рисков помогает Bacteroides fragilis сохраняться в бурной среде человеческого кишечника и означает, что успешное медицинское применение фагов должно учитывать эти скрытые, трудноубиваемые подпопуляции.
Цитирование: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
Ключевые слова: бактериофаги, микробиом кишечника, Bacteroides fragilis, секвенирование одиночных клеток, бактериальная защита