Clear Sky Science · es
Dinámica de las interacciones fago-hospedador en Bacteroides fragilis resuelta mediante transcriptómica de célula única
Por qué importan las pequeñas batallas en el intestino
Nuestros intestinos albergan innumerables bacterias y los virus que las persiguen. Este estudio se centra en uno de esos duelos entre una bacteria intestinal común, Bacteroides fragilis, y un virus que la infecta. Al observar decenas de miles de células bacterianas individuales a la vez, los investigadores revelan por qué algunas bacterias sucumben mientras otras permanecen a salvo y permiten que la población se recupere. Estas estrategias de supervivencia ocultas condicionan la respuesta de nuestro ecosistema intestinal a los ataques virales y pueden orientar futuras terapias con fagos.
Mirar células individuales en lugar de caldo turbio
La mayor parte del trabajo previo sobre bacterias y sus virus se ha realizado en tubos de ensayo en masa, donde el comportamiento de millones de células se promedia. Ese enfoque oculta que no todas las células se comportan igual. Aquí, el equipo utilizó un método llamado secuenciación de ARN de célula única microbiana para leer qué genes estaban activos en unas 50 000 células individuales de B. fragilis tras la exposición a un virus recién aislado de aguas residuales. Esto les permitió separar células infectadas de no infectadas en la misma cultura y ver cómo cambiaba la actividad tanto del hospedador como del virus a lo largo de la infección.
Reconstruir una línea temporal de la infección invisible
Aunque los investigadores tomaron solo una instantánea temporal, las células infectadas se captaron en muchas etapas distintas de la enfermedad. Al comparar sus patrones de actividad génica, el equipo ordenó esas células a lo largo de una línea temporal virtual que sigue el progreso de la infección. En las fases iniciales, el virus impulsó a la bacteria a aumentar su maquinaria básica de lectura génica y síntesis de proteínas. En la fase intermedia, el hospedador activó genes que suministran bloques de construcción de ADN, que el virus probablemente secuestra para copiar su genoma. Ya en la fase tardía, los mensajes propios del hospedador prácticamente desaparecieron mientras que los genes virales para ensamblar nuevas partículas y lisar la célula se dispararon, señalando una inminente liberación de descendencia viral.
Subtipos ocultos que sortearon el ataque
No todas las células de la cultura expuesta al virus estaban infectadas. Una fracción considerable quedó intacta, y los datos de célula única mostraron que esto no fue solo casualidad. La bacteria baraja de forma natural ciertos interruptores de ADN, creando subgrupos que exhiben diferentes recubrimientos de azúcares, llamados cápsulas, y distintas fibras superficiales, o fimbrias. El equipo encontró que las células con tipos específicos de cápsula, en especial las denominadas PSB y PSG, tenían muchas menos probabilidades de ser infectadas que las células con otros recubrimientos. Otro sistema superficial, controlado por un interruptor de ADN llamado Tsr16, se volvió especialmente protector cuando estaba altamente activo, reduciendo aún más las probabilidades de infección.
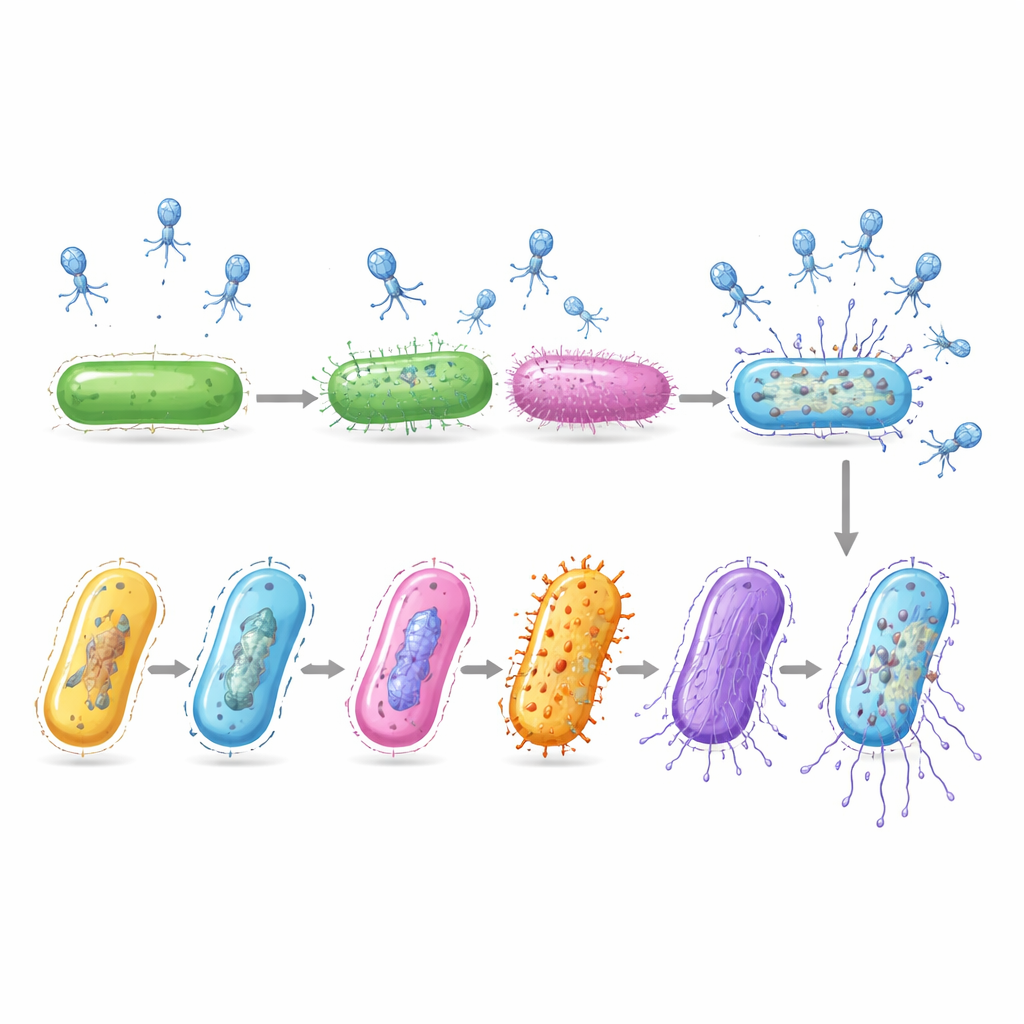
Capas de defensa que actúan en conjunto
El estudio también examinó herramientas antivirales conocidas dentro de la bacteria, como sistemas que cortan ADN extraño o que sacrifican una célula infectada. Por sí solas, estas defensas no explicaron completamente qué células sobrevivían. Pero cuando ciertas defensas internas estaban activas en las mismas células que portaban cápsulas protectoras, la probabilidad de infección cayó casi a cero. En experimentos de crecimiento separados usando cepas bloqueadas para producir solo un tipo de cápsula, las bacterias con el recubrimiento PSG resistieron el virus, mientras que las cepas con recubrimientos más vulnerables fueron eliminadas. El posterior secuenciado del ADN de las bacterias supervivientes mostró que la resistencia procedía principalmente de la selección de estos tipos protectores preexistentes, más que de nuevas mutaciones.
Qué significa esto para nuestro intestino y el uso de fagos
Para el lector general, el mensaje principal es que las bacterias intestinales no todas se ven ni se comportan igual, incluso cuando comparten los mismos genes. Al mezclar constantemente sus rasgos superficiales y otras defensas, crean pequeños subgrupos que pueden sobrevivir a ataques virales repentinos y más tarde repoblar la comunidad. Esta estrategia interna de diversificación ayuda a Bacteroides fragilis a persistir en el ambiente turbulento del intestino humano y sugiere que el uso médico exitoso de fagos tendrá que tener en cuenta estas subpoblaciones ocultas y difíciles de eliminar.
Cita: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
Palabras clave: bacteriófagos, microbioma intestinal, Bacteroides fragilis, secuenciación de célula única, defensa bacteriana