Clear Sky Science · de
Dynamik von Phagen-Wirt-Interaktionen in Bacteroides fragilis aufgelöst durch Einzelzell-Transkriptomik
Warum winzige Kämpfe im Darm wichtig sind
Unser Darm beherbergt unzählige Bakterien und die Viren, die sie jagen. Diese Studie zoomt auf einen solchen Zweikampf zwischen einem verbreiteten Darmbakterium, Bacteroides fragilis, und einem es infizierenden Virus. Indem die Forschenden Zehntausende einzelner Bakterienzellen gleichzeitig beobachteten, zeigen sie, warum einige Zellen dem Opfer fallen, während andere verschont bleiben und die Population sich wieder erholt. Diese verborgenen Überlebensstrategien prägen, wie unser Darmökosystem auf virale Angriffe reagiert und können Hinweise für künftige Phagentherapien liefern.
Einzelzellen statt trüber Brühe betrachten
Die meisten früheren Arbeiten zu Bakterien und ihren Viren wurden in Bulk-Ansätzen in Reagenzgläsern durchgeführt, wo das Verhalten von Millionen Zellen gemittelt wird. Dieser Ansatz verschleiert, dass nicht jede Zelle gleich reagiert. Hier nutzte das Team eine Methode namens mikrobielles Einzelzell-RNA-Sequencing, um zu erfassen, welche Gene in etwa 50.000 einzelnen B. fragilis-Zellen nach Kontakt mit einem neu aus Abwasser isolierten Virus aktiv waren. Dadurch konnten sie infizierte von nicht infizierten Zellen in derselben Kultur trennen und verfolgen, wie sich Aktivität von Wirt und Virus im Verlauf der Infektion veränderte.
Eine unsichtbare Infektions-Zeitleiste rekonstruieren
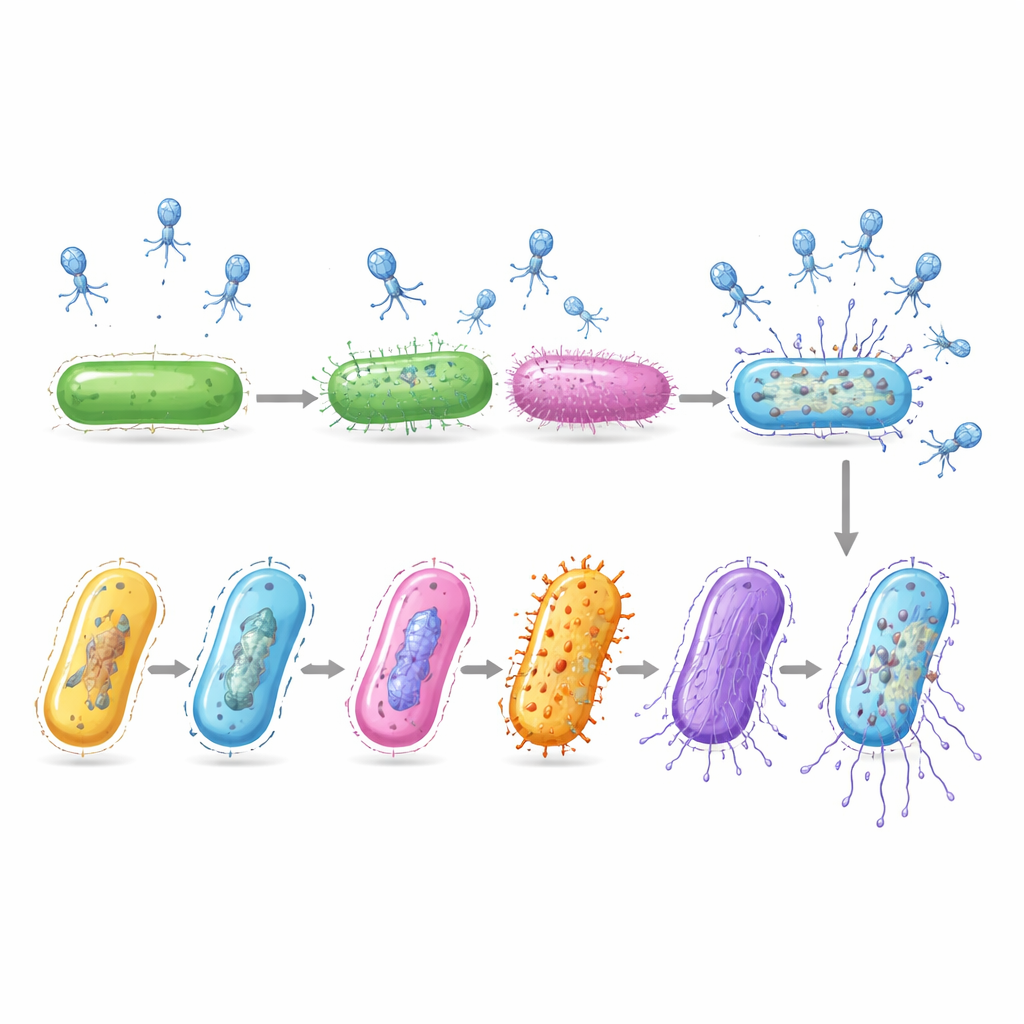
Obwohl die Forschenden nur einen zeitlichen Schnappschuss aufnahmen, wurden infizierte Zellen in vielen verschiedenen Krankheitsstadien erfasst. Durch den Vergleich ihrer Genaktivitätsmuster ordnete das Team diese Zellen entlang einer virtuellen Zeitleiste, die den Verlauf der Infektion abbildet. Zu Beginn veranlasste das Virus das Bakterium, seine grundlegenden Transkriptions- und Proteinsynthesemaschinen hochzufahren. In der mittleren Phase schaltete der Wirt Gene ein, die DNA-Bausteine liefern — die das Virus vermutlich zur Kopie seines Genoms kapert. Später gingen die Wirts-mRNAs größtenteils verloren, während virale Gene für den Aufbau neuer Partikel und das Aufbrechen der Zelle stark zunahmen, was auf eine bevorstehende Freisetzung von Virusnachkommen hindeutet.
Verborgene Subtypen, die Angriffe abschütteln
Nicht alle Zellen in der virus-exponierten Kultur waren infiziert. Ein beträchtlicher Anteil blieb unberührt, und die Einzelzell-Daten zeigten, dass dies keine bloße Zufälligkeit war. Das Bakterium variiert auf natürliche Weise bestimmte DNA-Schalter und erzeugt so Subgruppen, die unterschiedliche Zuckerschichten, sogenannte Kapseln, und verschiedene Oberflächenfasern, Fimbrien, zeigen. Das Team fand, dass Zellen mit spezifischen Kapseltypen, insbesondere solche namens PSB und PSG, deutlich seltener infiziert wurden als Zellen mit anderen Hüllen. Ein weiteres Oberflächensystem, kontrolliert von einem DNA-Schalter namens Tsr16, erwies sich bei hoher Aktivität als besonders schützend und verringerte zusätzlich die Infektionswahrscheinlichkeit.
Mehrere Verteidigungsebenen arbeiten zusammen
Die Studie untersuchte auch bekannte antivirale Werkzeuge im Bakterium, etwa Systeme, die fremde DNA zerschneiden, oder Mechanismen, die eine infizierte Zelle opfern. Allein erklärten diese Abwehrmechanismen nicht vollständig, welche Zellen überlebten. Wenn jedoch bestimmte interne Abwehrsysteme in denselben Zellen aktiv waren, die schützende Kapseln trugen, sank die Infektionswahrscheinlichkeit nahezu auf null. In separaten Wachstumsexperimenten mit Stämmen, die fest auf die Produktion eines einzigen Kapseltyps eingestellt waren, widerstand die PSG-hüllende Variante dem Virus, während Stämme mit empfindlicheren Hüllen ausgelöscht wurden. Nachfolgende DNA-Sequenzierung der überlebenden Bakterien zeigte, dass die Resistenz vorwiegend aus der Selektion dieser bereits vorhandenen schützenden Typen stammte und weniger aus neuen Mutationen.
Was das für unseren Darm und den Einsatz von Phagen bedeutet
Für interessierte Laien lautet die Kernbotschaft: Darmbakterien sehen nicht alle gleich aus und verhalten sich nicht einheitlich, selbst wenn sie dieselben Gene besitzen. Indem sie ständig ihre Oberflächeneigenschaften und andere Abwehrmechanismen durchmischen, schaffen sie kleine Subgruppen, die plötzliche Virusangriffe überstehen und später die Gemeinschaft wieder besiedeln können. Dieses eingebaute Risikostreuen hilft Bacteroides fragilis, im turbulenten Milieu des menschlichen Darms zu persistieren, und legt nahe, dass ein erfolgreicher medizinischer Einsatz von Phagen diese verborgenen, schwer zu eliminierenden Subpopulationen berücksichtigen muss.
Zitation: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
Schlüsselwörter: Bakteriophagen, Darmmikrobiom, Bacteroides fragilis, Einzelzell-Sequenzierung, bakterielle Abwehr