Clear Sky Science · pl
Dynamika interakcji fag‑gospodarz u Bacteroides fragilis badana za pomocą transkryptomiki pojedynczych komórek
Dlaczego te drobne bitwy w jelitach mają znaczenie
Nasze jelita są miejscem bytowania niezliczonych bakterii oraz wirusów, które je atakują. W tej pracy przyjrzano się bliżej jednej z takich potyczek między powszechną bakterią jelitową, Bacteroides fragilis, a wirusem ją infekującym. Obserwując dziesiątki tysięcy pojedynczych komórek bakteryjnych jednocześnie, badacze pokazują, dlaczego niektóre bakterie padają ofiarą, podczas gdy inne pozostają bezpieczne i umożliwiają odbudowę populacji. Ukryte strategie przetrwania kształtują reakcję naszego ekosystemu jelitowego na ataki wirusowe i mogą pomóc w opracowaniu przyszłych terapii fagowych.
Patrzenie na pojedyncze komórki zamiast na mętny bulion
Większość wcześniejszych badań nad bakteriami i ich wirusami prowadzono w zbiorczych probówkach, gdzie zachowanie milionów komórek uśrednia się. Takie podejście ukrywa fakt, że nie każda komórka zachowuje się tak samo. W tym badaniu zespół użył metody zwanej mikrobiologicznym sekwencjonowaniem RNA pojedynczych komórek, aby odczytać, które geny były aktywne w około 50 000 pojedynczych komórek B. fragilis po ekspozycji na niedawno wyizolowanego wirusa z ścieków. Pozwoliło to oddzielić komórki zakażone od niezakażonych w tej samej hodowli i zobaczyć, jak aktywność zarówno gospodarza, jak i wirusa zmieniała się w przebiegu infekcji.
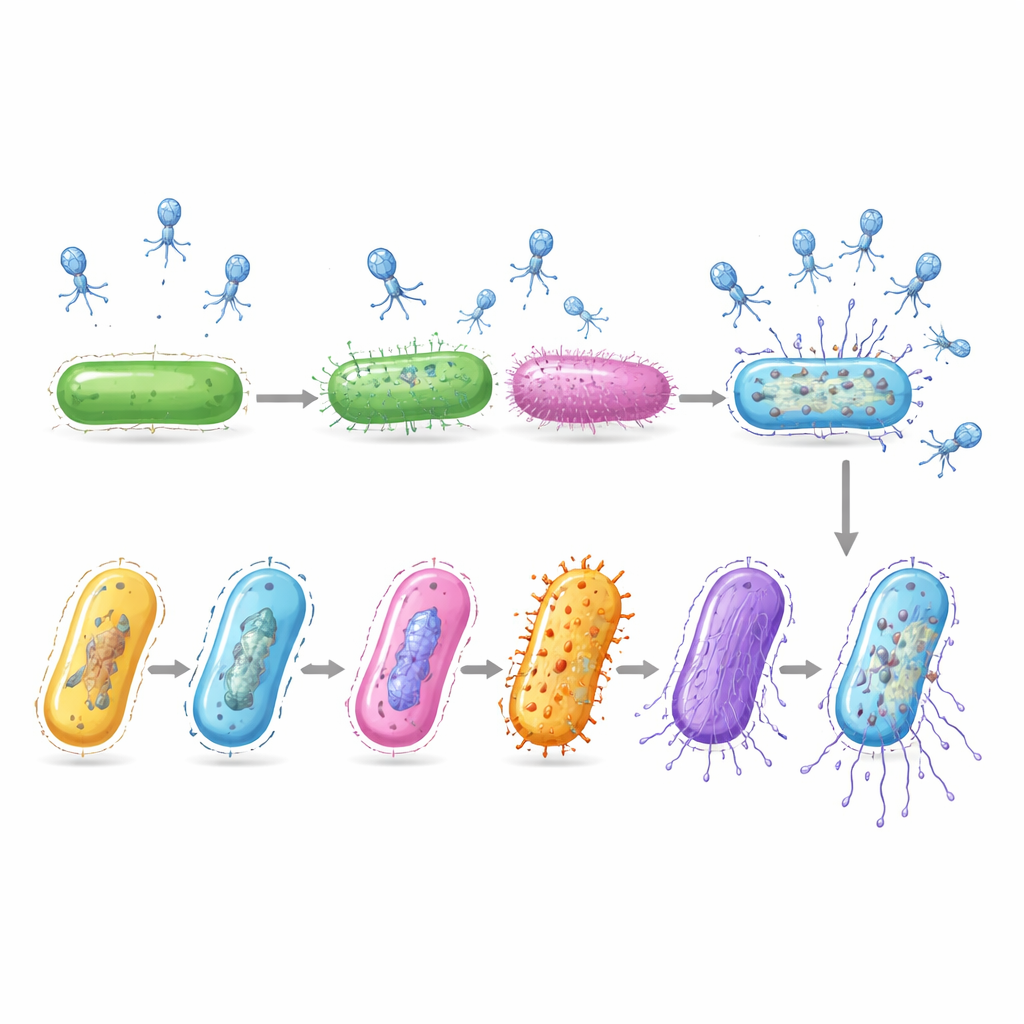
Odtwarzanie niewidzialnej osi czasu infekcji
Chociaż badacze wykonali tylko jedno zdjęcie w czasie, komórki zakażone zostały uchwycone na różnych etapach choroby. Porównując ich wzorce aktywności genów, zespół uporządkował te komórki wzdłuż wirtualnej osi czasu, śledząc postęp infekcji. Na wczesnym etapie wirus nakłaniał bakterię do zwiększenia podstawowych procesów odczytu genów i syntezy białek. W fazie środkowej gospodarz włączał geny dostarczające składników do budowy DNA, które wirus prawdopodobnie przejmuje, by kopiować swój genom. Pod koniec procesu wiadomości komórkowe gospodarza niemal zniknęły, podczas gdy geny wirusa odpowiadające za składanie nowych cząstek wirusowych i lizę komórki gwałtownie wzrosły, sygnalizując zbliżające się uwolnienie potomstwa wirusa.
Ukryte podtypy, które zbywają atak
Nie wszystkie komórki w hodowli wystawionej na wirusa zostały zakażone. Znaczna część pozostała nietknięta, a dane z pojedynczych komórek pokazały, że nie była to tylko kwestia szczęścia. Bakteria naturalnie przestawia pewne przełączniki DNA, tworząc podgrupy wykazujące różne osłony cukrowe, zwane kapsułami, oraz różne włókna powierzchniowe, czyli fimbrie. Zespół wykrył, że komórki mające określone typy kapsuł, szczególnie określone jako PSB i PSG, były znacznie mniej podatne na zakażenie niż komórki z innymi osłonami. Inny system powierzchniowy, kontrolowany przez przełącznik DNA o nazwie Tsr16, stał się szczególnie ochronny przy wysokiej aktywności, dodatkowo obniżając prawdopodobieństwo infekcji.
Wielowarstwowa obrona działająca wspólnie
Badanie przyjrzało się także znanym narzędziom przeciwwirusowym wewnątrz bakterii, takim jak systemy tnące obce DNA czy mechanizmy poświęcenia zakażonej komórki. Same w sobie te obrony nie wyjaśniały w pełni, które komórki przetrwały. Jednak gdy niektóre wewnętrzne mechanizmy ochronne były aktywne w tych samych komórkach, które nosiły ochronne kapsuły, szansa zakażenia spadała niemal do zera. W odrębnych eksperymentach wzrostu, używając szczepów zablokowanych w produkcji tylko jednego typu kapsuły, bakterie z osłoną PSG były odporne na wirusa, podczas gdy szczepy z bardziej podatnymi osłonami zostały zniszczone. Dalsze sekwencjonowanie DNA przetrwałych bakterii wykazało, że odporność wynikała głównie z selekcji tych uprzednio istniejących ochronnych typów, a nie z nowych mutacji.
Co to oznacza dla naszych jelit i zastosowań fagów
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że bakterie jelitowe nie wyglądają i nie zachowują się identycznie, nawet jeśli mają te same geny. Poprzez stałe mieszanie cech powierzchniowych i innych mechanizmów obronnych tworzą małe podgrupy, które potrafią przetrwać nagłe ataki wirusowe i później odbudować społeczność. To wbudowane zabezpieczenie przez dywersyfikację pomaga Bacteroides fragilis utrzymać się w burzliwym środowisku ludzkiego jelita i sugeruje, że skuteczne medyczne wykorzystanie fagów będzie musiało uwzględniać te ukryte, trudne do wyeliminowania podpopulacje.
Cytowanie: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
Słowa kluczowe: bakteriofagi, mikrobiom jelitowy, Bacteroides fragilis, sekwencjonowanie pojedynczych komórek, obrona bakteryjna