Clear Sky Science · nl
Dynamiek van faag-gastheerinteracties in Bacteroides fragilis ontrafeld met single-cell transcriptomica
Waarom kleine gevechten in de darm ertoe doen
Onze darmen herbergen talloze bacteriën en de virussen die hen belagen. Deze studie zoomt in op één zulk duel tussen een veelvoorkomende darmbacterie, Bacteroides fragilis, en een virus dat haar infecteert. Door tienduizenden individuele bacteriële cellen tegelijk te volgen laten de onderzoekers zien waarom sommige bacteriën ten prooi vallen terwijl andere ongedeerd blijven en de populatie zich herstelt. Deze verborgen overlevingstrucs bepalen hoe ons darm-ecosysteem op virale aanvallen reageert en kunnen richting geven aan toekomstige faagtherapieën.
Kijken naar individuele cellen in plaats van troebele vloeistof
Het merendeel van eerder werk aan bacteriën en hun virussen gebeurde in bulkbuisjes, waar het gedrag van miljoenen cellen wordt gemiddeld. Die aanpak verbergt dat niet elke cel hetzelfde doet. Hier gebruikte het team een methode genaamd microbiele single-cell RNA-sequencing om te lezen welke genen actief waren in ongeveer 50.000 individuele B. fragilis-cellen na blootstelling aan een nieuw geïsoleerde faag uit afvalwater. Daardoor konden ze geïnfecteerde en ongeïnfecteerde cellen binnen dezelfde cultuur scheiden en zien hoe zowel gastheer- als faagactiviteit veranderde tijdens het infectieverloop.
Het reconstrueren van een onzichtbare infectietijdlijn
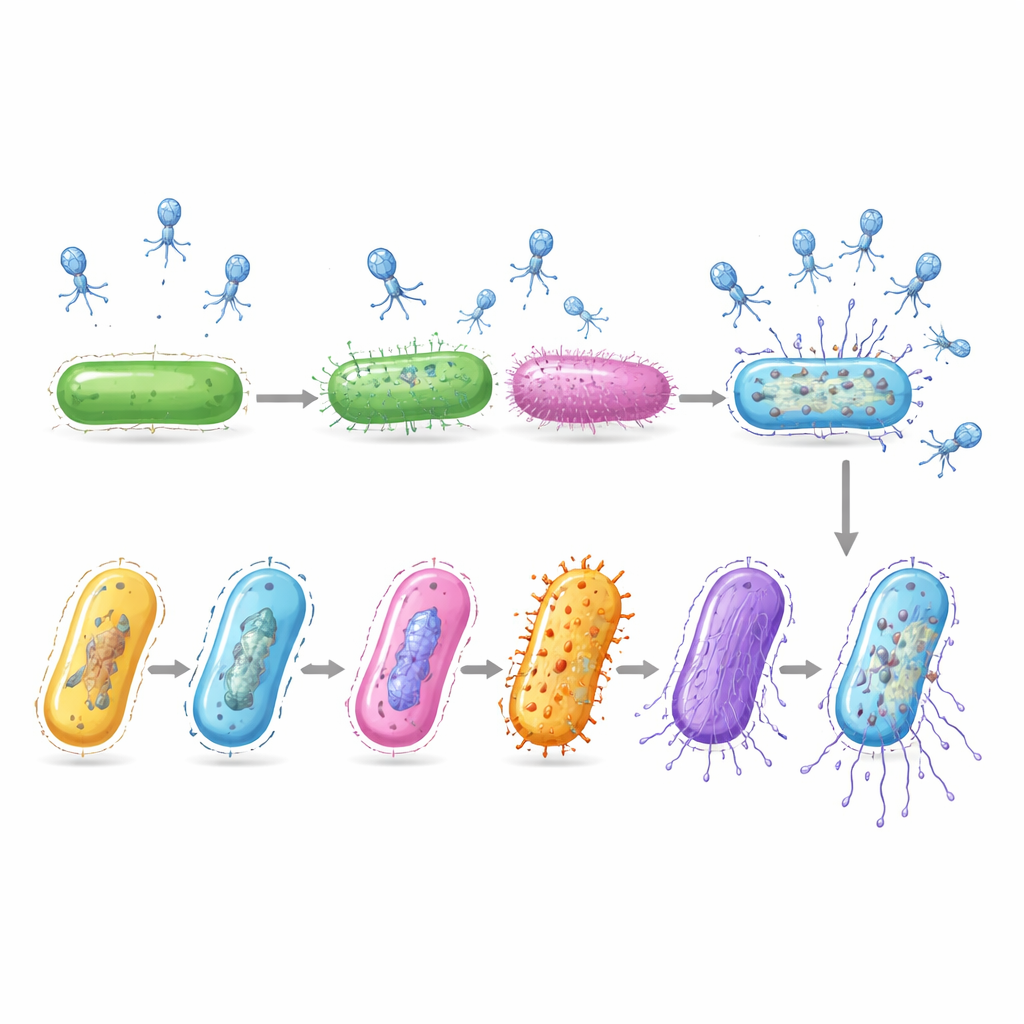
Hoewel de onderzoekers slechts één momentopname namen, werden geïnfecteerde cellen in veel verschillende stadia van de ziekte aangetroffen. Door hun genexpressiepatronen te vergelijken, ordende het team deze cellen langs een virtuele tijdlijn die het verloop van de infectie volgt. Vroeg in het proces zette het virus de bacterie ertoe aan zijn basale transcriptie- en eiwitsynthesemachinerie op te voeren. In de middenfase schakelde de gastheer genen aan die bouwstenen voor DNA leveren, die het virus vermoedelijk kaapt om zijn genoom te kopiëren. Laat in het proces verdwenen de eigen boodschappers van de gastheer grotendeels, terwijl virale genen voor het bouwen van nieuwe deeltjes en het lyseren van de cel sterk toenamen, wat wijst op een op handen zijnde uitbarsting van nakomelingen van het virus.
Verborgen subtypes die een aanval afslaan
Niet alle cellen in de faag-blootgestelde cultuur waren geïnfecteerd. Een aanzienlijk deel bleef ongedeerd, en single-cellgegevens toonden dat dit niet slechts geluk was. De bacterie schakelt van nature bepaalde DNA-schakelaars om, waardoor subgroepen ontstaan die verschillende suikerkappen, zogenaamde kapsels, en verschillende oppervlakvezels, of fimbriae, tonen. Het team ontdekte dat cellen met specifieke kapseltypes, vooral die genoemd PSB en PSG, veel minder kans hadden om geïnfecteerd te worden dan cellen met andere kappen. Een ander oppervlaktesysteem, gestuurd door een DNA-schakelaar genaamd Tsr16, werd bijzonder beschermend wanneer het sterk actief was en verlaagde zo de infectiekans verder.
Verdedigingslagen die samenwerken
De studie onderzocht ook bekende antivirale instrumenten binnen de bacterie, zoals systemen die vreemd DNA knippen of een geïnfecteerde cel opofferen. Op zichzelf verklaarden deze verdedigingsmechanismen niet volledig welke cellen overleefden. Maar wanneer bepaalde interne verdedigingen actief waren in dezelfde cellen die beschermende kapsels droegen, daalde de kans op infectie tot bijna nul. In aparte groeiexperimenten met stammen die vastgezet waren op het produceren van slechts één kapseltype, weerstond de PSG-coat de faag terwijl stammen met kwetsbaardere kappen werden weggevaagd. Verdere DNA-sequencing van overlevende bacteriën toonde aan dat resistentie vooral voortkwam uit selectie van deze reeds bestaande beschermende types, eerder dan uit nieuwe mutaties.
Wat dit betekent voor onze darm en voor het gebruik van faagtherapieën
Voor de niet-specialist is de belangrijkste boodschap dat darmbacteriën niet allemaal hetzelfde uitzien of zich hetzelfde gedragen, zelfs als ze dezelfde genen delen. Door voortdurend hun oppervlaktestructuren en andere verdedigingsmiddelen te variëren, creëren ze kleine subgroepen die plotselinge virale aanvallen kunnen overleven en later de gemeenschap opnieuw bevolken. Deze ingebouwde risicospreiding helpt Bacteroides fragilis te volharden in de turbulente omgeving van de menselijke darm en suggereert dat succesvolle medische toepassing van faagtherapieën rekening zal moeten houden met deze verborgen, moeilijk uitroeibare subpopulaties.
Bronvermelding: Gupta, A., Morella, N., Sutormin, D. et al. Dynamics of phage-host interactions in Bacteroides fragilis resolved by single-cell transcriptomics. Nat Commun 17, 4035 (2026). https://doi.org/10.1038/s41467-026-70381-8
Trefwoorden: bacteriophagen, darmmicrobioom, Bacteroides fragilis, single-cell sequencing, bacteriële verdediging