Clear Sky Science · zh
基于全基因组的心室表型分析揭示心力衰竭的新位点和治疗靶点
为什么心脏的“隐性代码”很重要
心力衰竭是导致死亡和致残的主要原因之一,但在出现症状时,心脏的许多损伤往往已不可逆。如今医生可以对心脏的主要泵血腔室——左、右心室——进行精细扫描,以评估其功能。但直到最近,我们对决定这些结构的遗传密码知之甚少,也不了解它如何指示潜在的新疗法。本研究深入分析了超过五万六千人的DNA,揭示了数千个微小遗传差异如何影响心脏大小与收缩力,进而影响心力衰竭风险。
深入数千颗心脏的内部
研究人员使用心脏磁共振成像(CMR),这是一种高精度的成像方法,测量了二十项关于心室结构与泵血功能的指标。其中包括经典指标,例如左右心室每搏容积与射血量,以及更综合的新指标,这些指标把心脏大小与肌肉质量结合起来评估泵功能。所有扫描均来自英国生物样本库(UK Biobank)的参与者,研究还使用了先进的计算算法对心腔进行自动且一致的描记,覆盖了超过56,000名个体。
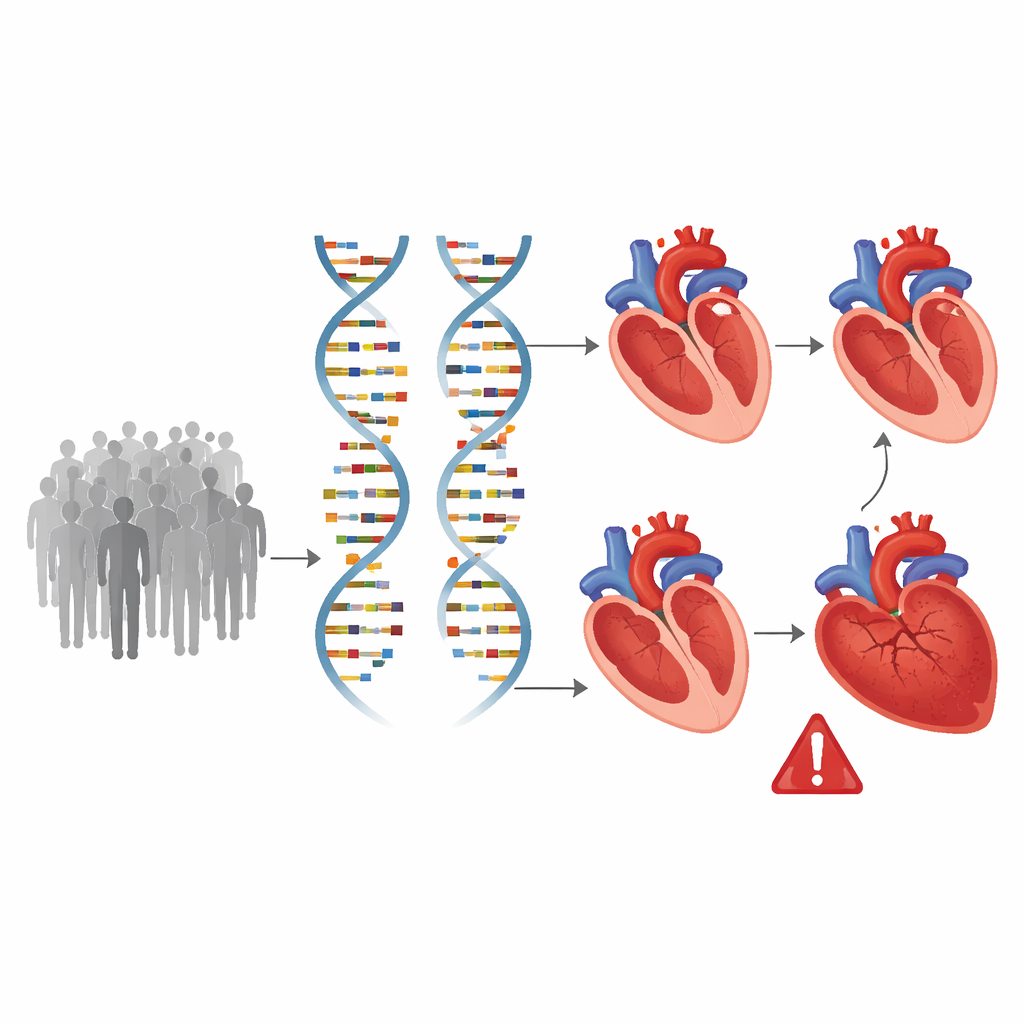
在全基因组中寻找塑造心脏的基因
掌握这些精细的心脏测量后,研究团队扫查了整个基因组,检测了约890万个常见遗传变异,寻找与心室结构与功能差异相关联的位点。他们发现了200个与至少一项心脏表型相关的基因组区域,其中58个此前未与心脏影像学指标相连。许多位点影响多项测量,提示存在影响心室大小与泵血能力的共同生物通路。计算显示,遗传因素可解释这些性状大约五分之一到三分之一的变异,证实我们的DNA在心室发育与随时间重塑中起着重要作用。
从DNA信号到疾病风险
接着,科学家考察了这些塑心变异与真实世界疾病之间的联系。他们将结果与以往关于心力衰竭及其他心血管疾病的遗传研究进行比对,发现有23个基因组区域似乎同时影响心室表型与心力衰竭本身。其中一些区域含有已知的遗传性心肌病相关基因,另一些(例如参与机械应激或低氧反应的基因)则指出了导致损伤的额外生物路径。通过构建多基因风险评分——将许多微小DNA效应综合计算——研究表明,遗传上倾向于心室扩大或增厚的人群,其心力衰竭、高血压和心律失常发生率也更高。相反,遗传特征偏向更高效泵血的个体(由左心室全局功能指数和心肌收缩分数等新指标表征)则与这些疾病风险较低相关。
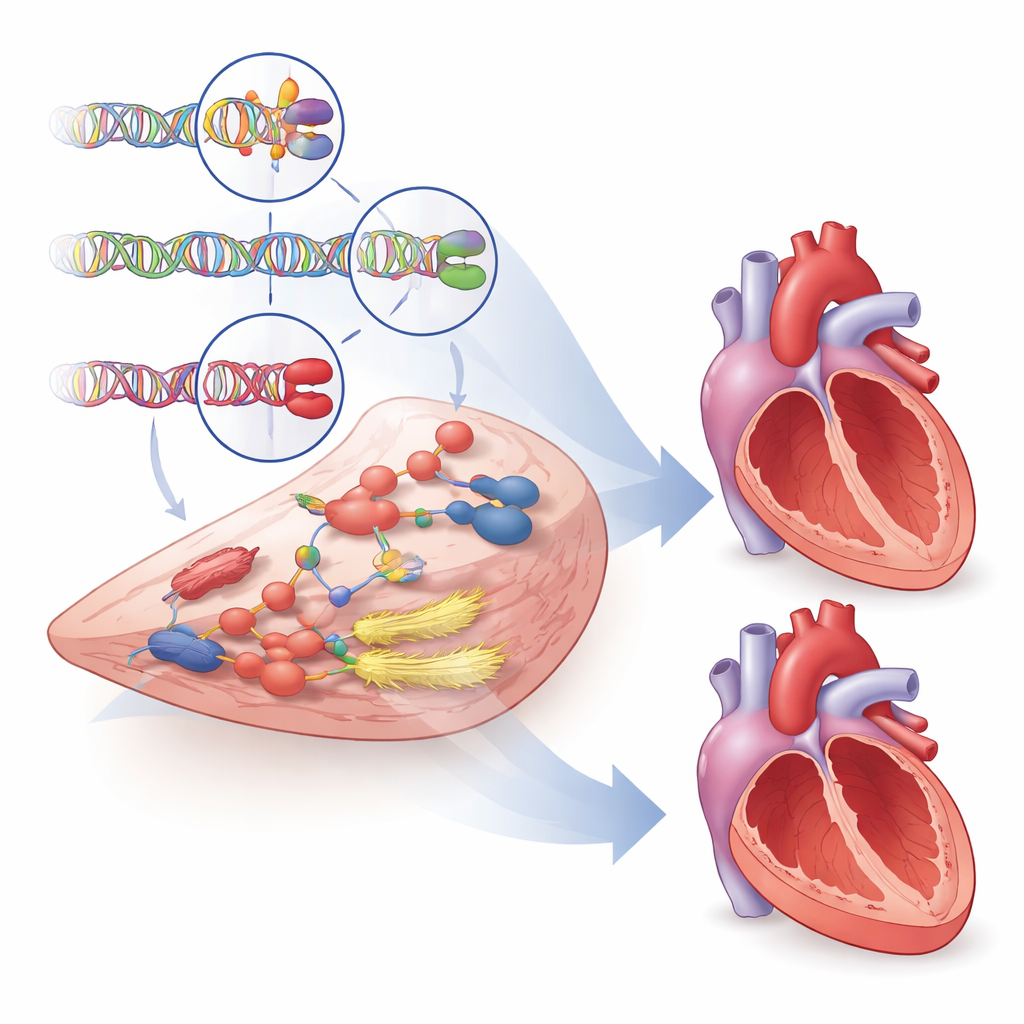
对新疗法的启示
除了阐明为什么有些心脏更易脆弱外,研究还寻找可能成为药物靶点的基因。研究者利用多个数据库、动物研究与基因表达模式,对超过一千个邻近基因进行了系统评分,并突出显示了近500个具有参与心室结构与功能证据的基因。其中数十个基因与现有心血管药物有相互作用,包括影响心肌收缩与血管张力的药物,这提示了药物再利用或优化治疗的可能性。一个显著例子是PDE3A基因,其变异与有害重塑迹象相关。现有药物通常同时抑制PDE3A和其近亲PDE3B,但遗传数据表明,设计更具选择性地靶向PDE3A的治疗可能在避免目前非选择性药物副作用的同时改善疗效。
这对患者意味着什么
通俗地说,这项研究将我们DNA中的微小差异与心脏主要泵血腔室的构造与功能联系起来,进而把这些模式与谁更可能发生心力衰竭相连。通过结合前沿影像学、大规模遗传学与药物靶点分析,该研究不仅加深了我们对心脏破裂原因的理解,还指向了未来药物可以把握的具体分子靶标。尽管仍需更多工作——尤其是在不同族群与实验模型中的验证——这些发现让我们更接近于一种前景:通过影像与基因检测的组合,早期预测心力衰竭并指导更精确、基于遗传信息的治疗。}
引用: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
关键词: 心力衰竭, 心脏磁共振成像, 遗传学, 心室重塑, 药物靶点