Clear Sky Science · ru
Геномный анализ фенотипов желудочков сердца выявляет новые локусы и терапевтические мишени при сердечной недостаточности
Почему важен скрытый код сердца
Сердечная недостаточность — одна из ведущих причин смерти и инвалидности, однако к моменту появления симптомов большая часть повреждений сердца уже имеет место. Врачи теперь могут получать детальные снимки главных камер насоса сердца — левого и правого желудочков — чтобы оценить их работу. Но до недавнего времени мы знали гораздо меньше о генетическом коде, формирующем эти структуры, и о том, как он может указывать на новые подходы к лечению. В этом исследовании проанализировали ДНК более чем пятидесяти шести тысяч человек, чтобы выяснить, как тысячи мелких генетических вариантов влияют на размеры сердца, его силу и, в конечном счёте, риск сердечной недостаточности.
Внутри тысяч сердец
Исследователи использовали кардиальную магнитно‑резонансную томографию — высокоточный метод сканирования — чтобы измерить двадцать показателей строения и насосной функции желудочков. Сюда входили классические параметры, такие как объём крови в левом и правом отделах сердца и выброс при каждом сокращении, а также более новые, целостные показатели насосной работы, сочетающие размеры сердца и массу миокарда. Все сканы были получены у участников UK Biobank — крупного исследования здоровья, а продвинутые компьютерные алгоритмы автоматически и последовательно выделяли камеры сердца более чем у 56 000 человек.
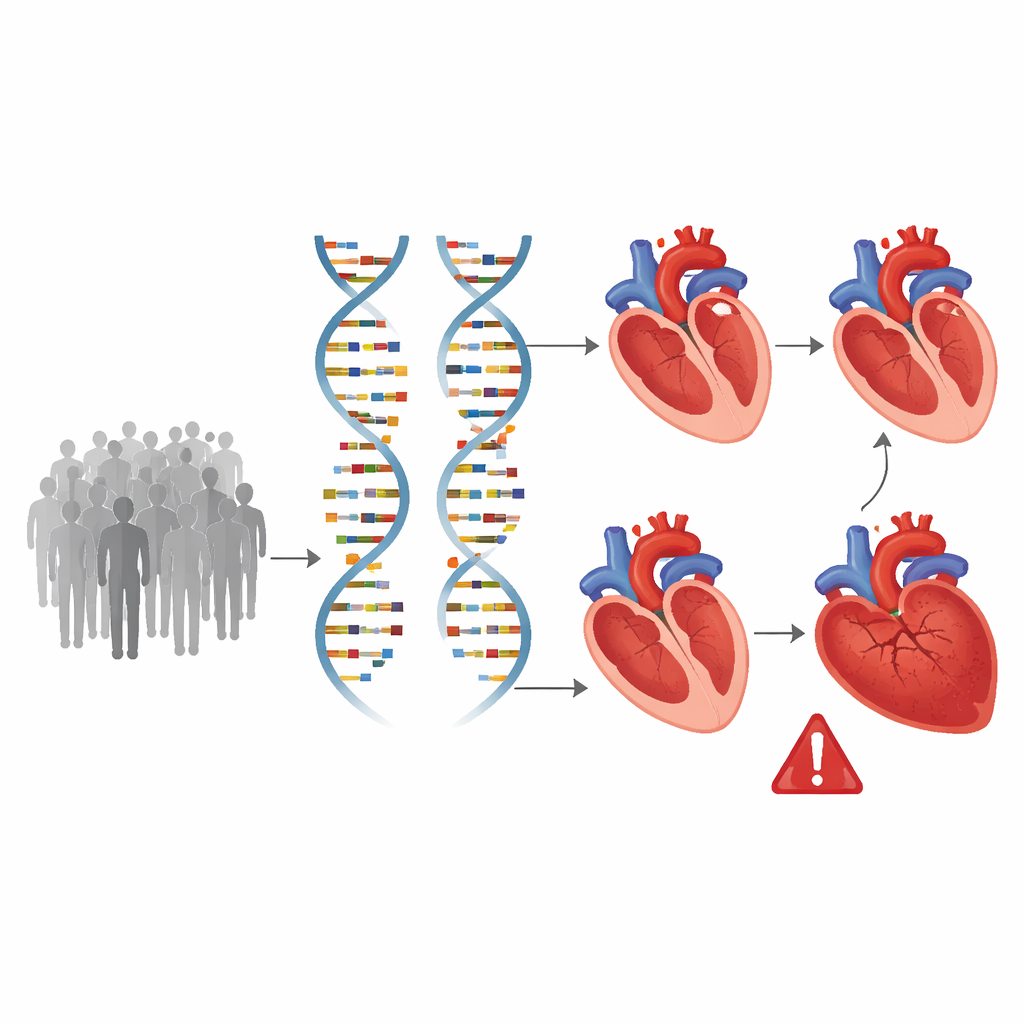
Поиск генов, формирующих сердце, по всему геному
Имея эти подробные измерения сердца, команда просканировала весь геном, протестировав около 8,9 миллиона распространённых генетических вариантов, чтобы увидеть, какие из них коррелируют с различиями в строении и функции желудочков. Были обнаружены 200 локусов в геноме, связанных по меньшей мере с одной чертой сердца, 58 из которых ранее не связывали с кардиальной визуализацией. Многие из этих генетических участков влияли сразу на несколько показателей, что указывает на общие биологические пути, затрагивающие и размер сердца, и его насосную силу. Расчёты показали, что наследственные факторы объясняют примерно от одной пятой до одной трети вариации этих признаков, подтверждая значительную роль ДНК в развитии и ремоделировании желудочков со временем.
От ДНК‑сигналов к риску болезни
Учёные затем изучили, как эти варианты, формирующие сердце, соотносятся с реальным риском заболеваний. Они сравнили свои результаты с предыдущими генетическими исследованиями сердечной недостаточности и других сердечно‑сосудистых состояний и выявили 23 геномные региона, которые, по‑видимому, влияют и на признаки желудочков, и на саму сердечную недостаточность. Некоторые гены в этих регионах уже известны как участники наследственных заболеваний сердечной мышцы, тогда как другие, например связанные с ответом на механическое напряжение или гипоксию, освещают дополнительные биологические пути повреждения. Построив полиgenные скоринговые показатели — совмещённые меры многих небольших эффектов ДНК — команда показала, что у людей, чья генетика предсказывает более расширенные или утолщённые желудочки, чаще встречаются сердечная недостаточность, гипертония и нарушения ритма. Напротив, генетические профили, сопровождающиеся более эффективной насосной функцией, фиксируемой новыми показателями, такими как индекс глобальной функции левого желудочка и фракция сокращения миокарда, были связаны с пониженным риском этих заболеваний.
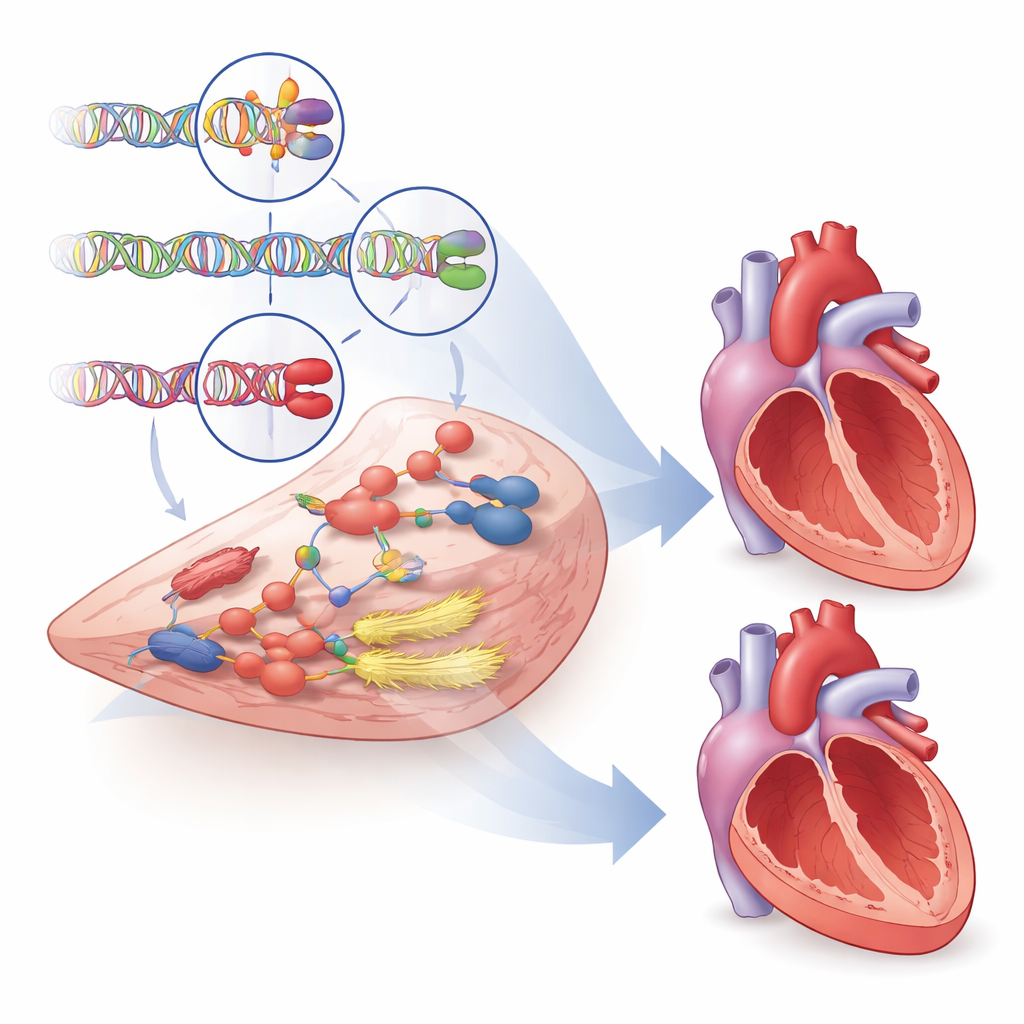
Подсказки для новых и лучших терапий
Помимо объяснения, почему одни сердца более уязвимы, чем другие, исследование искало гены, которые могли бы стать мишенями для лекарств. С помощью нескольких баз данных, данных на животных и паттернов активности генов авторы систематически оценили более тысячи близлежащих генов и выделили почти 500 с доказательствами роли в строении и функции желудочков. Десятки из этих генов взаимодействуют с существующими кардиологическими препаратами, в том числе с лекарствами, влияющими на сократимость миокарда и тонус сосудов, что указывает на возможности репозиционирования или оптимизации терапии. Яркий пример — ген PDE3A: его варианты связаны с признаками вредного ремоделирования. Существующие препараты блокируют как PDE3A, так и ближайший родственник PDE3B, но генетические данные указывают, что разработка средств, более селективно нацеленных на PDE3A, может улучшить исходы и уменьшить побочные эффекты, наблюдаемые при нынешних неселективных препаратах.
Что это значит для пациентов
Проще говоря, это исследование связывает крошечные различия в нашей ДНК с тем, как устроены главные насосные камеры сердца и насколько хорошо они работают, а затем связывает эти закономерности с тем, кто с большей вероятностью разовьёт сердечную недостаточность. Объединив передовую визуализацию, крупномасштабную генетику и анализ лекарственных мишеней, исследование не только углубляет наше понимание причин сердечной недостаточности, но и указывает на конкретные молекулярные «ручки», за которые в будущем могут ухватиться лекарства. Хотя необходимы дополнительные исследования — особенно в различных популяциях и в лабораторных моделях — эти результаты приближают нас к будущему, где скан и генетический тест вместе помогут раннему прогнозу сердечной недостаточности и направят более точные, основанные на генетике лечения.
Цитирование: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
Ключевые слова: сердечная недостаточность, кардиальная МРТ, генетика, ремоделирование желудочков, целевые препараты