Clear Sky Science · it
Analisi genome‑wide dei fenotipi ventricolari cardiaci rivela nuovi loci e bersagli terapeutici per l’insufficienza cardiaca
Perché il codice nascosto del cuore è importante
L’insufficienza cardiaca è una delle principali cause di morte e disabilità, eppure quando compaiono i sintomi gran parte del danno al cuore è già avvenuto. Oggi i medici possono ottenere immagini dettagliate delle principali camere pompanti del cuore, i ventricoli sinistro e destro, per valutarne il funzionamento. Fino a poco tempo fa però sapevamo molto meno sul codice genetico che plasma queste strutture e su come possa indicare nuovi trattamenti. Questo studio esplora il DNA di oltre cinquantaseimila persone per scoprire come migliaia di piccole differenze genetiche influenzino le dimensioni del cuore, la sua forza e, in ultima istanza, il rischio di insufficienza cardiaca.
Alla scoperta di migliaia di cuori
I ricercatori hanno utilizzato la risonanza magnetica cardiaca, un metodo di imaging molto preciso, per misurare venti aspetti della struttura e della funzione ventricolare. Tra questi figurano misure classiche, come il volume e la frazione di eiezione dei ventricoli destro e sinistro, e misure più recenti e olistiche delle prestazioni di pompaggio che combinano dimensione cardiaca e massa muscolare. Tutte le scansioni provenivano da partecipanti allo UK Biobank, un ampio studio sanitario, e algoritmi informatici avanzati sono stati usati per tracciare automaticamente e in modo coerente le camere cardiache in oltre 56.000 persone.
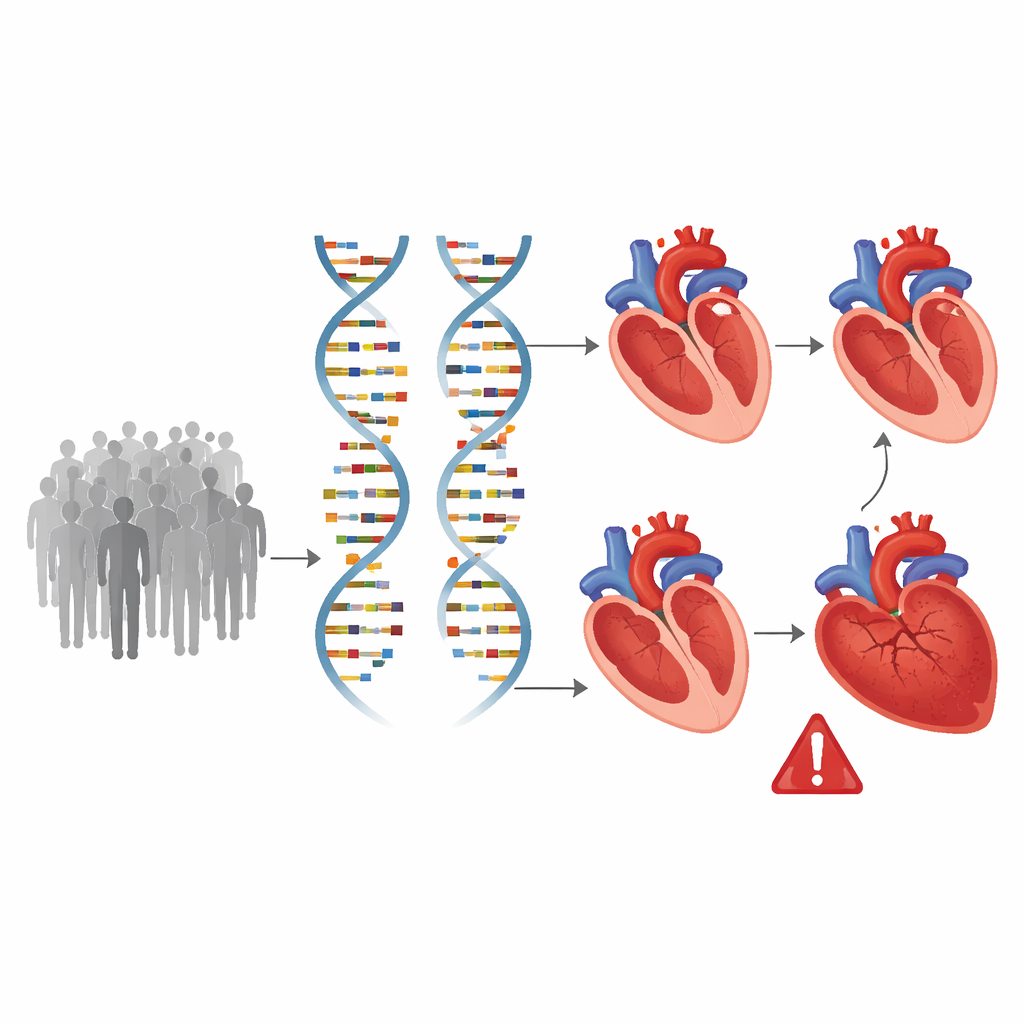
Individuare i geni che modellano il cuore nel genoma
Con queste misure cardiache dettagliate, il gruppo ha scandagliato l’intero genoma, testando circa 8,9 milioni di varianti genetiche comuni per vedere quali fossero associate a differenze nella struttura e nella funzione ventricolare. Hanno identificato 200 posizioni nel genoma legate ad almeno una delle caratteristiche cardiache, 58 delle quali non erano state precedentemente collegate all’imaging cardiaco. Molti di questi siti genetici influenzano più di una misura, suggerendo vie biologiche condivise che interessano sia la dimensione del cuore sia la sua capacità di pompa. I calcoli hanno mostrato che i fattori ereditari spiegano approssimativamente un quinto‑un terzo della variazione di questi tratti, confermando che il nostro DNA gioca un ruolo sostanziale nello sviluppo e nel rimodellamento ventricolare nel tempo.
Dai segnali del DNA al rischio di malattia
Gli scienziati hanno quindi esaminato come queste varianti che modellano il cuore si rapportino alle malattie reali. Hanno confrontato i loro risultati con studi genetici precedenti su insufficienza cardiaca e altre condizioni cardiovascolari e hanno trovato 23 regioni genomiche che sembrano influenzare sia i tratti ventricolari sia l’insufficienza cardiaca stessa. Alcuni geni in queste regioni sono già noti per il loro ruolo nelle cardiomiopatie ereditarie, mentre altri, per esempio quelli coinvolti nella risposta allo stress meccanico o all’ipossia, evidenziano ulteriori vie biologiche al danno. Costruendo punteggi di rischio poligenici — misure combinate di molti piccoli effetti genetici — il team ha mostrato che le persone la cui genetica predice ventricoli più dilatati o ispessiti presentano tassi più elevati di insufficienza cardiaca, ipertensione e disturbi del ritmo. Al contrario, profili genetici che favoriscono un pompaggio più efficiente, catturati da misure più recenti come l’indice globale di funzione ventricolare sinistra e la frazione di contrazione miocardica, sono stati associati a un rischio più basso di queste malattie.
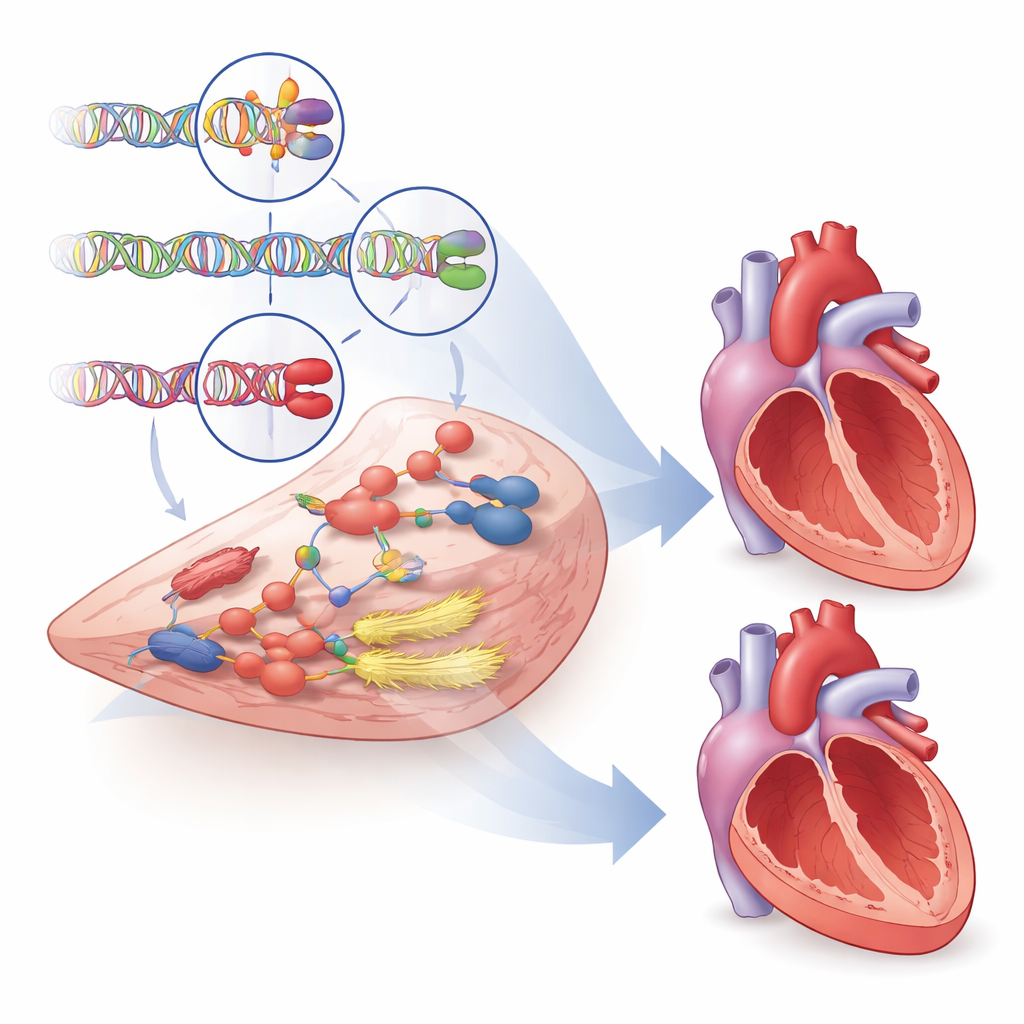
Indizi per terapie nuove e migliori
Oltre a spiegare perché alcuni cuori sono più vulnerabili, lo studio ha cercato geni che potrebbero diventare bersagli farmacologici. Utilizzando più banche dati, studi animali e profili di espressione genica, gli autori hanno valutato sistematicamente più di mille geni vicini e ne hanno evidenziati quasi 500 con prove di coinvolgimento nella struttura e nella funzione ventricolare. Dozzine di questi geni interagiscono con farmaci cardiovascolari esistenti, inclusi medicinali che influenzano la contrazione miocardica e il tono dei vasi sanguigni, indicando opportunità per riposizionare o perfezionare terapie. Un esempio notevole è il gene PDE3A, le cui varianti sono state collegate a segni di rimodellamento dannoso. I farmaci attuali bloccano sia PDE3A sia il suo parente PDE3B, ma i dati genetici suggeriscono che sviluppare trattamenti che mirino più selettivamente PDE3A potrebbe migliorare gli esiti evitando effetti collaterali associati ai farmaci non selettivi attuali.
Cosa significa per i pazienti
In termini concreti, questa ricerca collega piccole differenze nel nostro DNA al modo in cui le principali camere pompanti del cuore sono costruite e funzionano, e poi associa quei modelli a chi è più probabile sviluppare insufficienza cardiaca. Combinando imaging all’avanguardia, genetica su larga scala e analisi dei bersagli farmacologici, lo studio non solo approfondisce la nostra comprensione del perché il cuore fallisca, ma indica anche prese molecolari concrete su cui potrebbero agire i farmaci futuri. Pur essendo necessari ulteriori studi — soprattutto in popolazioni diverse e in modelli di laboratorio — questi risultati ci avvicinano a un futuro in cui una scansione e un test genetico insieme aiutino a prevedere precocemente l’insufficienza cardiaca e a guidare trattamenti più precisi e informati geneticamente.
Citazione: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
Parole chiave: insufficienza cardiaca, risonanza magnetica cardiaca, genetica, rimodellamento ventricolare, bersagli farmacologici