Clear Sky Science · de
Genomweite Analyse kardialer Ventrikelphänotypen enthüllt neue Loci und therapeutische Zielstrukturen für Herzinsuffizienz
Warum der verborgene Code des Herzens wichtig ist
Herzinsuffizienz gehört zu den häufigsten Todes‑ und Invaliditätsursachen, doch zum Zeitpunkt des Auftretens von Symptomen ist ein Großteil des Schadens am Herzen bereits eingetreten. Ärztinnen und Ärzte können inzwischen hochauflösende Aufnahmen der wichtigsten Auswurfflächen, der linken und rechten Ventrikel, erstellen, um deren Funktion zu beurteilen. Bis vor kurzem wussten wir jedoch deutlich weniger über den genetischen Code, der diese Strukturen formt, und darüber, wie er auf neue Behandlungsansätze hinweisen könnte. Diese Studie durchleuchtet die DNA von mehr als 56.000 Menschen, um aufzudecken, wie tausende kleiner genetischer Unterschiede Herzgröße, Kraft und letztlich das Risiko für Herzinsuffizienz beeinflussen.
Blick in Tausende Herzen
Die Forschenden nutzten die kardiale Magnetresonanztomographie, eine sehr präzise Untersuchungsmethode, um zwanzig Aspekte des Aufbaus und der Pumpleistung der Ventrikel zu messen. Dazu gehörten klassische Messgrößen wie das Schlagvolumen der linken und rechten Herzhälften sowie neuere, ganzheitlichere Kennzahlen der Pumpfunktion, die Herzgröße und Muskelmasse kombinieren. Alle Aufnahmen stammten aus der UK Biobank, einer großen Gesundheitsstudie, und fortschrittliche Computeralgorithmen wurden eingesetzt, um die Herzkammern bei über 56.000 Personen automatisch und konsistent zu segmentieren.
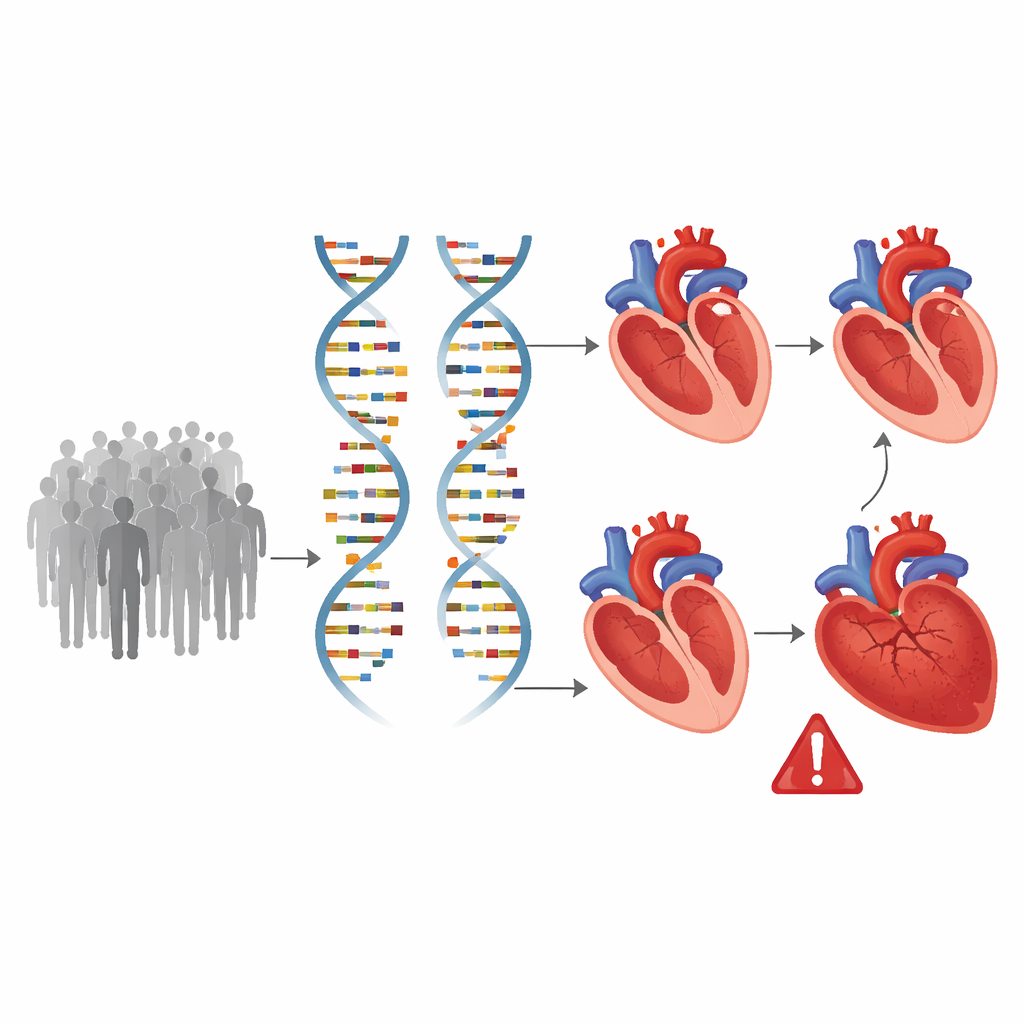
Herzformende Gene im gesamten Genom finden
Mit diesen detaillierten Herzmessungen durchsuchte das Team das gesamte Genom und testete etwa 8,9 Millionen häufige genetische Varianten darauf, welche mit Unterschieden in Ventrikelstruktur und -funktion zusammenhängen. Sie identifizierten 200 Genomstellen, die mit mindestens einem Herzmerkmal verknüpft sind, davon 58, die zuvor nicht mit kardialen Bildgebungsbefunden assoziiert waren. Viele dieser genetischen Orte beeinflussten mehr als eine Messgröße, was auf gemeinsame biologische Wege hindeutet, die sowohl Herzgröße als auch Pumpleistung betreffen. Berechnungen zeigten, dass vererbte Faktoren ungefähr ein Fünftel bis ein Drittel der Variabilität dieser Merkmale erklären, was bestätigt, dass unsere DNA eine bedeutsame Rolle bei der Entwicklung und Remodellierung der Ventrikel über die Zeit spielt.
Von DNA‑Signalen zum Krankheitsrisiko
Die Wissenschaftlerinnen und Wissenschaftler untersuchten anschließend, wie sich diese herzformenden Varianten auf das reale Krankheitsgeschehen auswirken. Sie verglichen ihre Ergebnisse mit früheren genetischen Studien zu Herzinsuffizienz und anderen Herz‑Kreislauf‑Erkrankungen und fanden 23 genomische Regionen, die offenbar sowohl Ventrikelmerkmale als auch Herzinsuffizienz beeinflussen. Einige Gene in diesen Regionen sind bereits als Verursacher genetisch bedingter Herzmuskelerkrankungen bekannt, andere, etwa solche, die an der Reaktion auf mechanische Belastung oder niedrigen Sauerstoff beteiligt sind, weisen auf zusätzliche biologische Pfade zur Schädigung hin. Durch den Aufbau polygener Risikoscores — kombinierte Maße vieler kleiner DNA‑Effekte — zeigte das Team, dass Menschen, deren Genetik zu vergrößerten oder verdickten Ventrikeln tendiert, auch höhere Raten von Herzinsuffizienz, Bluthochdruck und Herzrhythmusstörungen aufweisen. Demgegenüber waren genetische Profile, die eine effizientere Pumpfunktion begünstigen — erfasst durch neuere Messgrößen wie den linken ventrikulären Global Function Index und die Myokardial Contraction Fraction — mit einem geringeren Risiko für diese Erkrankungen verbunden.
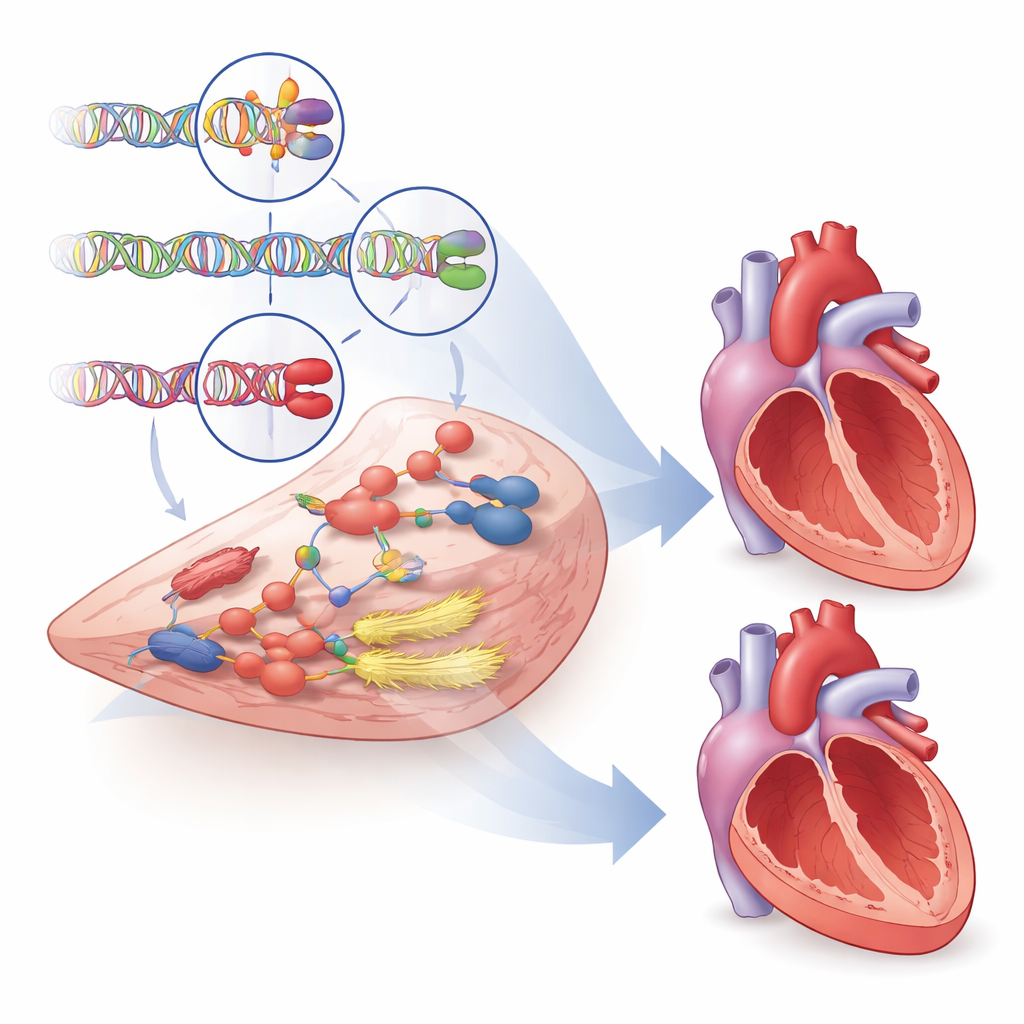
Hinweise auf neue und bessere Behandlungen
Über die Erklärung, warum manche Herzen anfälliger sind als andere, suchte die Studie nach Genen, die sich als Arzneimittelziele eignen könnten. Mithilfe mehrerer Datenbanken, Tierstudien und Muster der Genexpression beurteilten die Autorinnen und Autoren systematisch mehr als tausend benachbarte Gene und hoben nahezu 500 mit Evidenz für eine Beteiligung an Ventrikelstruktur und -funktion hervor. Dutzende dieser Gene interagieren mit bestehenden kardiovaskulären Medikamenten, darunter Substanzen, die Kontraktion des Herzmuskels und den Gefäßtonus beeinflussen, was Chancen für ein Repositionieren oder Verfeinern von Therapien aufzeigt. Ein auffälliges Beispiel ist das Gen PDE3A: Varianten darin standen im Zusammenhang mit Zeichen schädlicher Remodellierung. Bestehende Medikamente hemmen sowohl PDE3A als auch das nahe verwandte PDE3B, doch deuten die genetischen Daten darauf hin, dass eine selektivere Hemmung von PDE3A die Ergebnisse verbessern könnte, während Nebenwirkungen vermieden werden, die bei aktuellen nicht‑selektiven Wirkstoffen auftreten.
Was das für Patientinnen und Patienten bedeutet
Alltäglich ausgedrückt verbindet diese Forschung winzige Unterschiede in unserer DNA mit der Bauweise und Funktion der wichtigsten Herzkammern und verknüpft diese Muster mit der Wahrscheinlichkeit, eine Herzinsuffizienz zu entwickeln. Durch die Kombination modernster Bildgebung, groß angelegter Genetik und Analyse potenzieller Arzneimittelziele vertieft die Studie nicht nur unser Verständnis dafür, warum Herzen versagen, sondern weist auch auf konkrete molekulare Ansatzpunkte hin, die künftige Medikamente nutzen könnten. Zwar sind weitere Arbeiten nötig — insbesondere in diversen Bevölkerungsgruppen und in Laborversuchen —, doch rücken diese Befunde eine Zukunft näher, in der eine Aufnahme und ein Gentest gemeinsam helfen, Herzinsuffizienz früh vorherzusagen und präzisere, genetisch informierte Therapien zu steuern.
Zitation: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
Schlüsselwörter: Herzinsuffizienz, kardiale MRT, Genetik, ventrikuläre Remodellierung, Arzneimittelziele