Clear Sky Science · fr
Analyse à l’échelle du génome des phénotypes ventriculaires cardiaques révèle de nouveaux loci et cibles thérapeutiques pour l’insuffisance cardiaque
Pourquoi le code caché du cœur compte
L’insuffisance cardiaque est l’une des principales causes de décès et d’invalidité, mais lorsque les symptômes apparaissent, une grande partie des lésions cardiaques est déjà installée. Les médecins peuvent maintenant réaliser des examens détaillés des principales cavités de pompage du cœur, les ventricules gauche et droit, pour évaluer leur fonctionnement. Jusqu’à récemment, nous en savions beaucoup moins sur le code génétique qui façonne ces structures et sur la manière dont il pourrait indiquer de nouveaux traitements. Cette étude explore l’ADN de plus de cinquante‑six mille personnes pour révéler comment des milliers de petites différences génétiques influent sur la taille du cœur, sa puissance et, en fin de compte, le risque d’insuffisance cardiaque.
À l’intérieur de milliers de cœurs
Les chercheurs ont utilisé l’imagerie par résonance magnétique cardiaque, une méthode de scanner très précise, pour mesurer vingt aspects de la structure et du pompage des ventricules. Cela comprenait des mesures classiques, comme les volumes sanguins et l’éjection systolique des côtés gauche et droit, ainsi que des mesures plus récentes et plus globales de la performance de la pompe qui combinent taille cardiaque et masse musculaire. Tous les examens provenaient de participants de la UK Biobank, une grande étude de santé, et des algorithmes informatiques avancés ont servi à tracer automatiquement et de manière cohérente les cavités cardiaques chez plus de 56 000 personnes.
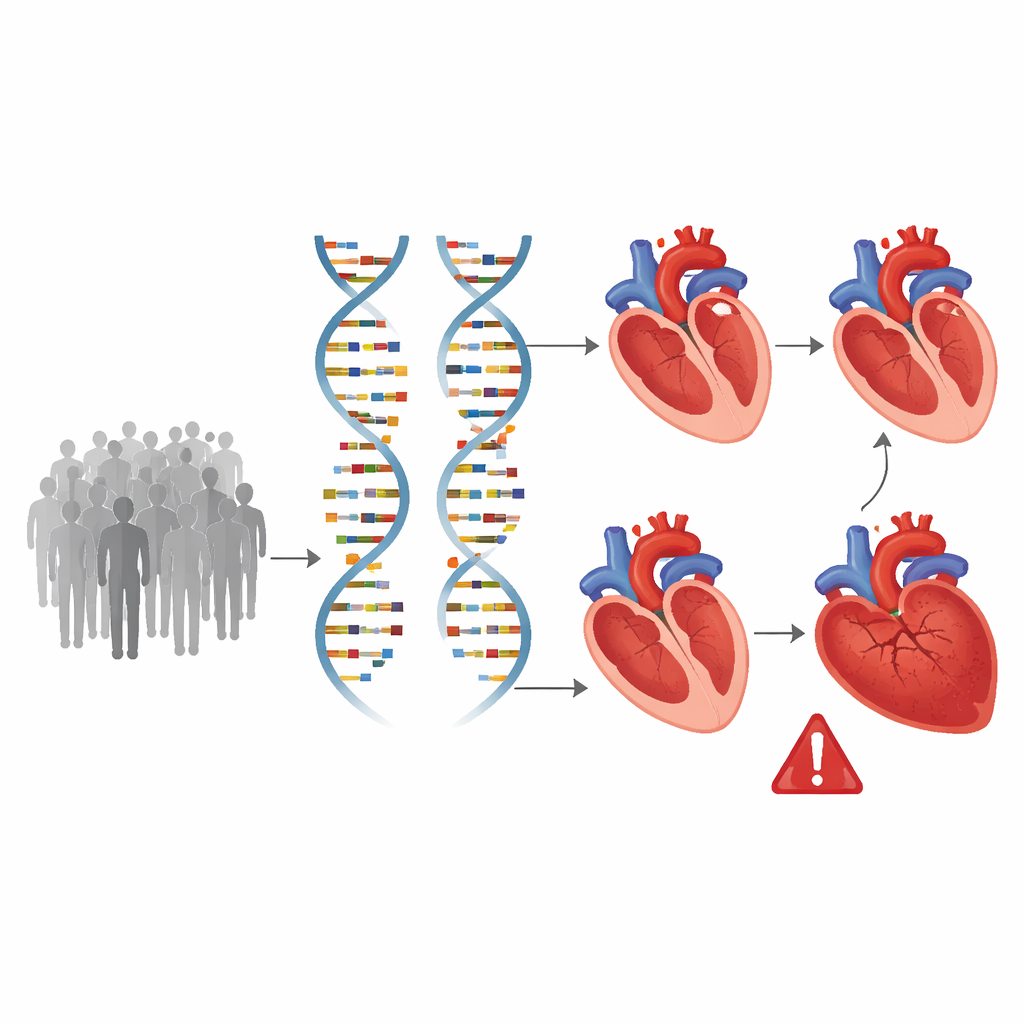
Identifier les gènes qui façonnent le cœur à l’échelle du génome
Munie de ces mesures cardiaques détaillées, l’équipe a parcouru le génome entier, testant environ 8,9 millions de variants génétiques courants pour voir lesquels étaient associés aux différences de structure et de fonction ventriculaires. Ils ont découvert 200 emplacements génomiques liés à au moins un des traits cardiaques, dont 58 n’avaient pas été précédemment associés à l’imagerie cardiaque. Nombre de ces sites génétiques influençaient plus d’une mesure, suggérant des voies biologiques partagées affectant à la fois la taille du cœur et sa puissance de pompage. Les calculs ont montré que les facteurs héréditaires expliquent environ un cinquième à un tiers de la variation de ces traits, confirmant que notre ADN joue un rôle important dans le développement et le remodelage des ventricules au fil du temps.
Des signaux d’ADN au risque de maladie
Les scientifiques ont ensuite étudié comment ces variants « façonneurs de cœur » se rapportent aux maladies réelles. Ils ont comparé leurs résultats à des études génétiques antérieures sur l’insuffisance cardiaque et d’autres affections cardiovasculaires et ont identifié 23 régions génomiques qui semblent influencer à la fois les traits ventriculaires et l’insuffisance cardiaque elle‑même. Certains gènes dans ces régions sont déjà connus pour intervenir dans les cardiomyopathies héréditaires, tandis que d’autres, par exemple ceux impliqués dans la réponse au stress mécanique ou à l’hypoxie, soulignent des voies biologiques additionnelles menant aux lésions. En construisant des scores de risque polygénique — des mesures combinées de nombreux petits effets de l’ADN — l’équipe a montré que les personnes dont la génétique prédit des ventricules plus dilatés ou épaissis présentent aussi des taux plus élevés d’insuffisance cardiaque, d’hypertension et de troubles du rythme. À l’inverse, des profils génétiques favorisant un pompage plus efficace, captés par des mesures récentes comme l’indice global de fonction ventriculaire gauche et la fraction de contraction myocardique, étaient associés à un moindre risque de ces maladies.
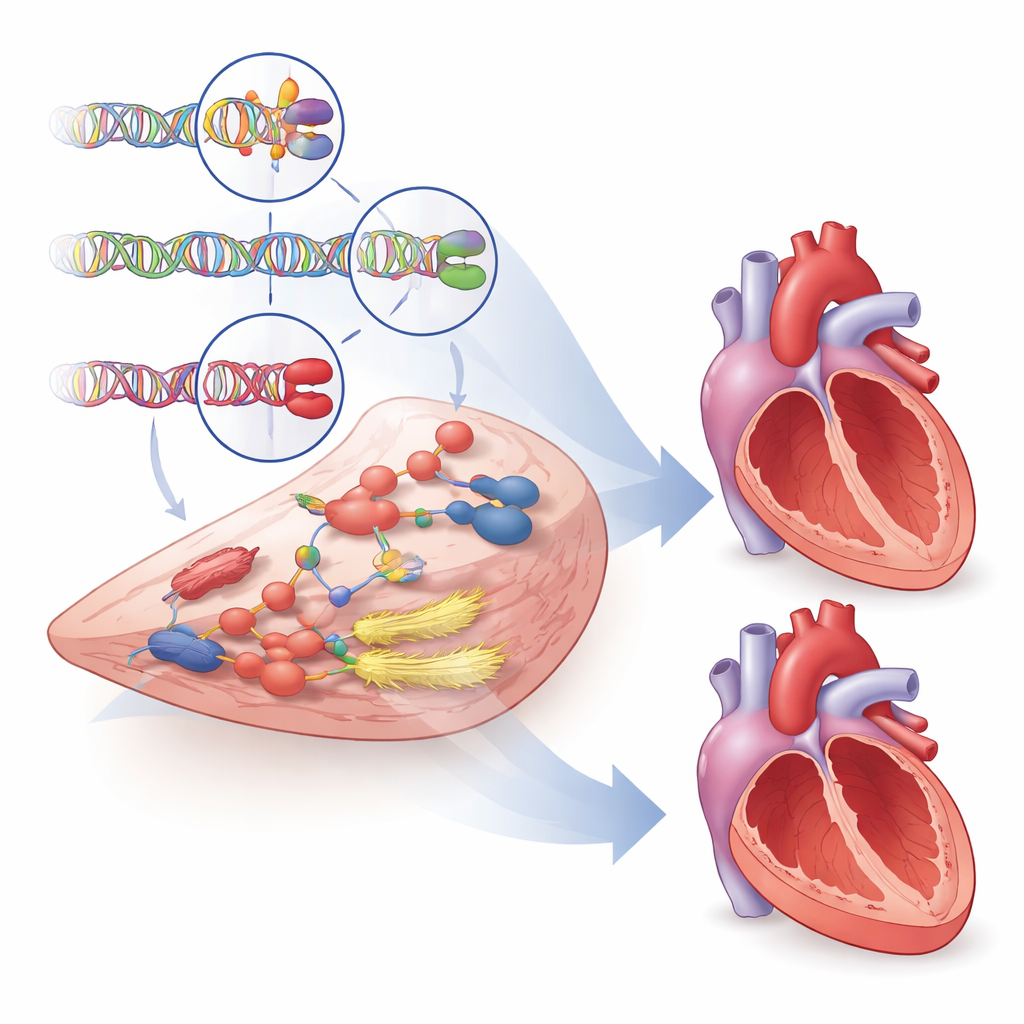
Indications pour de nouveaux traitements
Au‑delà d’expliquer pourquoi certains cœurs sont plus vulnérables, l’étude a recherché des gènes susceptibles de devenir des cibles médicamenteuses. En utilisant plusieurs bases de données, des études animales et des profils d’expression génique, les auteurs ont évalué de façon systématique plus d’un millier de gènes proches et ont mis en évidence près de 500 gènes avec des preuves d’implication dans la structure et la fonction ventriculaires. Des dizaines de ces gènes interagissent avec des médicaments cardiovasculaires existants, notamment des drogues qui modulent la contraction myocardique et le tonus vasculaire, ouvrant des opportunités de repositionnement ou d’amélioration des traitements. Un exemple marquant est le gène PDE3A, dont les variants ont été associés à des signes de remodelage délétère. Les médicaments actuels bloquent à la fois PDE3A et son homologue PDE3B, mais les données génétiques suggèrent que concevoir des traitements ciblant plus sélectivement PDE3A pourrait améliorer les résultats tout en évitant des effets indésirables observés avec les médicaments non sélectifs actuels.
Ce que cela signifie pour les patients
Concrètement, cette recherche relie de minuscules différences de notre ADN à la manière dont sont construites les principales cavités de pompage du cœur et à leur efficacité, puis associe ces profils au risque d’insuffisance cardiaque. En combinant imagerie de pointe, génétique à grande échelle et analyse des cibles médicamenteuses, l’étude enrichit non seulement notre compréhension des raisons de l’insuffisance cardiaque, mais met aussi en lumière des cibles moléculaires concrètes que de futurs médicaments pourraient exploiter. Bien que des travaux supplémentaires soient nécessaires — notamment dans des populations diversifiées et sur des modèles de laboratoire — ces résultats nous rapprochent d’un avenir où un examen et un test génétique conjoints aideront à prédire précocement l’insuffisance cardiaque et à guider des traitements plus précis, informés par la génétique.
Citation: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
Mots-clés: insuffisance cardiaque, IRM cardiaque, génétique, remodelage ventriculaire, cibles médicamenteuses