Clear Sky Science · sv
Genomeomfattande analys av hjärtventrikulära fenotyper avslöjar nya locus och terapeutiska mål för hjärtsvikt
Varför hjärtats dolda kod spelar roll
Hjärtsvikt är en av de ledande orsakerna till död och funktionsnedsättning, men när symtomen väl syns har mycket av skadan på hjärtat redan skett. Läkare kan nu ta detaljerade avbildningar av hjärtats huvudpumpkammare, vänster och höger kammare, för att bedöma hur väl de fungerar. Men fram tills nyligen visste vi betydligt mindre om den genetiska koden som formar dessa strukturer och hur den skulle kunna peka mot nya behandlingar. Denna studie dyker ner i DNA från mer än femtiosex tusen personer för att avslöja hur tusentals små genetiska skillnader påverkar hjärtats storlek, kraft och i förlängningen risken för hjärtsvikt.
Insyn i tusentals hjärtan
Forskarna använde hjärtmagnetisk resonansavbildning, en mycket precis skanningsmetod, för att mäta tjugo aspekter av hur ventriklarna är byggda och hur de pumpar blod. Detta inkluderade klassiska mått såsom hur mycket blod vänster och höger sida av hjärtat rymmer och tömmer vid varje slag, samt nyare, mer holistiska mått på pumpfunktion som kombinerar hjärtstorlek och muskelmassa. Alla bilder kom från deltagare i UK Biobank, en stor hälsoenkät, och avancerade datoralgoritmer användes för att automatisk och konsekvent avgränsa hjärtrummen hos mer än 56 000 personer.
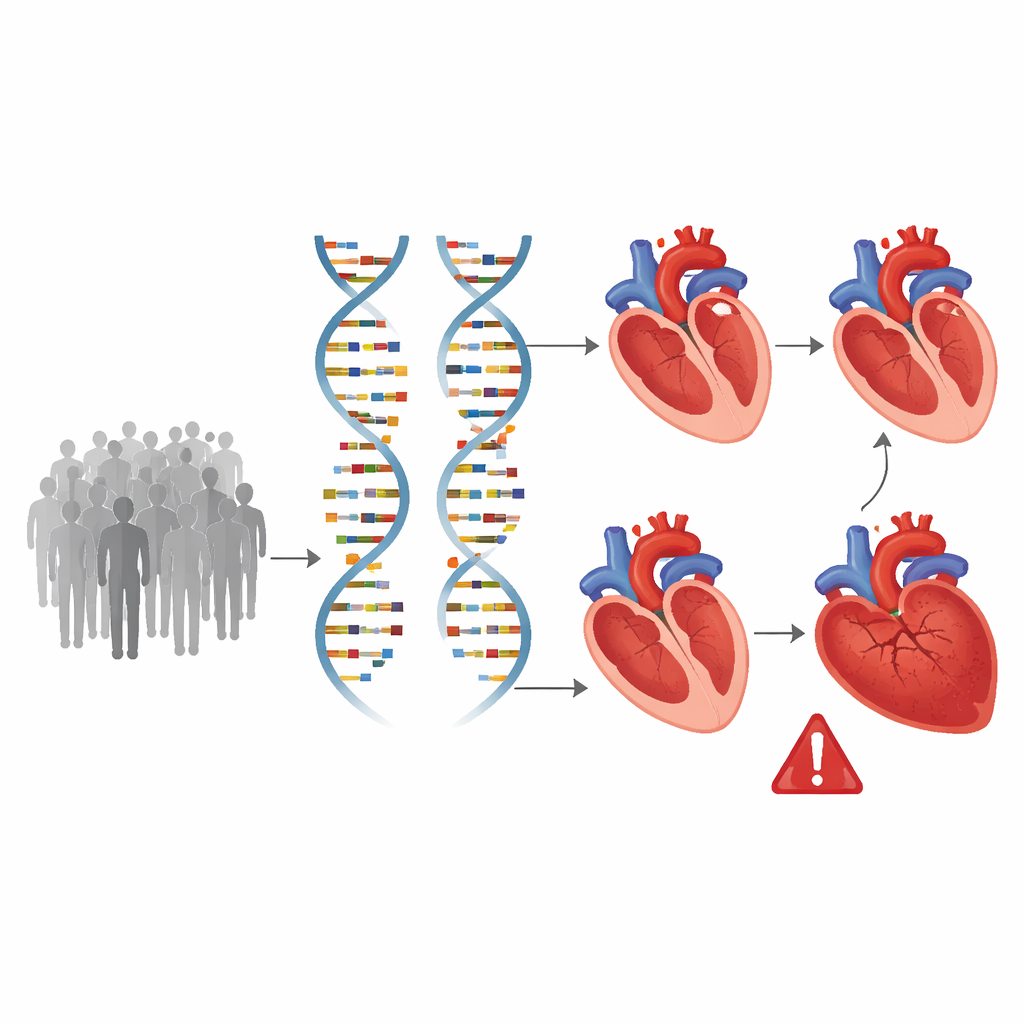
Att hitta gener som formar hjärtat över hela genomet
Utrustade med dessa detaljerade hjärtuppgifter skannade teamet hela genomet och testade omkring 8,9 miljoner vanliga genetiska varianter för att se vilka som korrelerade med skillnader i ventrikulär struktur och funktion. De upptäckte 200 platser i genomet kopplade till åtminstone ett av hjärtfenotyperna, varav 58 tidigare inte hade förknippats med hjärtavbildning. Många av dessa genetiska platser påverkade mer än ett mått, vilket tyder på delade biologiska vägar som påverkar både hjärtstorlek och pumpkraft. Beräkningar visade att ärftliga faktorer förklarar ungefär en femtedel till en tredjedel av variationen i dessa egenskaper, vilket bekräftar att vårt DNA spelar en betydande roll i hur våra ventriklar utvecklas och byggs om över tid.
Från DNA-signaler till sjukdomsrisk
Forskarna frågade sedan hur dessa hjärtformande varianter relaterar till verklig sjukdom. De jämförde sina fynd med tidigare genetiska studier av hjärtsvikt och andra kardiovaskulära tillstånd och fann 23 genomiska regioner som verkar påverka både ventrikulära egenskaper och själva hjärtsvikten. Några gener i dessa regioner är redan kända aktörer vid ärftlig hjärtmuskelsjukdom, medan andra, exempelvis de som är involverade i svar på mekanisk belastning eller lågt syre, belyser ytterligare biologiska vägar till skada. Genom att bygga polygenetiska riskpoäng — samlade mått av många små DNA-effekter — visade teamet att personer vars genetik förutsäger mer förstorade eller förtjockade ventriklar också har högre incidens av hjärtsvikt, högt blodtryck och rytmrubbningar. Däremot kopplades genetiska profiler som favoriserar effektivare pumpning, fångade av nyare mått som vänsterkammarens globala funktionsindex och myokardiets kontraktionsfraktion, till lägre risk för dessa sjukdomar.
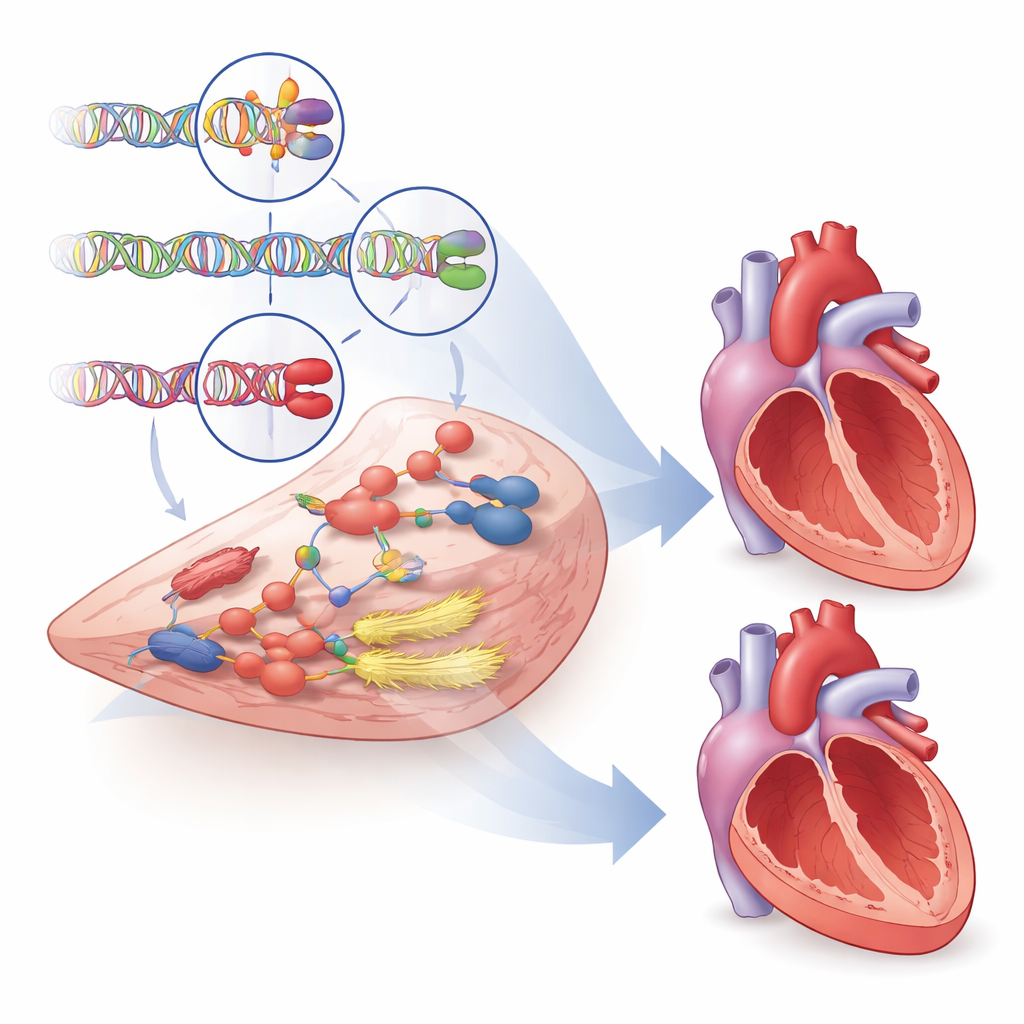
Ledtrådar till nya och bättre behandlingar
Bortom att förklara varför vissa hjärtan är mer sårbara än andra, sökte studien efter gener som skulle kunna bli läkemedelsmål. Genom att använda flera databaser, djurstudier och mönster i genaktivitet scoreade författarna systematiskt mer än tusen närliggande gener och lyfte fram nästan 500 med bevis för inblandning i ventrikulär struktur och funktion. Dussintals av dessa gener interagerar med befintliga kardiovaskulära läkemedel, inklusive läkemedel som påverkar hjärtmuskelns kontraktion och blodkärlens tonus, vilket pekar på möjligheter för omfördelning eller förfining av terapier. Ett slående exempel är en gen kallad PDE3A, vars varianter kopplades till tecken på skadlig ombyggnad. Befintliga läkemedel blockerar både PDE3A och dess närbesläktade PDE3B, men de genetiska uppgifterna tyder på att utformning av behandlingar som mer selektivt riktar sig mot PDE3A skulle kunna förbättra utfall och samtidigt undvika biverkningar som ses med dagens icke‑selektiva läkemedel.
Vad detta betyder för patienter
I vardagliga termer kopplar denna forskning små skillnader i vårt DNA till hur hjärtats huvudpumpkammare är byggda och hur väl de fungerar, och länkar sedan dessa mönster till vem som löper större risk att utveckla hjärtsvikt. Genom att kombinera toppmodern bildteknik, storskalig genetik och analys av läkemedelsmål fördjupar studien inte bara vår förståelse för varför hjärtan sviktar utan pekar också på konkreta molekylära handtag som framtida läkemedel kan rikta in sig på. Ytterligare arbete behövs — särskilt i mångsidiga populationer och i laboratorium — men dessa fynd för oss närmare en framtid där en avbildning och ett genetiskt test tillsammans kan hjälpa till att förutsäga hjärtsvikt tidigt och styra mer precisa, genetiskt informerade behandlingar.
Citering: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
Nyckelord: hjärtsvikt, hjärt‑MRI, genetik, ventrikulär ombyggnad, läkemedelsmål