Clear Sky Science · ar
تحليل على مستوى الجينوم لظواهر بطين القلب يكشف مواقع جديدة وأهداف علاجية لفشل القلب
لماذا يهم الشيفرة المخفية للقلب
يُعد فشل القلب من الأسباب الرئيسية للوفاة والعجز، ومع ذلك بحلول ظهور الأعراض يكون الكثير من الضرر قد حدث بالفعل في القلب. يمكن للأطباء الآن إجراء مسح تفصيلي للغرف الضخّ الرئيسية في القلب، البطين الأيسر والبطين الأيمن، لرصد مدى كفاءتهما. لكن حتى وقت قريب كنا نعرف أقل بكثير عن الشيفرة الوراثية التي تشكل هذه البنى وكيف يمكن أن تشير إلى علاجات جديدة. تتعمق هذه الدراسة في حمض نووي لأكثر من ستة وخمسين ألف شخص لاكتشاف كيف تؤثر آلاف الاختلافات الوراثية الصغيرة في حجم القلب وقوته، وفي النهاية خطر الإصابة بفشل القلب.
نظرة داخل آلاف القلوب
استخدم الباحثون تصويرًا بالرنين المغناطيسي القلبي، وهو أسلوب مسح دقيق للغاية، لقياس عشرين جانبًا من كيفية بناء البطينات وكيفية ضخها للدم. شملت هذه المقاييس التقليدية مثل كمية الدم التي تمتلكها وتضخها الجهة اليسرى واليمنى من القلب مع كل نبضة، بالإضافة إلى مقاييس أحدث وأكثر شمولية لأداء الضخ تجمع بين حجم القلب وكتلة العضلة القلبية. جاءت جميع الفحوص من مشاركين في بنك المملكة المتحدة الحيوي، وهو دراسة صحية كبيرة، واستخدمت خوارزميات حاسوبية متقدمة لتتبع حجرات القلب تلقائيًا وبشكل متسق عبر أكثر من 56,000 شخص.
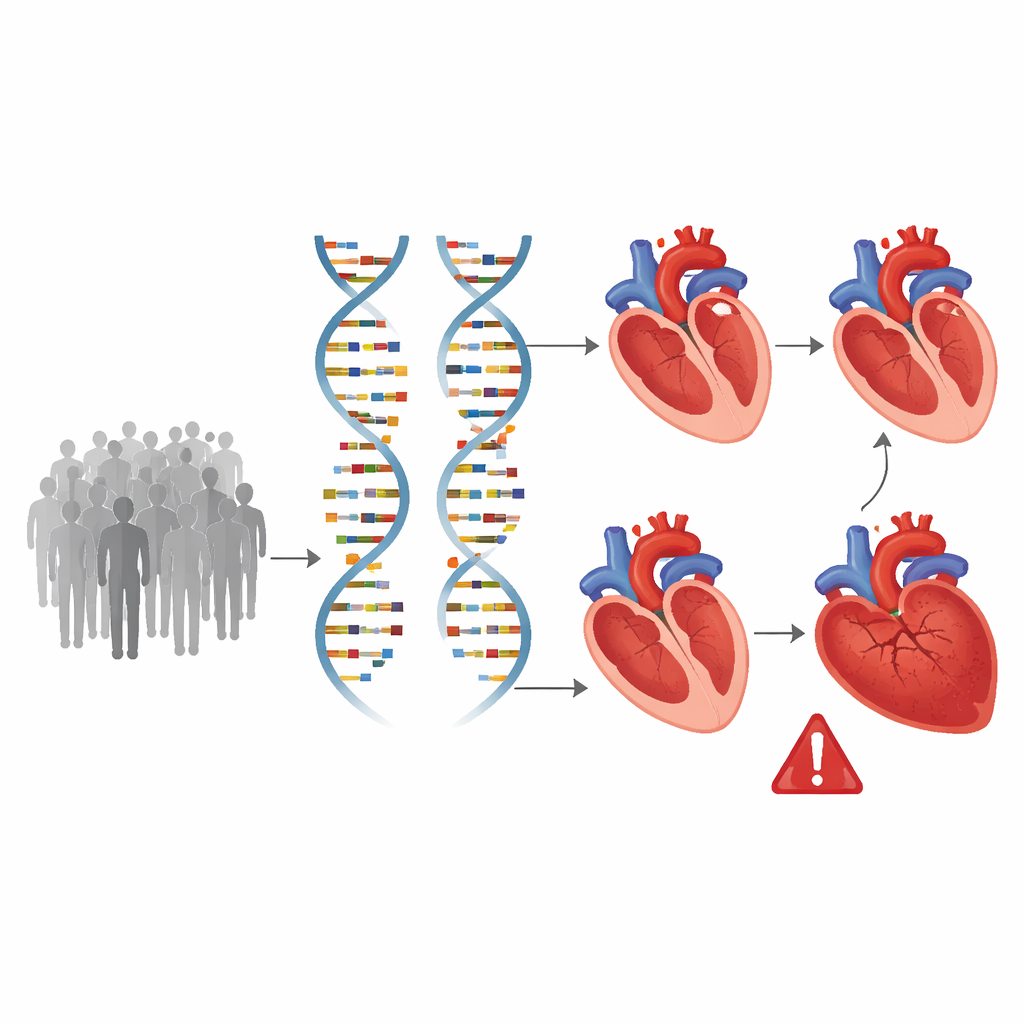
اكتشاف جينات تشكل القلب عبر الجينوم
مسلحين بهذه القياسات القلبية التفصيلية، أجرى الفريق مسحًا لكامل الجينوم، مختبرًا نحو 8.9 مليون متغير وراثي شائع لمعرفة أيها يتزامن مع اختلافات في بنية البطين ووظيفته. اكتشفوا 200 موقع في الجينوم مرتبطة بصفة واحدة على الأقل من صفات القلب، من بينها 58 موقعًا لم تربط سابقًا بتصوير القلب. أثر العديد من هذه المواقع الوراثية في أكثر من قياس واحد، مما يوحي بوجود مسارات بيولوجية مشتركة تؤثر على كل من حجم القلب وقوة الضخ. أظهرت الحسابات أن العوامل الموروثة تفسر نحو خُمس إلى ثلث التباين في هذه الصفات، مؤكدة أن حمضنا النووي يلعب دورًا جوهريًا في كيفية تطور البطينات وإعادة تشكيلها مع مرور الوقت.
من إشارات الحمض النووي إلى خطر المرض
سأل العلماء بعد ذلك كيف ترتبط هذه المتغيرات التي تشكل القلب بخطر المرض في العالم الواقعي. قارنوا نتائجهم مع دراسات وراثية سابقة لفشل القلب وحالات قلبية وعائية أخرى ووجدوا 23 منطقة جينومية تبدو أنها تؤثر في كل من صفات البطين وفشل القلب نفسه. بعض الجينات في هذه المناطق معروفة بالفعل كلاعبين في أمراض عضلة القلب الوراثية، في حين أن آخرين، مثل الجينات المشاركة في الاستجابة للإجهاد الميكانيكي أو نقص الأكسجة، يسلطون الضوء على مسارات بيولوجية إضافية للضرر. من خلال بناء درجات الخطر متعددة الجينات — مقاييس مجمعة للعديد من التأثيرات الصغيرة في الحمض النووي — أظهر الفريق أن الأشخاص الذين توحي جيناتهم ببطينات أكثر توسعًا أو سماكة لديهم أيضًا معدلات أعلى من فشل القلب وارتفاع ضغط الدم واضطرابات النظم. في المقابل، ارتبطت الملفات الجينية التي تفضّل ضخًا أكثر كفاءة، والتي تلتقطها مقاييس أحدث مثل مؤشر الوظيفة العالمية للبطين الأيسر وكسر انقباض العضلة القلبية، بانخفاض مخاطر هذه الأمراض.
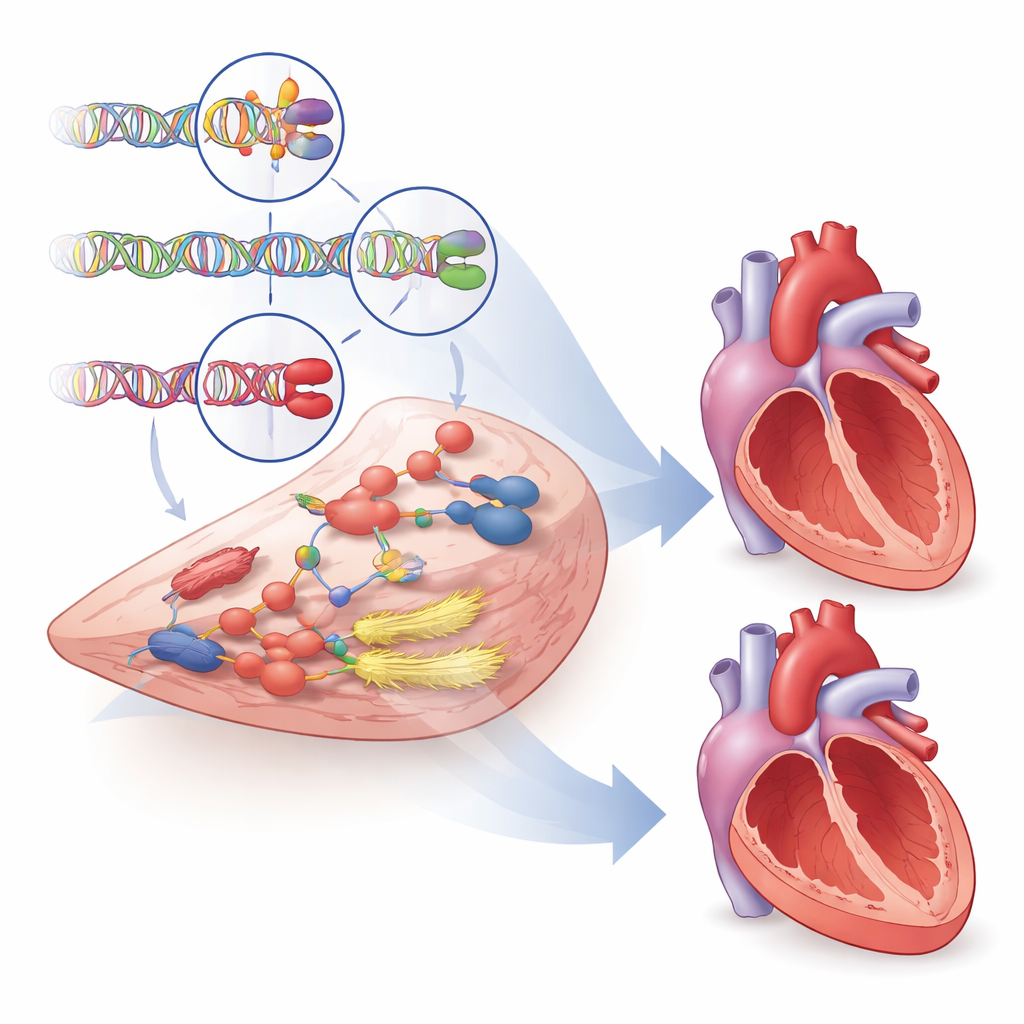
دلائل لعلاجات جديدة وأفضل
بعيدًا عن تفسير سبب تعرض بعض القلوب لهشاشة أكثر من غيرها، بحثت الدراسة عن جينات يمكن تحويلها إلى أهداف دوائية. باستخدام قواعد بيانات متعددة، ودراسات على الحيوانات، وأنماط نشاط الجينات، قيّم المؤلفون بشكل منهجي أكثر من ألف جين مجاور وأبرزوا ما يقرب من 500 جين يوجد دليل على تورطها في بنية البطين ووظيفته. تتفاعل عشرات من هذه الجينات مع أدوية قلبية وعائية موجودة، بما في ذلك أدوية تؤثر على انقباض عضلة القلب ونبرة الأوعية الدموية، مما يشير إلى فرص لإعادة توظيف الأدوية أو تحسينها. مثال لافت هو جين يسمى PDE3A، ارتبطت متغيراته بعلامات إعادة تشكيل ضار. تحجب الأدوية الحالية كلًا من PDE3A وقريبه PDE3B، لكن البيانات الوراثية توحي بأن تصميم علاجات تستهدف PDE3A بشكل أكثر انتقائية قد يحسن النتائج مع تجنّب آثار جانبية تُرى مع الأدوية غير الانتقائية الحالية.
ماذا يعني هذا للمرضى
بكلمات بسيطة، تربط هذه الأبحاث اختلافات طفيفة في حمضنا النووي بطريقة بناء البطينات الضخّ الرئيسة في القلب وكيفية أدائها، ثم تربط تلك الأنماط بمن هو أكثر عرضة لتطوير فشل القلب. من خلال الجمع بين تصوير متقدم، وبيانات وراثية واسعة النطاق، وتحليل أهداف دوائية، لا تُعمّق الدراسة فهمنا لسبب فشل القلوب فحسب، بل تشير أيضًا إلى مقابض جزيئية ملموسة قد تستهدفها أدوية مستقبلية. ومع أن هناك حاجة لمزيد من العمل — خصوصًا في مجموعات سكانية متنوعة ونماذج مخبرية — فإن هذه النتائج تقربنا من مستقبل يمكن فيه للمسح والاختبار الجيني معًا التنبؤ بفشل القلب مبكرًا وتوجيه علاجات أكثر دقة قائمة على الوراثة.
الاستشهاد: Nicholls, H.L., Vargas, J.D., Sanghvi, M.M. et al. Genome-wide analysis of cardiac ventricular phenotypes reveals novel loci and therapeutic targets for heart failure. Nat Commun 17, 3293 (2026). https://doi.org/10.1038/s41467-026-69982-0
الكلمات المفتاحية: فشل القلب, تصوير بالرنين المغناطيسي للقلب, علم الوراثة, إعادة تشكيل البطين, أهداف دوائية