Clear Sky Science · zh
连接组蛋白通过连接多个核小体巩固异质的核小体纤维接触
细胞内 DNA 的包装方式
你体内的每个细胞都要把近两米长的 DNA 压缩进远小于灰尘微粒的细胞核内。这种极端的包装不仅是储存技巧;它也参与决定哪些基因处于活跃或沉默状态。本研究深入探讨了这一过程中一个关键但常被忽视的角色——连接组蛋白,结果显示它们的作用更像是将多颗“珠子”和纤维联结在一起的多功能连接器,而不是只夹在单个 DNA 珠上的简单夹子。
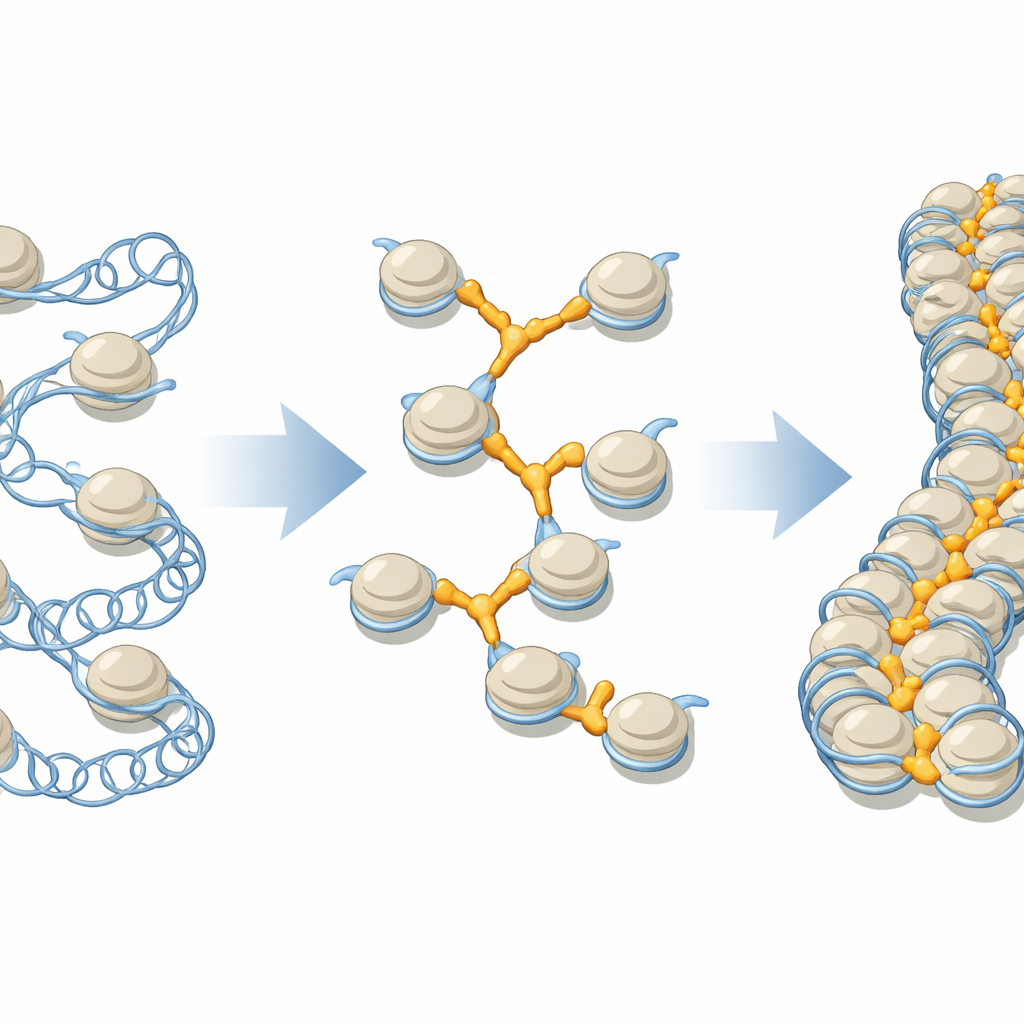
更近一步看 DNA 珠子及其连接子
我们的细胞中,DNA 绕着蛋白核形成称为核小体的单位,常被形象化为串在一起的珠子。这些珠子进一步折叠成更高阶的纤维,沿单条染色体可以延伸超过百万个单位。连接组蛋白——统称为 H1 的蛋白家族——长期以来被认为以标准方式位于每颗珠子上,帮助收紧局部结构。但细胞中存在若干不同的 H1 变体,每种在位置和功能上有偏好,而早期的结构学研究大多聚焦于孤立的珠子,而非真实染色体中拥挤、致密的环境。
构建模型纤维以揭示隐藏的结合模式
为探究连接组蛋白在致密环境中的行为,研究者设计了能自然拼接成连续纤维的核小体。这些设计的纤维可以结晶并通过 X 射线晶体学以近原子分辨率进行解析。将这些纤维与不同的连接组蛋白变体结合,包括 H1.0、H1x、H1.3 以及鸟类蛋白 H5,团队观察到的不仅是经典的“居中”结合到单个珠子的模式,还出现了多种替代排列,其中一枚连接组蛋白同时接触多枚核小体,甚至跨越多条纤维。实际上,H1 蛋白占据了只有当珠子在三维中紧密排列时才形成的富含 DNA 的口袋。
重塑 DNA 形态的多才连接器
这些结构快照显示,连接组蛋白的致密中央部分识别的是反复出现的 DNA 形状,而不仅仅是单一的固定位点。蛋白表面上的某些区域反复与双螺旋中变宽的沟槽和弯曲处相接,无论这些特征位于单个核小体的中心还是几枚核小体之间的特殊连接处。部分变体(如 H1x 和 H1.0)甚至能在特定位点弯曲 DNA,细微改变它在底层蛋白核心上的摆放方式。不同的 H1 类型偏好不同的结合模式:有些主要使用单一强接口,而另一些则使用两个稳固的接触区,形成依赖于蛋白变体和局部纤维几何的“连接模式”谱系。
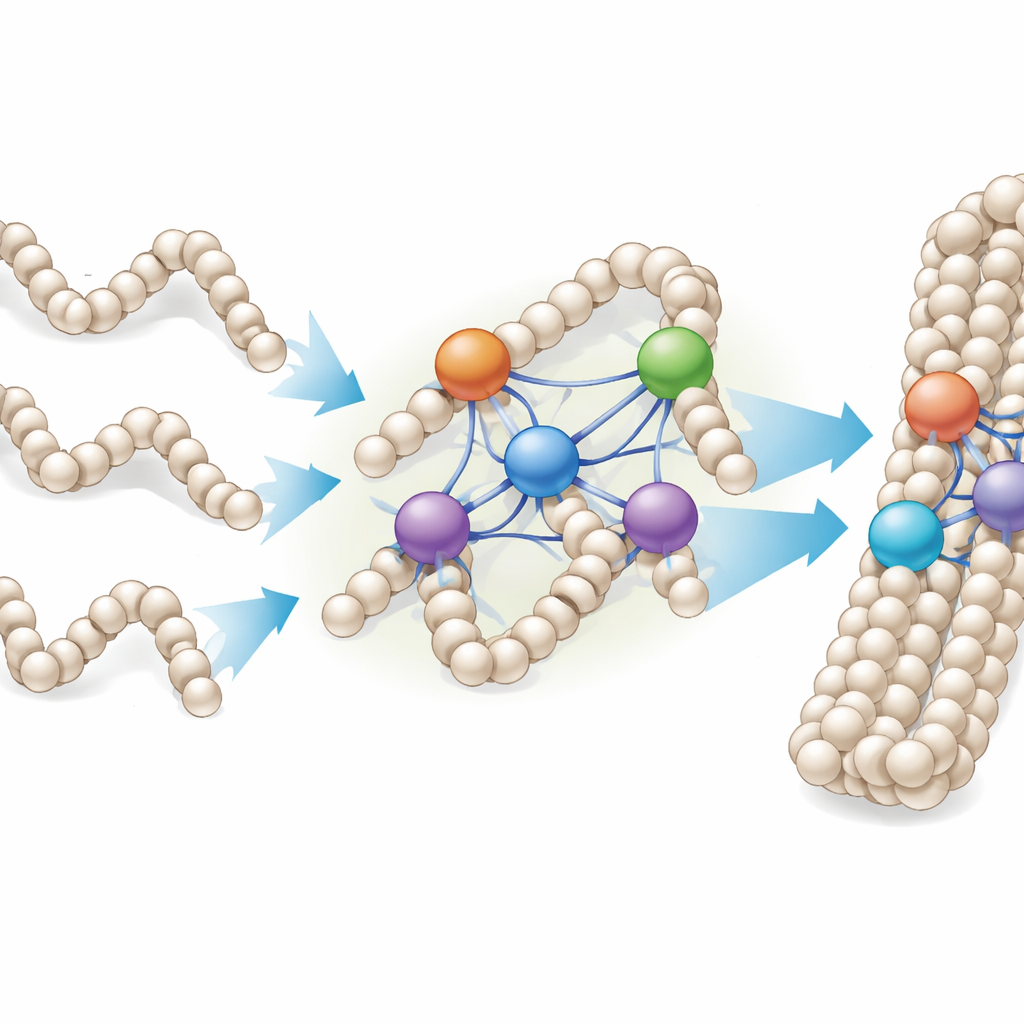
从单根纤维到致密的染色质液滴
鉴于活细胞中的染色体更像致密的染色质液滴而非整齐的孤立纤维,研究者还研究了连接组蛋白如何与实验室制备的染色质凝聚体结合——由许多重复核小体阵列组成的团块。他们发现 H1 蛋白并不会在与核小体达到简单一比一比例后就停止结合;相反,单个核小体可能与两到四个或更多 H1 分子相关联,具体取决于变体。在显微镜下,加入更多 H1 会促使小而球形的凝聚体融合为更大的链状“珠子”,表明连接组蛋白能将多个染色质液滴和纤维缝合成更致密的结构。
这对基因调控与疾病的意义
这些结果将连接组蛋白描绘成非僵硬地夹住单颗珠子的装置,而是利用一系列结合位点的可变、依赖变体的连接器。在低丰度下,H1 蛋白可能主要占据经典的单珠位点,维持基础的染色质组织。随着其活性或浓度上升,更多的连接模式被填充,使同一类蛋白能够桥接相邻的珠子、整条纤维,甚至分离的染色质液滴,推动更强的压缩。这一灵活的工具箱有助于解释不同 H1 变体如何调节基因活性、为何某些变体可作为肿瘤抑制因子,以及其丰度或修饰的细微变化如何重新组织局部染色质构象,从而在开放的富基因区与紧密封闭的沉默区域之间改变平衡。
引用: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
关键词: 染色质压缩, 连接组蛋白 H1, 核小体纤维, 基因组组织, 表观遗传调控