Clear Sky Science · ar
الهستونات الرابطية توحّد تلامسات ليف النوكليوزوم المتغايرة بربط نوكليوزومات متعددة
كيف يُعبَّأ الحمض النووي داخل خلايانا
كل خلية في جسمك تضغط ما يقرب من مترين من الحمض النووي داخل نواة أصغر بكثير من ذرة غبار. هذا التغليف الشديد ليس مجرد حيلة تخزينية؛ فهو يساعد في تحديد أي الجينات نشطة أو صامتة. يتعمق هذا الدراسة في أحد العناصر الأساسية التي غالباً ما تُهمل في هذا السياق، وهي الهستونات الرابطية، وتُظهر أنها تعمل أقل كدبابيس بسيطة على خرزات منفردة وأكثر كموصلات مرنة تربط العديد من الخرزات والألياف معاً.
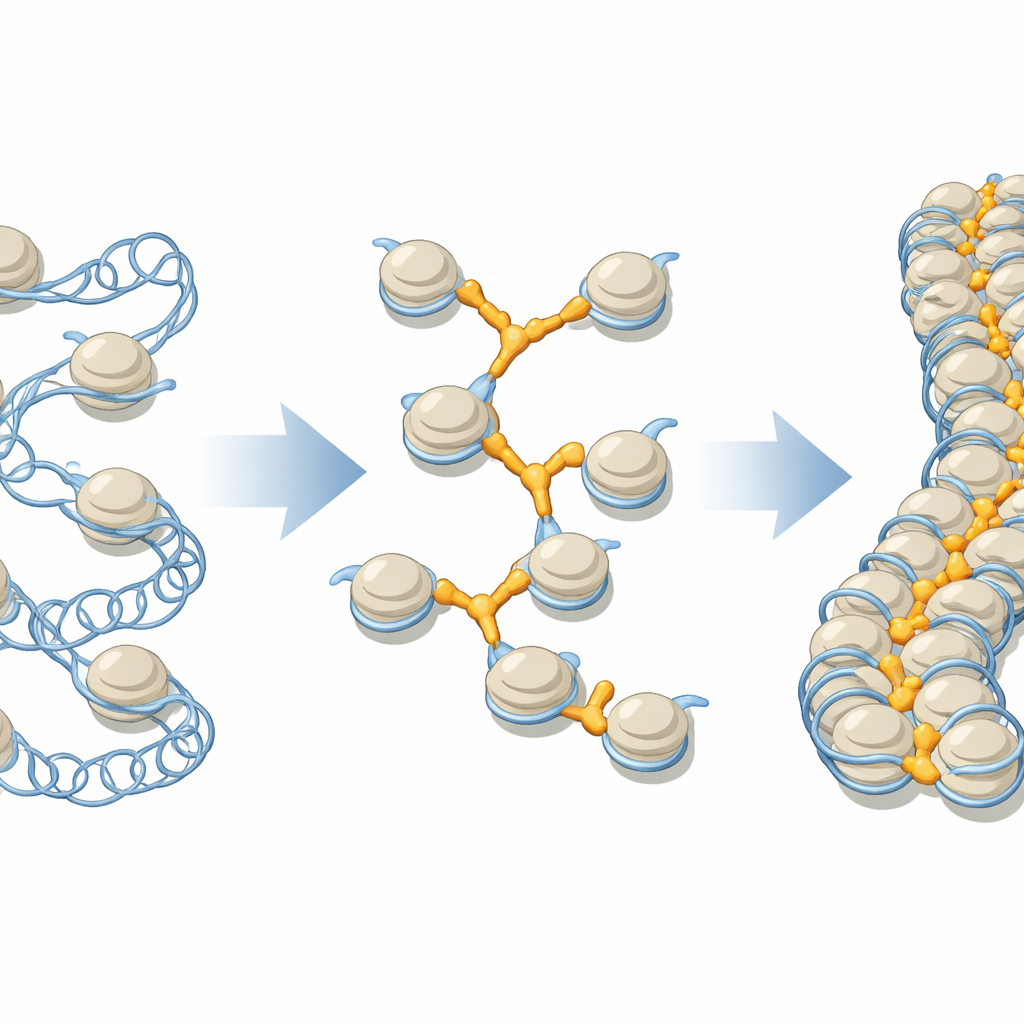
نظرة أقرب على خرزات الحمض النووي وموصلاتها
الحمض النووي في خلايانا يلتف حول نوى بروتينية لتشكيل وحدات تسمى نوكليوزومات، وغالبًا ما تُصوَّر كخرزات على خيط. ثم تطوى هذه الخرزات إلى ألياف ذات ترتيب أعلى قد تمتد لأكثر من مليون وحدة على طول كروموسوم واحد. اعتُقد منذ زمن طويل أن الهستونات الرابطية، وهي عائلة بروتينات تُعرف عامةً باسم H1، تجلس على كل خرزة بطريقة قياسية تساعد في إحكام البنية المحلية. لكن الخلايا تحتوي على عدة متغيرات مختلفة من H1، لكل منها مواقع مفضلة وأدوار خاصة، والأعمال الهيكلية السابقة ركزت في الغالب على خرزات معزولة، وليس على البيئة المكتظة والمضغوطة الموجودة في الكروموسومات الحقيقية.
هندسة ألياف نموذجية لكشف أوضاع الارتباط المخفية
لاستكشاف سلوك الهستونات الرابطية في بيئة كثيفة، هندس الباحثون نوكليوزومات تتصاق طبيعيًا معًا لتشكيل ألياف مستمرة. أمكن تبلور هذه الألياف المصممة وتحليلها بدقة قريبة من الذرية باستخدام حيود أشعة X. من خلال الجمع بين هذه الألياف ومختلف متغيرات الهستون الرابط، بما في ذلك H1.0 وH1x وH1.3 والبروتين الطيري H5، لاحظ الفريق ليس فقط الارتباط الكلاسيكي "في المركز" بخرزة مفردة، بل أيضًا ترتيبات بديلة متعددة حيث يتلامس هستون رابط واحد مع عدة نوكليوزومات في وقت واحد، أو حتى مع ألياف متعددة. وبفعْل ذلك وُجدت بروتينات H1 تحتل جيوبًا مملوءة بالحمض النووي تتشكل فقط عند تحزيم الخرزات معًا في ثلاثة أبعاد.
موصلات متعددة الاستخدامات تعيد تشكيل شكل الحمض النووي
كشفت هذه اللقطات الهيكلية أن الجزء المركزي المدمج من كل هستون رابط يتعرف على أشكال متكررة في الحمض النووي بدلاً من موقع ثابت واحد فقط. تتفاعل بقع سطحية معينة على البروتين مرارًا مع تجاويف واتساعات وانحناءات في اللولب المزدوج، سواء وجدت تلك السمات في مركز نوكليوزوم واحد أو عند وصلات خاصة بين عدة نوكليوزومات. بعض المتغيرات، مثل H1x وH1.0، يمكنها حتى أن تُحدث انثناءات صغيرة في الحمض النووي في نقاط محددة، مما يغير بشكل طفيف كيفية استلقائه على النواة البروتينية الأساسية. فضلت أنواع H1 المختلفة أنماط ارتباطية متنوعة: استخدم بعضها واجهة قوية واحدة في المقام الأول، بينما استخدم أخرى منطقتي تلامس قويّتين، مكوِّنة طيفًا من "طرائق الربط" التي تعتمد على كل من متغير البروتين والهندسة المحلية لليف.
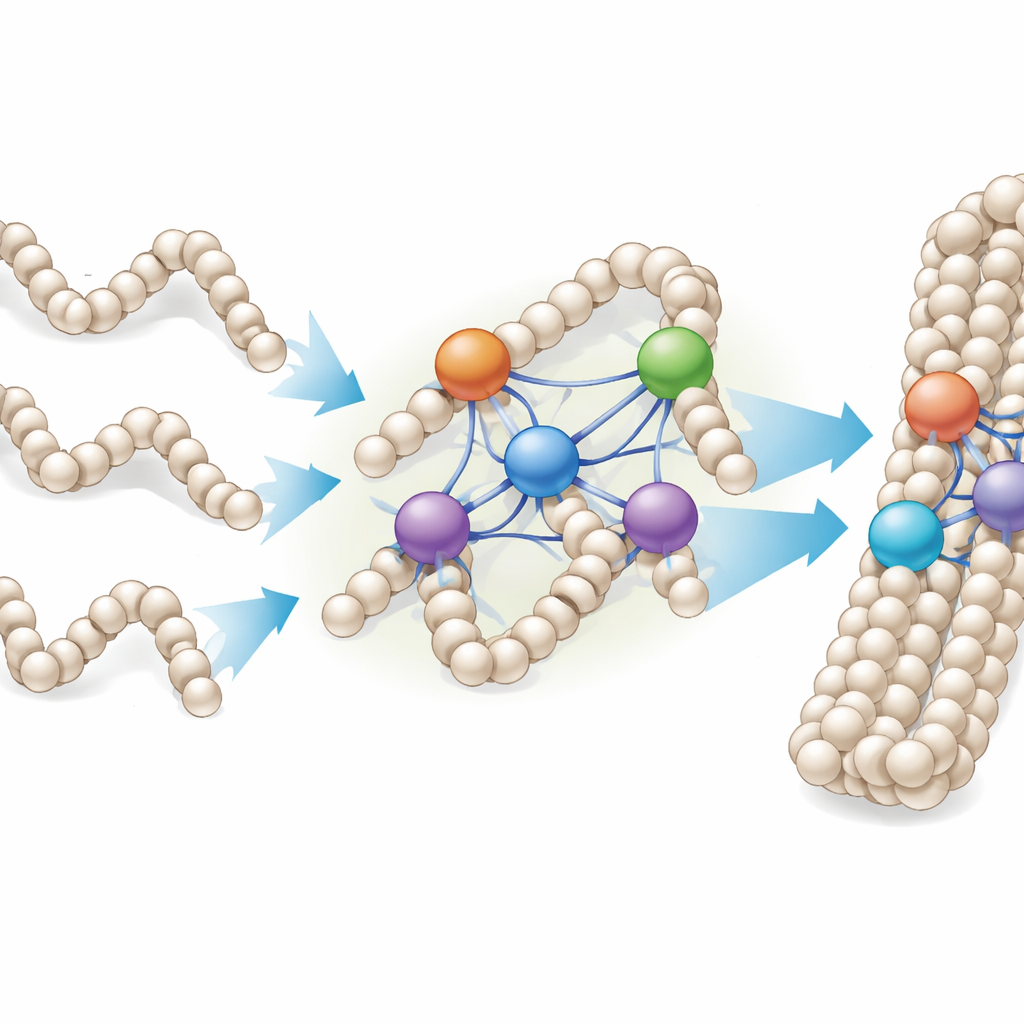
من ألياف مفردة إلى قطرات كثيفة من الكروماتين
نظرًا لأن الكروموسومات في الخلايا الحية تشبه قطرات كثيفة من الكروماتين أكثر من كونها أليافًا معزولة مرتبة، درس الباحثون أيضًا كيفية ارتباط الهستونات الرابطية بتكاثفات كروماتين مصنوعة مخبريًا—كتل من مجموعات متكررة من مصفوفات النوكليوزوم. وجدوا أن بروتينات H1 لم تتوقف عن الارتباط بعد الوصول إلى نسبة بسيطة واحد لواحد مع النوكليوزومات؛ بل إن النوكليوزومات الفردية كان يمكن أن ترتبط باثنين إلى أربعة أو أكثر من جزيئات H1، اعتمادًا على المتغير. وتحت المجهر، أدى إضافة المزيد من H1 إلى اندماج التكاثفات الكروية الصغيرة لتشكيل سلاسل أكبر تشبه الخرز، ما يشير إلى أن الهستونات الرابطية تستطيع خياطة قطرات وألياف كروماتين متعددة معًا لتكوين مجمّعات أكثر إحكامًا.
لماذا يهم هذا في التحكم الجيني والمرض
ترسم هذه النتائج صورة الهستونات الرابطية ليس كمشابك جامدة على خرزات مفردة، بل كموصلات قابلة للتكيف ومحددة حسب المتغير تستغل مجموعة من المخارج الارتباطية داخل كروماتين مكتظ. عند مستويات منخفضة، قد تحتل بروتينات H1 في الغالب المواقع الكلاسيكية على الخرزة الواحدة، مساعدةً في الحفاظ على التنظيم القاعدي للكروماتين. ومع ارتفاع نشاطها أو تركيزها، تزدحم أوضاع ربط إضافية، مما يمكّن نفس البروتينات من ردم المسافات بين الخرزات المجاورة والألياف الكاملة وحتى قطرات كروماتين منفصلة، دَافِعًا باتجاه تضاغط أقوى. تساعد هذه الأدوات المرنة على تفسير كيفية تعديل متغيرات H1 المختلفة لنشاط الجينات، ولماذا يعمل بعضها كعوامل مثبطة للأورام، وكيف أن تغييرات متواضعة في وفرتها أو في تعديلاتها قد تعيد تنظيم بنية الكروماتين المحلية، مغيرةً التوازن بين المناطق المفتوحة الغنية بالجينات والمجالات المضغوطة الصامتة.
الاستشهاد: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
الكلمات المفتاحية: تضاغط الكروماتين, الهستون الرابط H1, ليف النوكليوزوم, تنظيم الجينوم, التحكم فوق الجيني