Clear Sky Science · pl
Histony łącznikowe konsolidują heterogeniczne kontakty włókien nukleosomów przez łączenie wielu nukleosomów
Jak DNA jest upakowane w naszych komórkach
Każda komórka w twoim ciele upakowuje prawie dwa metry DNA w jądrze znacznie mniejszym niż pyłek kurzu. To ekstremalne upakowanie to nie tylko trik magazynowy; wpływa też na to, które geny są aktywne, a które wyciszone. W tym badaniu przyglądamy się jednemu z kluczowych, choć często pomijanych graczy w tym procesie — histonom łącznikowym — i pokazujemy, że funkcjonują one nie tyle jak proste klamry na pojedynczych „kulkach” DNA, ile jak wszechstronne łączniki spajające wiele kulek i włókien.
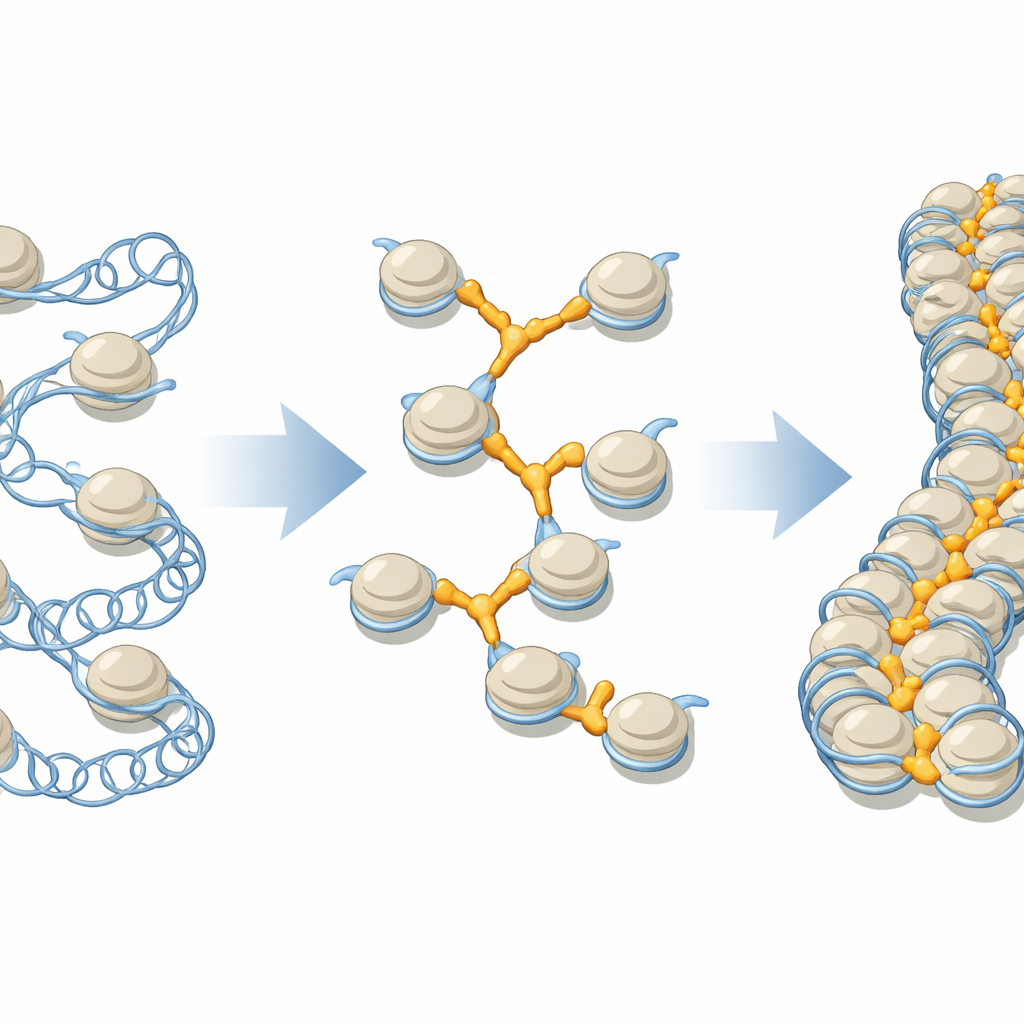
Bliższe spojrzenie na „kulki” DNA i ich łączniki
DNA w naszych komórkach owija się wokół rdzeni białkowych tworząc jednostki zwane nukleosomami, często przedstawiane jako kulki na sznurku. Te kulki składają się następnie w wyższe porządki włókien, które mogą obejmować ponad milion jednostek wzdłuż pojedynczego chromosomu. Histony łącznikowe, rodzina białek ogólnie oznaczana jako H1, od dawna uważano za osiadające na każdej kulce w standardowy sposób, pomagając lokalnie zaciskać strukturę. Tymczasem komórki zawierają kilka różnych wariantów H1, z odmiennymi preferencjami lokalizacyjnymi i rolami, a wcześniejsze prace strukturalne skupiały się głównie na izolowanych kulkach, nie na zatłoczonym, skondensowanym środowisku prawdziwych chromosomów.
Projektowanie modelowych włókien ujawnia ukryte tryby wiązania
Aby zbadać zachowanie histonów łącznikowych w gęstym otoczeniu, badacze skonstruowali nukleosomy, które naturalnie łączały się w ciągłe włókna. Takie zaprojektowane włókna można było skrystalizować i przeanalizować w niemal atomowej rozdzielczości przy użyciu krystalografii rentgenowskiej. Łącząc te włókna z różnymi wariantami histonów łącznikowych, w tym H1.0, H1x, H1.3 i białkiem ptasim H5, zespół zaobserwował nie tylko klasyczne „na środku” wiązanie do pojedynczej kulki, lecz także wiele alternatywnych układów, w których jeden histon łącznikowy kontaktował się jednocześnie z kilkoma nukleosomami, a nawet z wieloma włóknami. Innymi słowy, białka H1 zajmowały miejsca wypełnione DNA, które powstawały dopiero wtedy, gdy kulki pakowały się razem w trzech wymiarach.
Wszechstronne łączniki, które przeobrażają kształt DNA
Te strukturalne migawki ujawniły, że skompaktowana centralna część każdego histonu łącznikowego rozpoznaje powtarzające się kształty DNA, a nie tylko jedno sztywne miejsce. Pewne fragmenty powierzchni białka wielokrotnie oddziałują z poszerzonymi rowkami i zagięciami podwójnej helisy — niezależnie od tego, czy te cechy znajdują się w centrum jednego nukleosomu, czy w specjalnych złączach między kilkoma nukleosomami. Niektóre warianty, takie jak H1x i H1.0, potrafią nawet wygiąć DNA w określonych punktach, subtelnie zmieniając jego ułożenie względem rdzenia białkowego. Różne typy H1 faworyzowały różne schematy wiązania: jedne wykorzystywały głównie pojedynczy silny interfejs, inne używały dwóch intensywnych regionów kontaktu, tworząc spektrum „trybów łączenia” zależnych zarówno od wariantu białka, jak i lokalnej geometrii włókna.
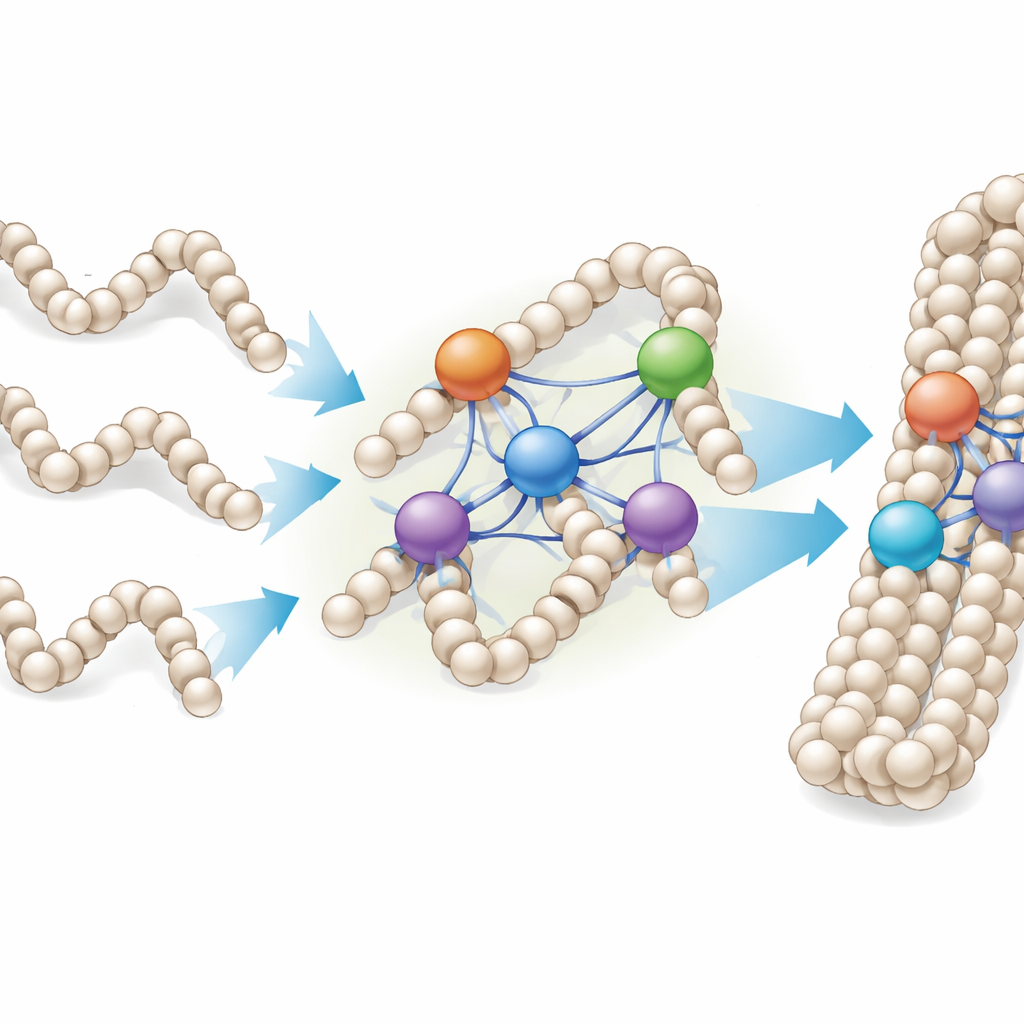
Od pojedynczych włókien po gęste krople chromatyny
Ponieważ chromosomy w żywych komórkach przypominają raczej gęste krople chromatyny niż uporządkowane, izolowane włókna, badacze sprawdzili także, jak histony łącznikowe wiążą się z laboratoryjnie przygotowanymi kondensatami chromatyny — skupiskami wielu powtarzających się arrayów nukleosomowych. Odkryli, że białka H1 nie przestawały wiązać się po osiągnięciu prostego stosunku jeden do jednego z nukleosomami; zamiast tego pojedyncze nukleosomy mogły być związane z dwoma, czterema lub nawet większą liczbą cząsteczek H1, w zależności od wariantu. Pod mikroskopem dodanie większej ilości H1 powodowało zlewanie się małych, kulistych kondensatów w większe, przypominające paciorki łańcuchy, co wskazuje, że histony łącznikowe mogą zszywać wiele kropli chromatyny i włókien w bardziej zwarte zespoły.
Dlaczego to ma znaczenie dla kontroli genów i chorób
Wyniki te przedstawiają histony łącznikowe nie jako sztywne zaciski na pojedynczych kulkach, lecz jako adaptacyjne, specyficzne dla wariantów łączniki, które wykorzystują różnorodne nisze wiązania w zatłoczonej chromatynie. Przy niskich poziomach białka H1 mogą głównie zajmować klasyczne pozycje na pojedynczych kulkach, pomagając utrzymać podstawową organizację chromatyny. Wraz ze wzrostem ich aktywności lub stężenia pojawiają się dodatkowe tryby łączenia, pozwalające tym samym białkom mostkować sąsiednie kulki, całe włókna, a nawet oddzielne krople chromatyny, napędzając silniejsze zagęszczenie. To elastyczne „narzędzie” pomaga wyjaśnić, jak różne warianty H1 mogą dostrajać aktywność genów, dlaczego niektóre z nich działają jako supresory nowotworów oraz jak skromne zmiany w ich obfitości lub modyfikacjach mogą przeorganizować lokalną architekturę chromatyny, przechylając równowagę między otwartymi, bogatymi w geny regionami a ściśle upakowanymi, cichymi domenami.
Cytowanie: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
Słowa kluczowe: zagęszczanie chromatyny, histon łącznikowy H1, włókno nukleosomowe, organizacja genomu, regulacja epigenetyczna