Clear Sky Science · de
Linker-Histon-Proteine konsolidieren heterogene Nukleosomenfaserkontakte, indem sie mehrere Nukleosomen verbinden
Wie DNA in unseren Zellen verpackt wird
Jede Zelle Ihres Körpers quetscht fast zwei Meter DNA in einen Zellkern, der weit kleiner ist als ein Staubkorn. Diese extreme Packung ist nicht nur ein Aufbewahrungstrick; sie beeinflusst mit, welche Gene aktiv oder stillgelegt sind. Diese Studie untersucht einen der zentralen, oft übersehenen Akteure in diesem Prozess, die Linker-Histon-Proteine, und zeigt, dass sie weniger wie einfache Klammern an einzelnen DNA‑Perlen wirken, sondern vielmehr als vielseitige Verbinder, die viele Perlen und Fasern zusammenbinden.
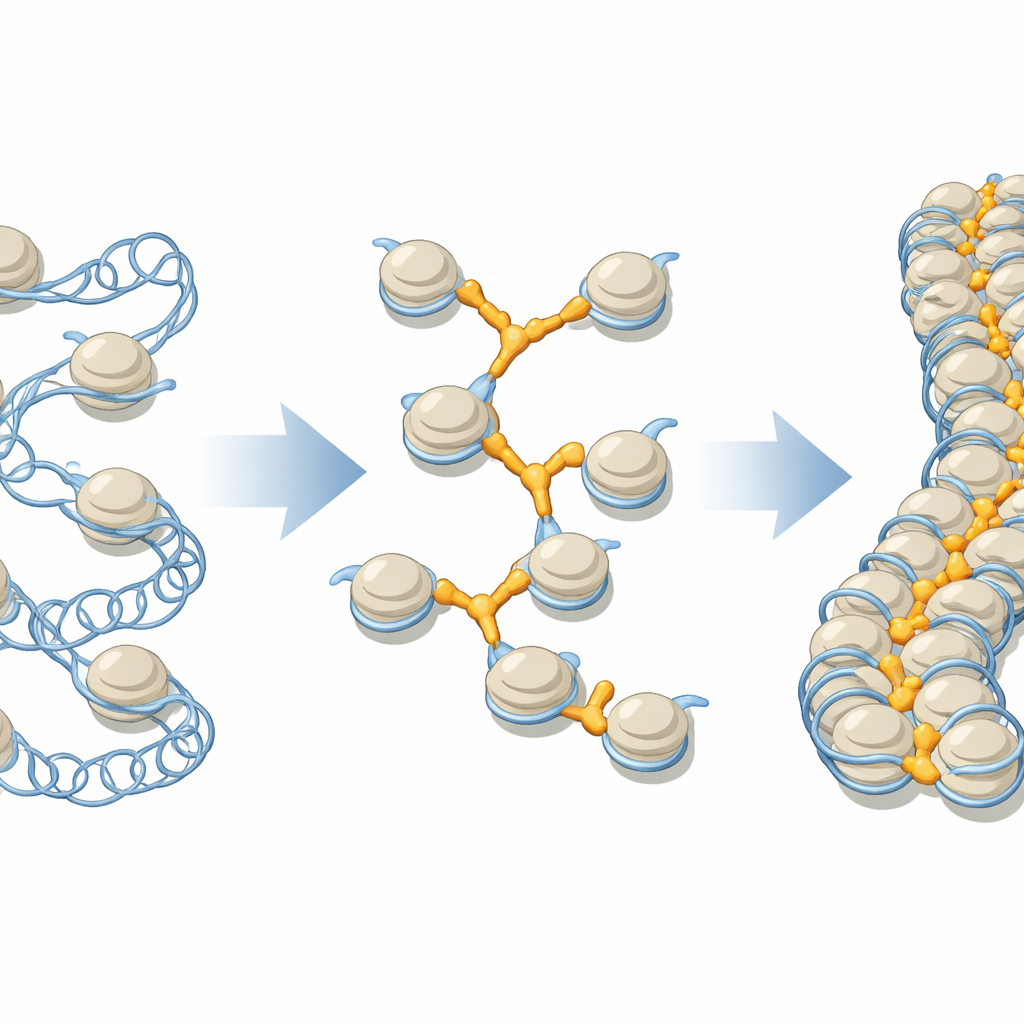
Ein genauerer Blick auf die DNA‑Perlen und ihre Verbinder
In unseren Zellen ist DNA um Proteinkerne gewickelt und bildet Einheiten, die Nukleosomen genannt werden und oft als Perlen auf einer Schnur dargestellt werden. Diese Perlen falten sich dann zu höher geordneten Fasern, die sich entlang eines Chromosoms auf über eine Million Einheiten erstrecken können. Linker-Histone, eine Proteinfamilie, die allgemein als H1 bezeichnet wird, galten lange als auf jeder Perle standardmäßig sitzend und helfen, die lokale Struktur zu verdichten. Aber Zellen enthalten mehrere unterschiedliche H1‑Varianten, jede mit ihren bevorzugten Orten und Funktionen, und frühere Strukturarbeiten konzentrierten sich meist auf isolierte Perlen statt auf die dicht gepackte Umgebung, wie sie in echten Chromosomen vorkommt.
Modellfasern entwerfen, um verborgene Bindungsmodi aufzudecken
Um zu erforschen, wie Linker-Histone sich in dichter Umgebung verhalten, konstruierten die Forschenden Nukleosomen, die sich von selbst zu durchgehenden Fasern zusammenfügen. Diese designer‑Fasern ließen sich kristallisieren und mit Röntgenkristallographie nahezu auf Atomniveau analysieren. Kombiniert mit verschiedenen Linker‑Histon‑Varianten, darunter H1.0, H1x, H1.3 und das Vogelprotein H5, beobachtete das Team nicht nur die klassische „Zentrum‑auf“-Bindung an eine einzelne Perle, sondern mehrere alternative Anordnungen, in denen ein Linker‑Histon mehrere Nukleosomen gleichzeitig oder sogar mehrere Fasern kontaktierte. Effektiv besetzten H1‑Proteine DNA‑gefüllte Taschen, die nur entstehen, wenn Perlen sich dreidimensional zusammenpacken.
Vielseitige Verbinder, die die DNA‑Form umgestalten
Diese strukturellen Momentaufnahmen zeigten, dass der kompakte zentrale Teil jedes Linker‑Histons wiederkehrende DNA‑Formen erkennt, statt nur eine einzige feste Stelle. Bestimmte Oberflächenbereiche des Proteins greifen wiederholt verbreiterte Rillen und Biegungen der Doppelhelix an, egal ob diese Merkmale im Zentrum eines Nukleosoms oder an speziellen Verbindungsstellen zwischen mehreren Nukleosomen liegen. Manche Varianten, etwa H1x und H1.0, können die DNA an bestimmten Stellen sogar knicken und damit subtil ändern, wie sie auf dem darunterliegenden Proteinkern liegt. Verschiedene H1‑Typen bevorzugten unterschiedliche Bindungsmuster: einige nutzten vorwiegend eine einzige starke Schnittstelle, andere verwendeten zwei robuste Kontaktregionen und erzeugten so ein Spektrum an „Verknüpfungsmodi“, das sowohl von der Proteinvariante als auch von der lokalen Fasergeometrie abhängt.
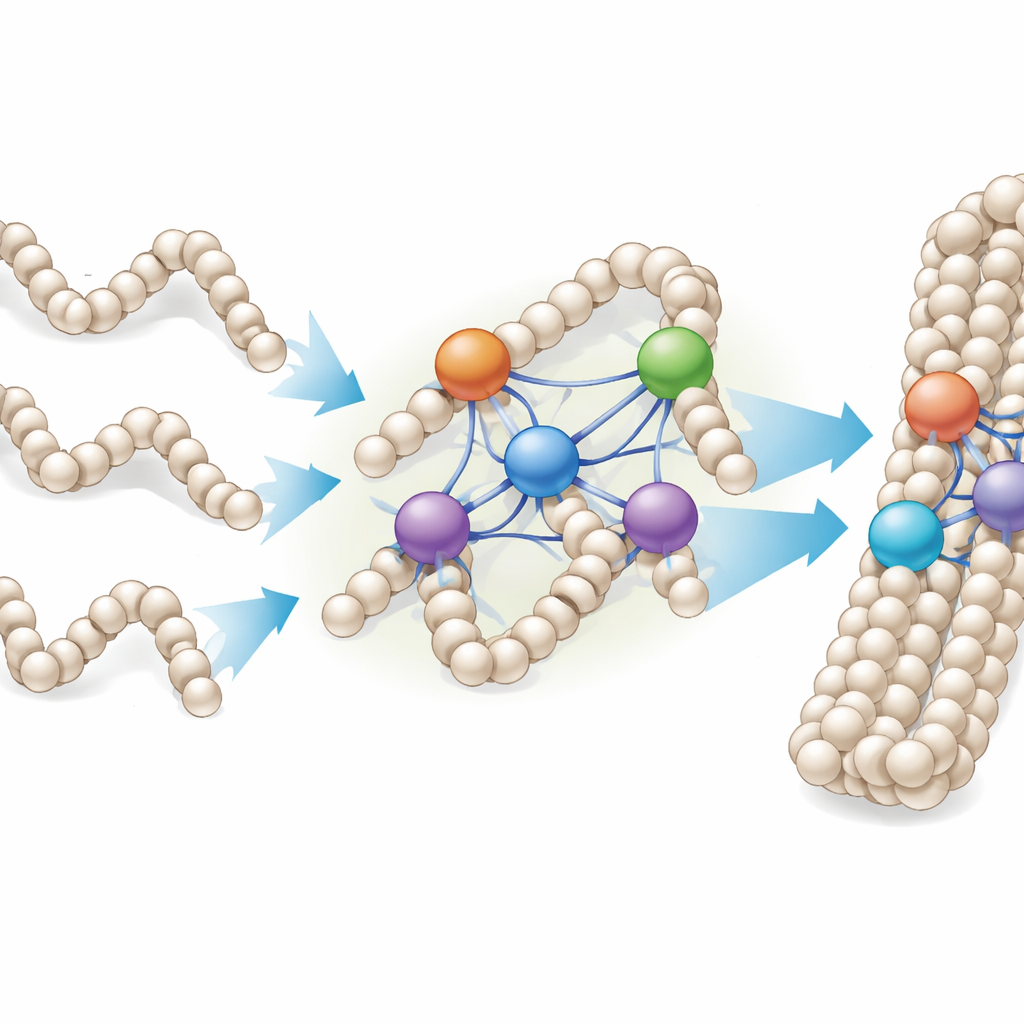
Von einzelnen Fasern zu dichten Chromatin‑Tröpfchen
Da Chromosomen in lebenden Zellen eher dichten Chromatin‑Tröpfchen als ordentlichen, isolierten Fasern gleichen, untersuchten die Forschenden auch, wie Linker‑Histone an im Labor hergestellte Chromatin‑Kondensate binden—Ansammlungen vieler wiederholter Nukleosomen‑Arrays. Sie fanden, dass H1‑Proteine nicht aufhörten zu binden, nachdem ein einfaches Eins‑zu‑Eins‑Verhältnis zu den Nukleosomen erreicht war; stattdessen konnten einzelne Nukleosomen je nach Variante mit zwei bis vier oder mehr H1‑Molekülen assoziiert sein. Unter dem Mikroskop führte die Zugabe von mehr H1 dazu, dass kleine, kugelförmige Kondensate zu größeren, perlenartigen Ketten verschmolzen, was darauf hinweist, dass Linker‑Histone mehrere Chromatin‑Tröpfchen und Fasern zu dichteren Assemblierungen zusammennähen können.
Warum das für Genregulation und Krankheit wichtig ist
Diese Ergebnisse zeichnen Linker‑Histone nicht als starre Klammern an einzelnen Perlen, sondern als anpassungsfähige, variantenspezifische Verbinder, die eine Reihe von Bindungsnischen im dicht gepackten Chromatin ausnutzen. Bei niedrigen Mengen besetzen H1‑Proteine vermutlich überwiegend die klassischen Einzelperlen‑Positionen und helfen, die grundlegende Chromatinorganisation aufrechtzuerhalten. Mit zunehmender Aktivität oder Konzentration werden zusätzliche Verknüpfungsmodi besetzt, wodurch dieselben Proteine benachbarte Perlen, ganze Fasern und sogar separate Chromatin‑Tröpfchen überbrücken und so stärkere Verdichtung antreiben können. Dieses flexible Werkzeugset erklärt, wie verschiedene H1‑Varianten die Genaktivität feinabstimmen, warum einige als Tumorsuppressoren fungieren und wie moderate Änderungen in ihrer Menge oder Modifikation die lokale Chromatinarchitektur umorganisieren und das Gleichgewicht zwischen offenen, genreichen Regionen und dicht gepackten, stillen Domänen verschieben können.
Zitation: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
Schlüsselwörter: Chromatinverdichtung, Linker-Histon H1, Nukleosomenfaser, Genomorganisation, epigenetische Regulation