Clear Sky Science · sv
Linkerhistoner konsoliderar heterogena kontakter i nukleosomfibrer genom att länka samman flera nukleosomer
Hur DNA packas inuti våra celler
Varje cell i din kropp trycker in nästan två meter DNA i en kärna som är mycket mindre än ett dammkorn. Denna extrema packning är inte bara ett lagringstrick; den hjälper också till att bestämma vilka gener som är aktiva eller tysta. Denna studie gräver i en av de nyckelspelare som ofta förbises i denna process, linkerhistonerna, och visar att de beter sig mindre som enkla klämmor på individuella DNA-pärlor och mer som mångsidiga förbindare som knyter samman många pärlor och fibrer.
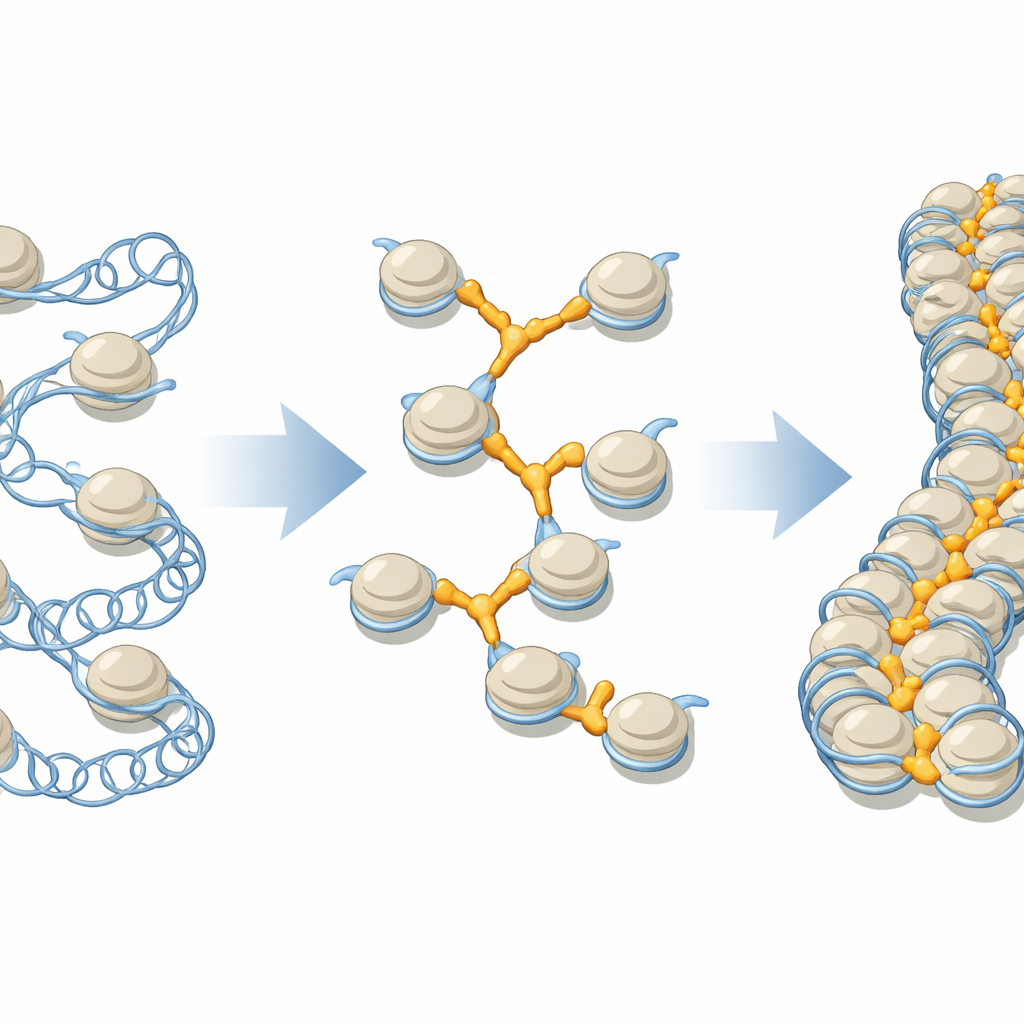
En närmare titt på DNA-pärlorna och deras förbindelser
DNA i våra celler är lindat runt proteinkärnor och bildar enheter som kallas nukleosomer, ofta avbildade som pärlor på en sträng. Dessa pärlor veckas sedan in i högre ordningens fibrer som kan sträcka sig över mer än en miljon enheter längs en enda kromosom. Linkerhistoner, en proteinfamilj som ofta betecknas H1, har länge antagits sitta på varje pärla på ett standardiserat sätt och hjälpa till att dra ihop den lokala strukturen. Men celler innehåller flera olika H1-varianter, var och en med sina föredragna platser och roller, och tidigare strukturarbeten fokuserade mest på isolerade pärlor, inte den trånga, kompakterade miljö som finns i verkliga kromosomer.
Konstruera modelfibrer för att avslöja dolda bindningssätt
För att utforska hur linkerhistoner beter sig i en tät miljö konstruerade forskarna nukleosomer som naturligt klickar ihop sig till kontinuerliga fibrer. Dessa designade fibrer kunde kristalliseras och analyseras med nästan atomupplösning med röntgenkristallografi. Genom att kombinera dessa fibrer med olika linkerhistonvarianter, inklusive H1.0, H1x, H1.3 och fågelproteinet H5, observerade teamet inte bara den klassiska ”mitt-på” bindningen till en enda pärla utan flera alternativa arrangemang där en linkerhiston kontaktade flera nukleosomer samtidigt, eller till och med flera fibrer. I praktiken fann man att H1-proteiner upptog DNA-fyllda fickor som bara bildas när pärlor packar ihop sig i tre dimensioner.
Mångsidiga förbindare som omformar DNA:s form
Dessa strukturella ögonblicksbilder visade att den kompakta centrala delen av varje linkerhiston känner igen återkommande DNA-former snarare än en enda fast plats. Vissa ytområden på proteinet engagerar upprepade gånger utvidgade spår och böjar i dubbelspiralen, oavsett om dessa kännetecken finns i mitten av en nukleosom eller vid särskilda korsningar mellan flera nukleosomer. Vissa varianter, såsom H1x och H1.0, kan till och med vika DNA:t i specifika punkter och subtilt flytta hur det ligger på den underliggande proteinkärnan. Olika H1-typer gynnade olika bindningsmönster: vissa använde främst ett enda starkt gränssnitt, medan andra använde två robusta kontaktområden, vilket skapade ett spektrum av ”länkningslägen” som beror både på proteinvarianten och den lokala fiberns geometri.
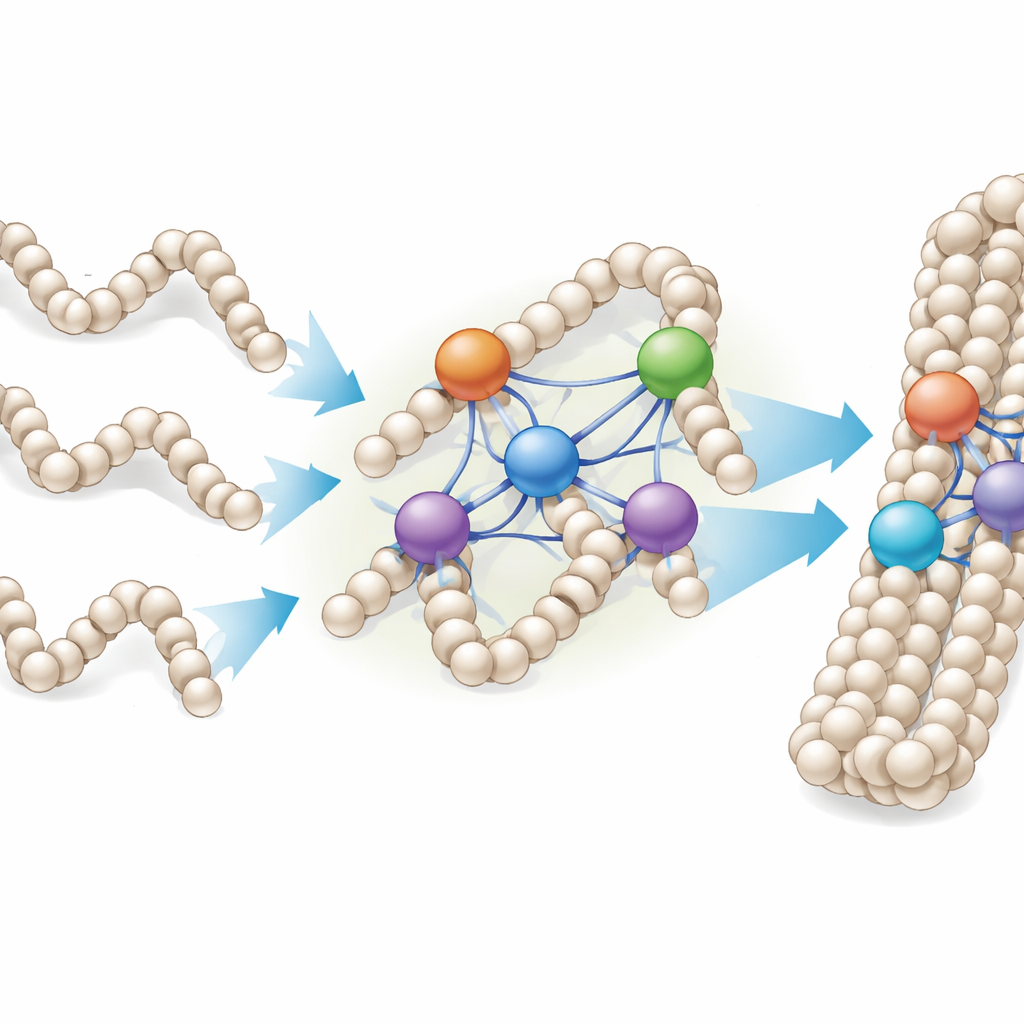
Från enskilda fibrer till täta kromatindroppar
Eftersom kromosomer i levande celler liknar täta droppar av kromatin snarare än prydliga, isolerade fibrer, studerade forskarna också hur linkerhistoner binder till laboratorietillverkade kromatinkondensat—klumpar av många upprepade nukleosomarrayer. De fann att H1-proteiner inte slutade binda efter att ha uppnått ett enkelt ett-till-ett-förhållande med nukleosomerna; istället kunde enskilda nukleosomer associeras med två till fyra eller fler H1-molekyler, beroende på variant. Under mikroskopet orsakade tillsats av mer H1 att små, sfäriska kondensat smälte samman till större, pärliknande kedjor, vilket indikerar att linkerhistoner kan sy ihop flera kromatindroppar och fibrer till mer kompakta sammanställningar.
Varför detta är viktigt för genreglering och sjukdom
Dessa resultat beskriver linkerhistoner inte som styva klämmor på enstaka pärlor, utan som anpassningsbara, variant-specifika förbindare som utnyttjar ett spektrum av bindningsnischer inom trångt kromatin. Vid låga nivåer kan H1-proteiner mestadels inta de klassiska en-pärla-positionerna och bidra till att upprätthålla grundläggande kromatinorganisation. När deras aktivitet eller koncentration ökar, fylls ytterligare länkningslägen, vilket gör det möjligt för samma proteiner att överbrygga intilliggande pärlor, hela fibrer och till och med separata kromatindroppar och därigenom driva starkare kompaktering. Detta flexibla verktyg förklarar hur olika H1-varianter kan finjustera genaktivitet, varför vissa fungerar som tumörsuppressorer, och hur måttliga förändringar i deras mängd eller modifiering kan omorganisera lokal kromatinarkitektur och rubba balansen mellan öppna, genrika regioner och tätt packade, tysta domäner.
Citering: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
Nyckelord: kromatinkompaktering, linkerhiston H1, nukleosomfibrer, genomorganisation, epigenetisk reglering