Clear Sky Science · fr
Les histones de liaison consolident des contacts hétérogènes entre fibres de nucléosomes en reliant plusieurs nucléosomes
Comment l’ADN est emballé dans nos cellules
Chaque cellule de votre corps parvient à comprimer près de deux mètres d’ADN dans un noyau bien plus petit qu’un grain de poussière. Cet empilement extrême n’est pas qu’un tour de stockage ; il contribue à déterminer quels gènes sont actifs ou silencieux. Cette étude examine l’un des acteurs clés mais souvent négligés de ce processus, les histones de liaison, et montre qu’ils fonctionnent moins comme de simples agrafes sur des perles isolées d’ADN que comme des connecteurs polyvalents qui relient de nombreuses perles et fibres entre elles.
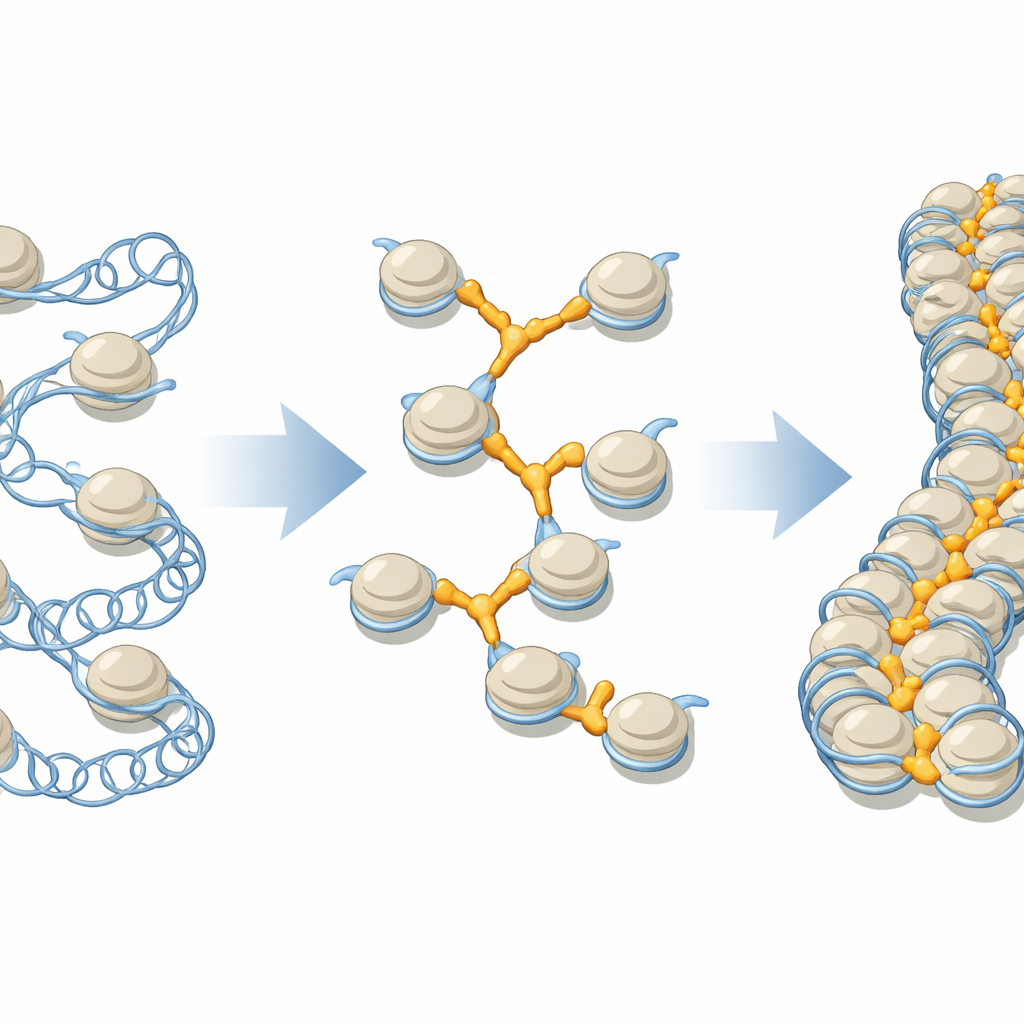
Un regard plus précis sur les perles d’ADN et leurs connecteurs
L’ADN dans nos cellules s’enroule autour de cœurs protéiques pour former des unités appelées nucléosomes, souvent représentées comme des perles sur une ficelle. Ces perles se replient ensuite en fibres de niveau supérieur qui peuvent dépasser un million d’unités le long d’un même chromosome. Les histones de liaison, une famille de protéines généralement désignée H1, ont longtemps été considérées comme se positionnant sur chaque perle de manière standard pour resserrer la structure locale. Mais les cellules contiennent plusieurs variants de H1, chacun avec ses localisations et rôles préférentiels, et les travaux structuraux antérieurs se sont surtout concentrés sur des perles isolées, pas sur l’environnement dense et compact des vrais chromosomes.
Conception de fibres modèles pour révéler des modes de liaison cachés
Pour explorer le comportement des histones de liaison dans un contexte dense, les chercheurs ont conçu des nucléosomes qui s’assemblent naturellement en fibres continues. Ces fibres artificielles ont pu être cristallisées et analysées à une résolution quasi atomique par cristallographie aux rayons X. En combinant ces fibres avec différents variants d’histones de liaison, dont H1.0, H1x, H1.3 et la protéine aviaire H5, l’équipe n’a pas observé seulement le classique lien « au centre » à une seule perle, mais plusieurs arrangements alternatifs dans lesquels une histone de liaison touchait plusieurs nucléosomes à la fois, voire plusieurs fibres. En pratique, les protéines H1 occupaient des poches remplies d’ADN formées uniquement lorsque les perles s’emboîtaient en trois dimensions.
Connecteurs polyvalents qui remodelent la conformation de l’ADN
Ces instantanés structuraux ont montré que la portion centrale compacte de chaque histone de liaison reconnaît des formes d’ADN récurrentes plutôt qu’un site unique et fixe. Certains patchs de surface de la protéine s’engagent de façon répétée avec des sillons élargis et des courbures de la double hélice, que ces traits se trouvent au centre d’un nucléosome ou à des jonctions particulières entre plusieurs nucléosomes. Certains variants, comme H1x et H1.0, peuvent même provoquer un angle dans l’ADN à des endroits spécifiques, modifiant subtilement sa position sur le cœur protéique sous-jacent. Les différents types de H1 privilégient des schémas de liaison distincts : certains utilisent principalement une interface unique et forte, tandis que d’autres mobilisent deux régions de contact robustes, créant un spectre de « modes de liaison » dépendant à la fois du variant protéique et de la géométrie locale de la fibre.
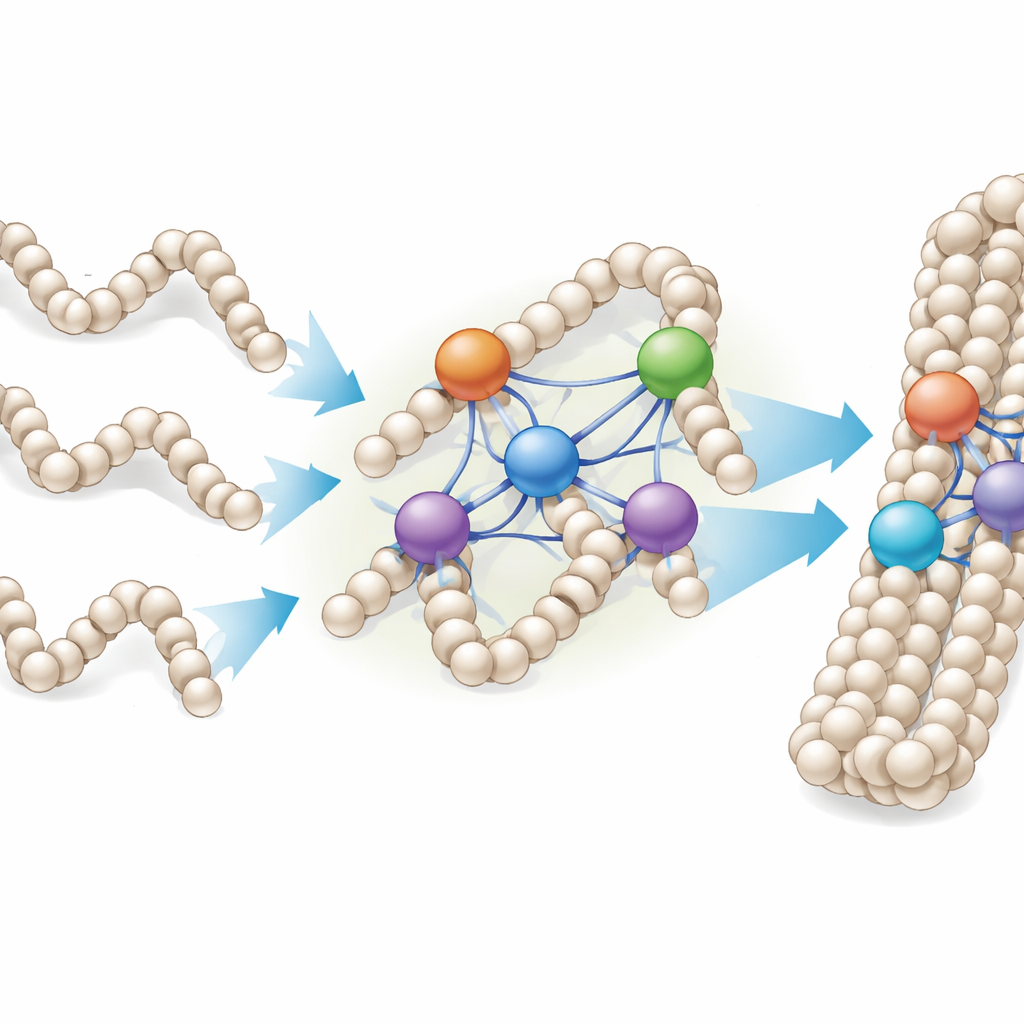
Des fibres isolées aux gouttelettes denses de chromatine
Comme les chromosomes dans les cellules vivantes ressemblent davantage à des gouttelettes denses de chromatine qu’à des fibres propres et isolées, les chercheurs ont également étudié comment les histones de liaison se fixent à des condensats de chromatine fabriqués en laboratoire — des amas de nombreux réseaux répétés de nucléosomes. Ils ont constaté que les protéines H1 ne cessaient pas de se lier après avoir atteint un simple rapport un pour un avec les nucléosomes ; au contraire, un nucléosome individuel pouvait être associé à deux, quatre H1 ou plus, selon le variant. Au microscope, l’ajout de H1 provoquait la fusion de petits condensats sphériques en chaînes plus grandes, en forme de perles, indiquant que les histones de liaison peuvent coudre ensemble plusieurs gouttelettes et fibres de chromatine pour former des assemblages plus compacts.
Pourquoi cela compte pour le contrôle des gènes et la maladie
Ces résultats présentent les histones de liaison non comme des pinces rigides sur des perles isolées, mais comme des connecteurs adaptables et spécifiques aux variants qui exploitent une gamme de niches de liaison au sein d’une chromatine encombrée. À faibles niveaux, les protéines H1 peuvent principalement occuper les positions classiques sur une seule perle, contribuant au maintien d’une organisation chromatinienne de base. À mesure que leur activité ou leur concentration augmente, des modes de liaison supplémentaires se mettent en place, permettant aux mêmes protéines de relier des perles voisines, des fibres entières et même des gouttelettes chromatiniennes séparées, favorisant une compaction plus forte. Cette boîte à outils flexible explique comment différents variants de H1 peuvent moduler l’activité des gènes, pourquoi certains jouent un rôle de suppresseurs de tumeurs, et comment des changements modestes dans leur abondance ou leur modification peuvent réorganiser l’architecture chromatinienne locale, faisant basculer l’équilibre entre régions ouvertes riches en gènes et domaines serrés et silencieux.
Citation: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
Mots-clés: compaction de la chromatine, histone de liaison H1, fibre de nucléosomes, organisation du génome, régulation épigénétique