Clear Sky Science · ru
Связывающие гистоны консолидируют гетерогенные контакты нуклеосомного волокна, объединяя несколько нуклеосом
Как ДНК упакована внутри наших клеток
Каждая клетка вашего тела помещает почти два метра ДНК в ядро, размером гораздо меньше пылинки. Такая крайняя упаковка — не просто способ хранения; она помогает определять, какие гены активны, а какие отключены. В этом исследовании рассматривается один из ключевых, но часто недооценённых участников процесса — связывающие гистоны — и показано, что они действуют не как простые прищепки на отдельных бусинах ДНК, а скорее как универсальные соединители, связывающие сразу множество бусин и волокон.
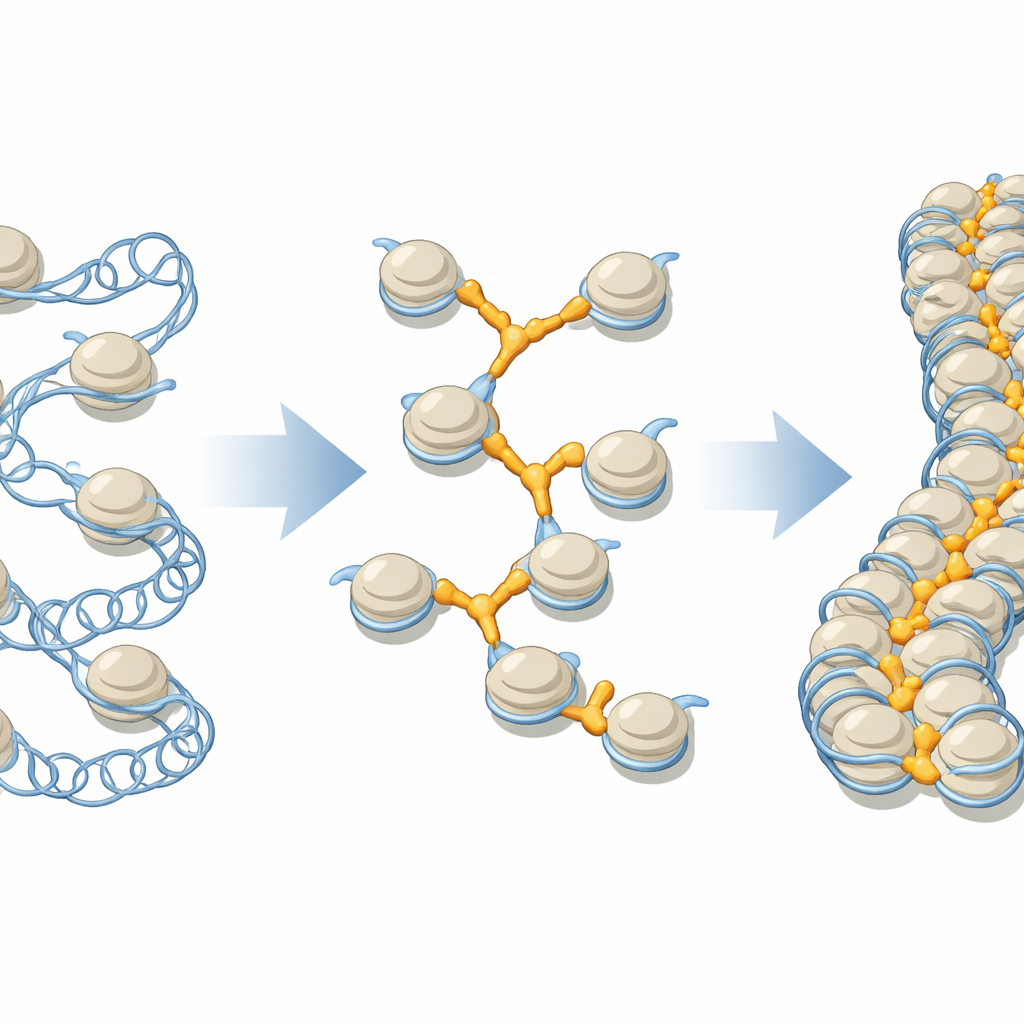
Ближе к «бусинам» ДНК и их соединителям
ДНК в наших клетках обвита вокруг белковых ядер, образуя единицы, называемые нуклеосомами, которые часто изображают как бусины на нитке. Эти бусины затем складываются в волокна более высокого порядка, которые вдоль одной хромосомы могут насчитывать свыше миллиона единиц. Связывающие гистоны, семейство белков, обычно объединяемое под обозначением H1, долгое время считали сидящими на каждой бусине по единой схеме и помогающими уплотнить локальную структуру. Но в клетке присутствуют несколько различных вариантов H1, у каждого — свои предпочтительные местоположения и функции, а ранние структурные исследования в основном фокусировались на изолированных бусинах, а не на тугой, плотной среде настоящих хромосом.
Создание модельных волокон для выявления скрытых режимов связывания
Чтобы выяснить, как связывающие гистоны ведут себя в плотной среде, исследователи сконструировали нуклеосомы, которые естественно сцепляются в непрерывные волокна. Эти модельные волокна удалось кристаллизовать и изучить с почти атомным разрешением методом рентгеновской кристаллографии. Комбинируя волокна с разными вариантами связывающих гистонов, включая H1.0, H1x, H1.3 и птиночный белок H5, команда наблюдала не только классическое «центральное» связывание с одной бусиной, но и множественные альтернативные расположения, при которых один связывающий гистон контактировал сразу несколько нуклеосом или даже несколько волокон. Проще говоря, белки H1 занимали заполненные ДНК-ом карманы, которые образуются только тогда, когда бусины упаковываются вместе в трёх измерениях.
Универсальные соединители, перестраивающие форму ДНК
Эти структурные «моментальные снимки» показали, что компактная центральная часть каждого связывающего гистона распознаёт повторяющиеся формы ДНК, а не только одно фиксированное место. Некоторые участки поверхности белка многократно взаимодействуют с расширенными бороздами и изгибами двойной спирали, независимо от того, находятся ли такие особенности в центре одной нуклеосомы или в особых стыках между несколькими нуклеосомами. Некоторые варианты, например H1x и H1.0, способны даже изламывать (вызывать сгиб) ДНК в определённых точках, тонко меняя её положение на белковом ядре. Различные типы H1 предпочитали разные схемы связывания: одни в основном использовали один сильный интерфейс, другие — два прочных контакта, создавая спектр «режимов связывания», который зависит как от варианта белка, так и от локальной геометрии волокна.
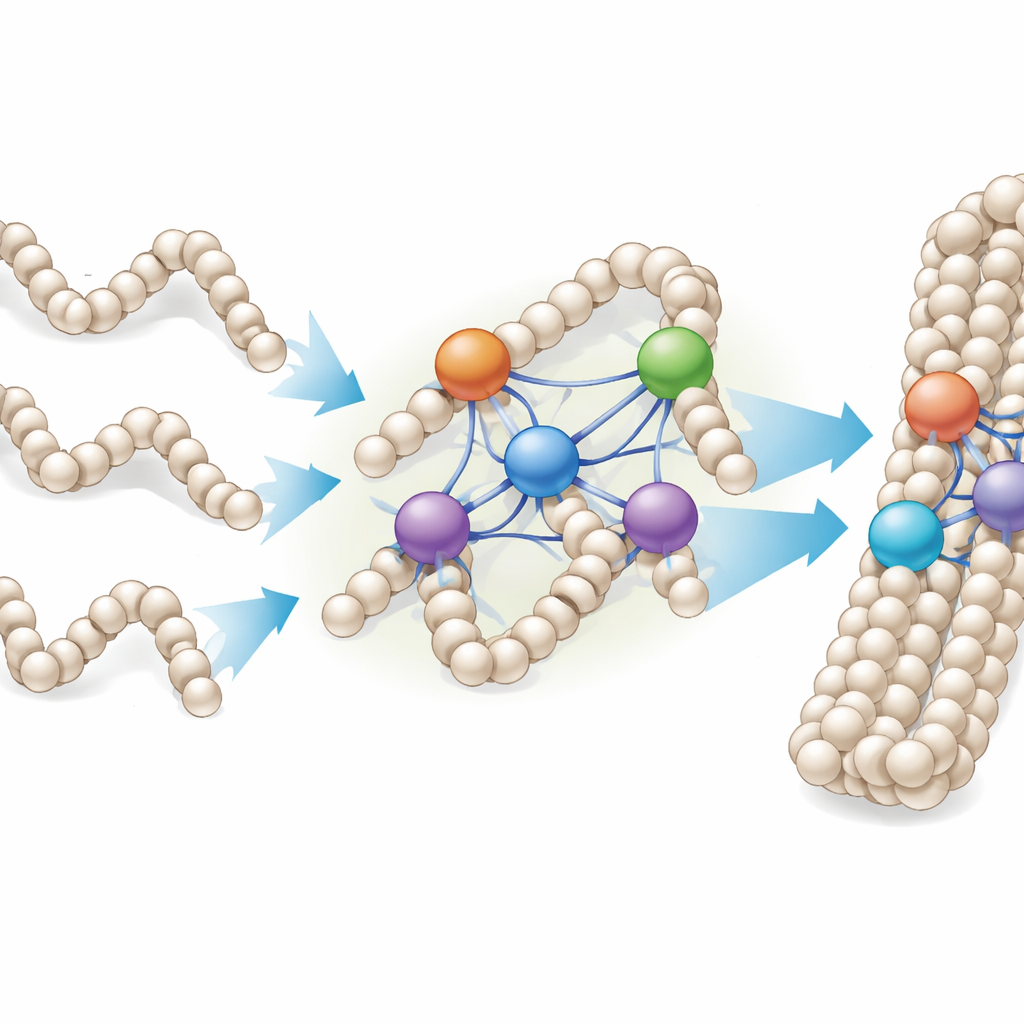
От одиночных волокон до плотных конденсатов хроматина
Поскольку хромосомы в живых клетках скорее напоминают плотные капли хроматина, чем аккуратные изолированные волокна, исследователи также изучали, как связывающие гистоны взаимодействуют с лабораторно собранными конденсатами хроматина — сгустками многих повторяющихся массивов нуклеосом. Они обнаружили, что белки H1 не прекращали связываться после достижения простого соотношения один к одному с нуклеосомами; напротив, отдельные нуклеосомы могли ассоциироваться с двумя, четырьмя и более молекулами H1, в зависимости от варианта. Под микроскопом добавление большего количества H1 вызывало слияние небольших сферических конденсатов в более крупные цепочки в виде бусин, что указывает на то, что связывающие гистоны способны сшивать вместе несколько хроматиновых капель и волокон в более компактные образования.
Почему это важно для регуляции генов и болезней
Эти результаты рисуют образ связывающих гистонов не как жёстких зажимов на отдельных бусинах, а как адаптивных, специфичных для вариантов соединителей, которые используют множество ниш связывания в плотно упакованном хроматине. При низкой концентрации H1 белки, вероятно, в основном занимают классические позиции на отдельных бусинах, помогая поддерживать базовую организацию хроматина. По мере роста их активности или концентрации появляются дополнительные режимы связывания, что позволяет тем же белкам мостить соседние бусины, целые волокна и даже отдельные хроматиновые капли, усиливая уплотнение. Этот гибкий набор инструментов помогает объяснить, как разные варианты H1 могут настраивать активность генов, почему некоторые из них выступают в роли супрессоров опухолей и как скромные изменения в их количестве или модификации могут реорганизовать локальную архитектуру хроматина, сдвигая баланс между открытыми, богатыми генами регионами и плотно упакованными, неактивными доменами.
Цитирование: Adhireksan, Z., Sharma, D., Bao, Q. et al. Linker histones consolidate heterogenous nucleosome fiber contacts by linking together multiple nucleosomes. Nat Commun 17, 3807 (2026). https://doi.org/10.1038/s41467-026-69842-x
Ключевые слова: уплотнение хроматина, связывающий гистон H1, нуклеосомное волокно, организация генома, эпигенетическая регуляция