Clear Sky Science · zh
内皮细胞衰老塑造慢性阻塞性肺病后期的T细胞活性
这对肺病患者为何重要
慢性阻塞性肺病(COPD)是全球导致气短、住院和早亡的主要原因之一,但现有药物大多只能缓解症状,而不能阻止疾病进展。本研究提出了一个更深层的问题:随着 COPD 从轻度发展到重度,肺内到底发生了什么变化?通过整合大型生物样本库数据、最先进的单细胞分析和机器学习,作者们发现了肺内老化血管与本应保护我们免受感染的免疫细胞之间的一个隐秘相互作用。
研究者如何在血液中寻找预警信号
为寻找与 COPD 严重程度相关的分子,研究团队首先利用来自英国生物样本库数万人的血液样本。借助机器学习,他们比较了无 COPD 人群、有 COPD 人群以及不同肺功能水平人群的蛋白模式。这一方法筛选出一小组随 COPD 出现和恶化而升高的蛋白质。其中两种蛋白 IL6 和 MMP12 尤为显著:更高的水平不仅与患 COPD 相关,还与疾病更重和随时间更差的生存率有关。在进一步查看肺组织时,IL6 显示出更明显的分期特异性信号。
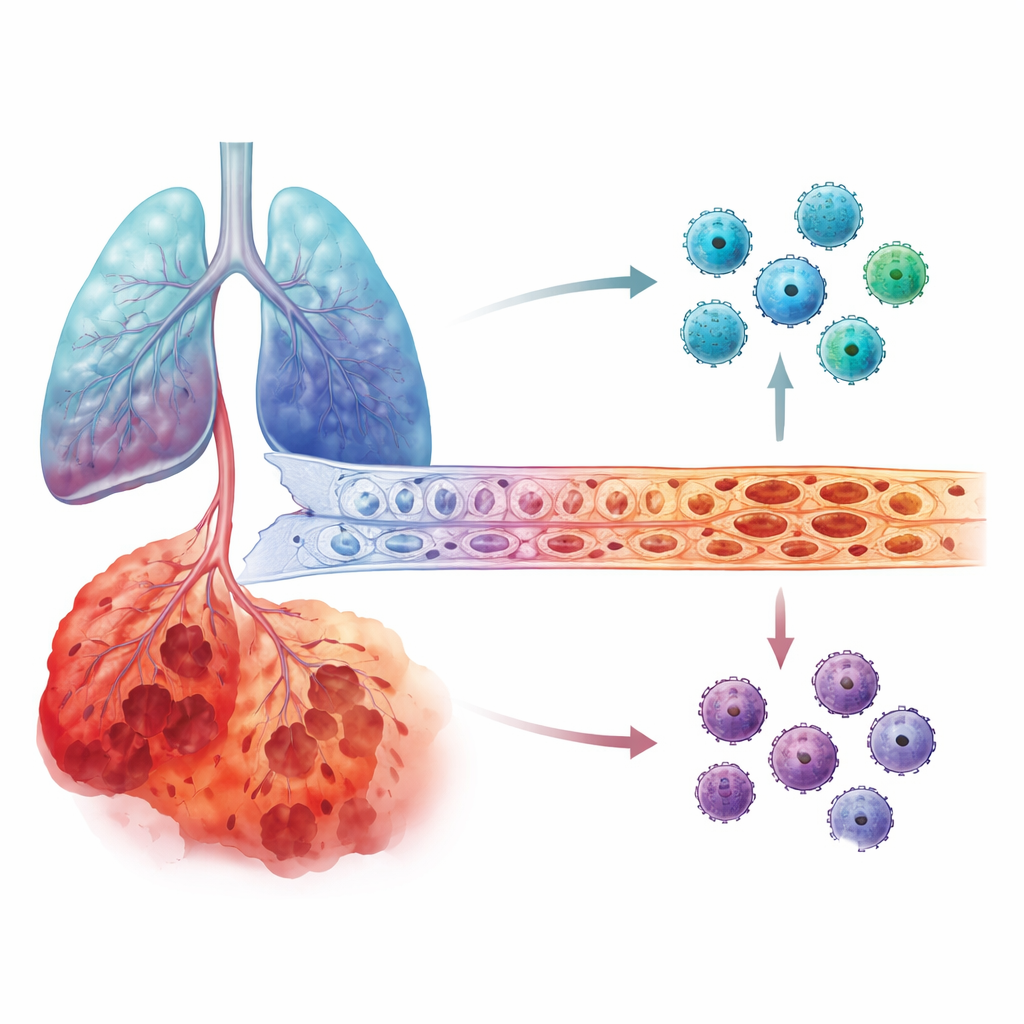
他们在受损肺组织中看到的情况
研究者随后转向肺组织数据集,包括基于总体样本的基因活动测量和可追踪每种细胞行为的单细胞 RNA 测序。他们发现 IL6 基因表达在 COPD 肺组织中明显高于健康肺组织。最为显著的是,在最严重的病例中,IL6 集中表达于肺血管内皮细胞(即血管内壁细胞)以及细小的肺泡细胞。相比之下,MMP12 并未表现出如此明显的分期突增。在多个独立患者队列中出现了相同模式:随着 COPD 的进展,晚期肺组织中的内皮细胞成为 IL6 的主要来源。
当血管细胞变老并失去平衡
深入分析后,团队探究为何重度 COPD 的内皮细胞产生大量 IL6。它们的基因谱呈现细胞衰老的典型特征——一种常被描述为“老化”或“耗竭”的永久性生长停滞状态。这些细胞表达经典的衰老基因、激活与衰老相关的调控开关,并产生被称为衰老相关分泌表型(SASP)的一组炎性分子。空间转录组学在保持真实组织位置的肺切片中显示,富含衰老标志的内皮细胞同时分泌更多 IL6。来自重度 COPD 患者的血液也呈现更强的衰老相关蛋白签名,表明这种衰老过程不仅局限于局部,而且在全身有反映。
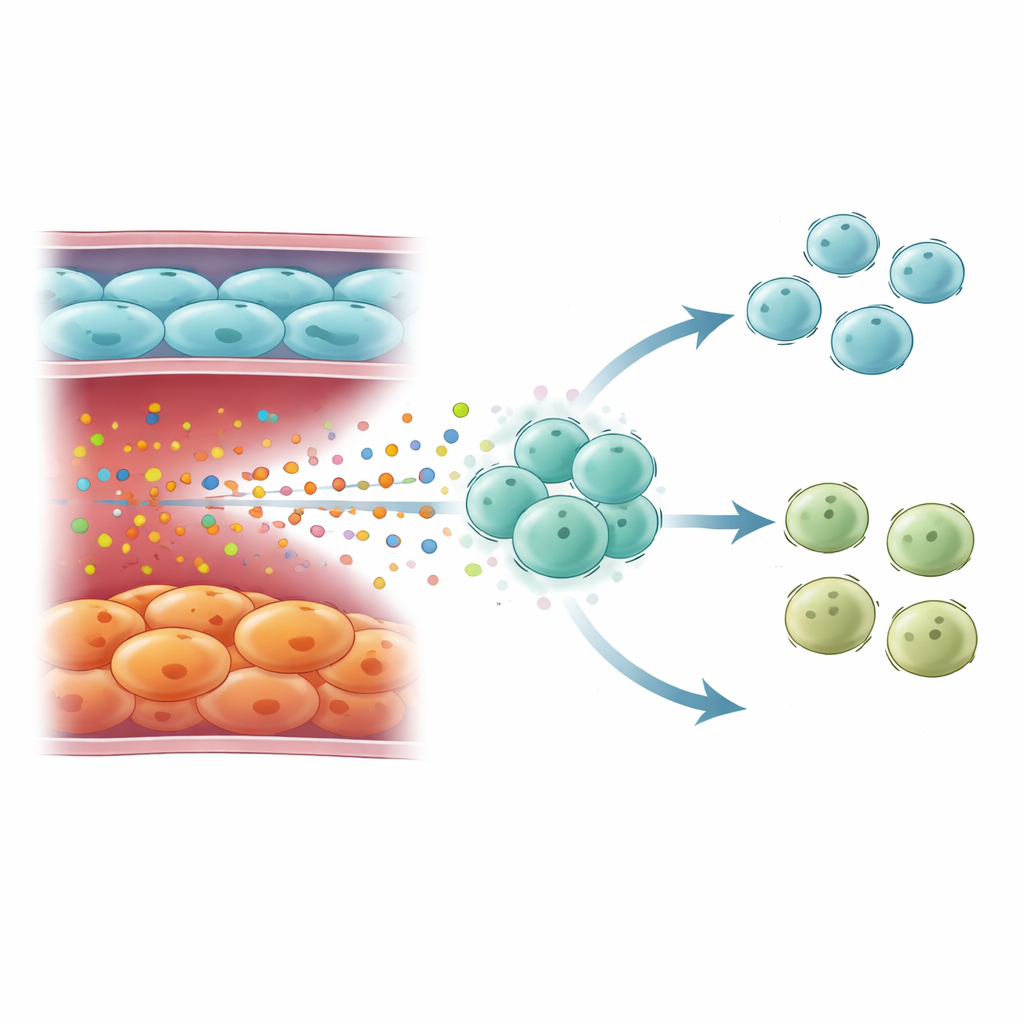
老化血管如何重塑免疫防御
来自衰老内皮细胞的高水平 IL6 并非孤立作用。对免疫细胞的单细胞图谱显示,这些信号主要指向初始状态的 T 细胞(naïve T 细胞),即能够分化为多种不同辅助类型的多才多艺白细胞。在重度 COPD 中,T 细胞群体发生了变化:初始 CD4 T 细胞累积,而对抗病毒和细菌重要的 1 型辅助 T 细胞(Th1)减少。干扰素-γ 反应的基因签名在重度疾病中下降,尽管在包括轻中度阶段的总体 COPD 中这些反应有时并不低下。晚期 COPD 的 T 细胞显示出 IL6 响应通路和 STAT3 的强烈激活,符合长期 IL6 暴露将它们从更有力的 Th1 命运转向更不具保护性的状态。
这对未来治疗意味着什么
对于患有 COPD 的人而言,这些发现提供了一种新的视角来理解为什么疾病随时间难以控制。研究表明,在晚期 COPD 中,肺血管中的老化内皮细胞像慢性信号灯一样,释放 IL6 抑制免疫防御的关键分支。这可能有助于解释为何重症患者更易感染和频繁恶化。研究还暗示,针对 IL6 或清除衰老细胞的药物可能仅在对晚期 COPD 患者进行精准治疗时才有效,而不能在所有分期一刀切地使用。简言之,本文将严重 COPD 重新框定为不仅仅是炎症加重的疾病,而是一个由悄然“老化”的血管削弱免疫系统的分期。
引用: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
关键词: COPD, 内皮细胞衰老, IL6 信号, T 细胞免疫, 慢性肺病