Clear Sky Science · de
Seneszenz von Endothelzellen prägt die T‑Zell‑Aktivität im Spätstadium der chronisch-obstruktiven Lungenerkrankung
Warum das für Menschen mit Lungenerkrankungen wichtig ist
Chronisch-obstruktive Lungenerkrankung (COPD) ist weltweit eine Hauptursache für Atemnot, Klinikeinweisungen und vorzeitigen Tod; die heutigen Medikamente lindern jedoch hauptsächlich Symptome, statt das Fortschreiten der Erkrankung zu stoppen. Diese Studie geht einer tiefergehenden Frage nach: Was verändert sich eigentlich in den Lungen, wenn COPD von milden zu schweren Stadien fortschreitet? Durch die Kombination großer Biobank‑Daten, moderner Einzelzellanalysen und maschinellen Lernens decken die Autorinnen und Autoren eine verborgene Wechselwirkung auf zwischen gealterten Blutgefäßen in der Lunge und den Immunzellen, die uns vor Infektionen schützen sollten.
Wie die Forschenden im Blut nach Warnsignalen suchten
Um Moleküle zu finden, die mit dem Schweregrad der COPD verbunden sind, startete das Team mit Blutproben von Zehntausenden Menschen aus der UK Biobank. Mithilfe maschineller Lernverfahren verglichen sie Proteingrundprofile von Personen ohne COPD, von Betroffenen und von Menschen mit unterschiedlichen Lungenfunktionswerten. Dieser Ansatz hob eine kleine Gruppe von Proteinen hervor, deren Spiegel mit dem Auftreten und der Verschlechterung der COPD anstiegen. Zwei davon, IL6 und MMP12, fielen besonders auf: höhere Konzentrationen standen nicht nur mit dem Vorliegen von COPD in Zusammenhang, sondern auch mit schwererer Erkrankung und schlechterer Überlebensprognose. Beim späteren Blick ins Lungengewebe erwies sich IL6 als das stadien‑spezifischere Signal.
Was sie in beschädigten Lungen sahen
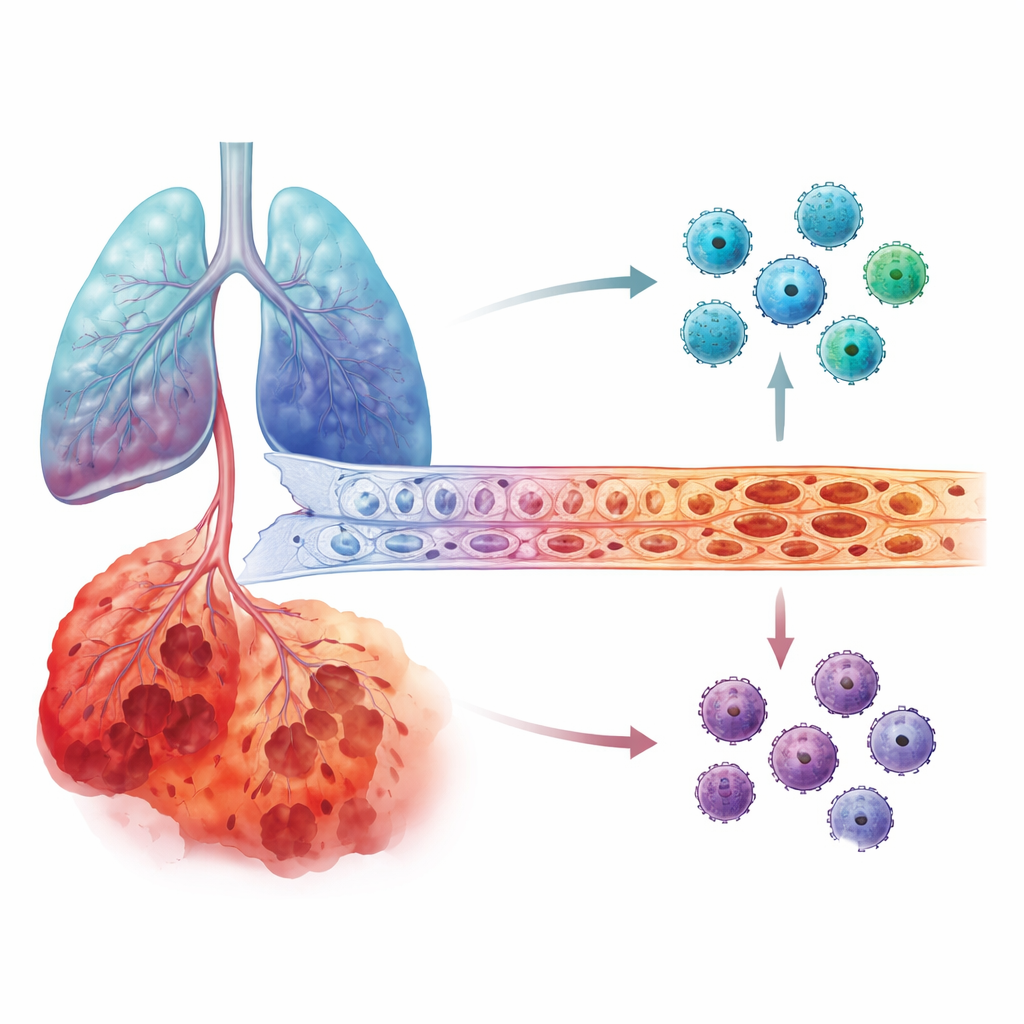
Die Forschenden untersuchten anschließend Datensätze aus Lungengewebe, darunter sowohl Bulk‑Messungen der Genaktivität als auch Einzelzell‑RNA‑Sequenzierungen, mit denen sich die Aktivität einzelner Zelltypen verfolgen lässt. Sie fanden, dass die IL6‑Genaktivität in COPD‑Lungen deutlich erhöht war im Vergleich zu gesunden Lungen. Am auffälligsten war in den schwersten Fällen, dass IL6 vor allem in den Zellen der Lungenblutgefäße (Endothelzellen) sowie in den feinen Alveolarzellen konzentriert war. Im Gegensatz dazu zeigte MMP12 keinen so deutlichen stadienabhängigen Anstieg. In mehreren unabhängigen Patientenkohorten zeigte sich dasselbe Muster: Mit fortschreitender COPD wurden Endothelzellen in Spätstadien zu einer dominanten IL6‑Quelle.
Wenn Gefäßzellen alt und unruhig werden
Auf der Suche nach dem Warum fragten die Forschenden, weshalb Endothelzellen in schwerer COPD so viel IL6 produzieren. Ihre Genmuster trugen die Kennzeichen zellulärer Seneszenz — einer Form dauerhaftem Wachstumsstillstands, die oft als „gealterte“ oder „abgenutzte“ Zellen bezeichnet wird. Diese Zellen brachten klassische Seneszenz‑Gene zum Ausdruck, aktivierten seneszenzassoziierte Steuerungswege und produzierten einen Cocktail entzündungsfördernder Moleküle, bekannt als seneszenzassoziiertes sekretorisches Phänotyp. Spatial Transcriptomics, das die räumliche Lage der Zellen in echten Lungenschnitten bewahrt, zeigte, dass Endothelzellen mit hohen Seneszenzmarkern auch vermehrt IL6 abgaben. Blutproben von Patientinnen und Patienten mit schwerer COPD zeigten ebenfalls stärkere seneszenzbezogene Proteinsignaturen, was darauf hindeutet, dass dieser Alterungsprozess nicht nur lokal begrenzt ist, sondern sich systemisch widerspiegelt.
Wie gealterte Gefäße die Immunabwehr umgestalten
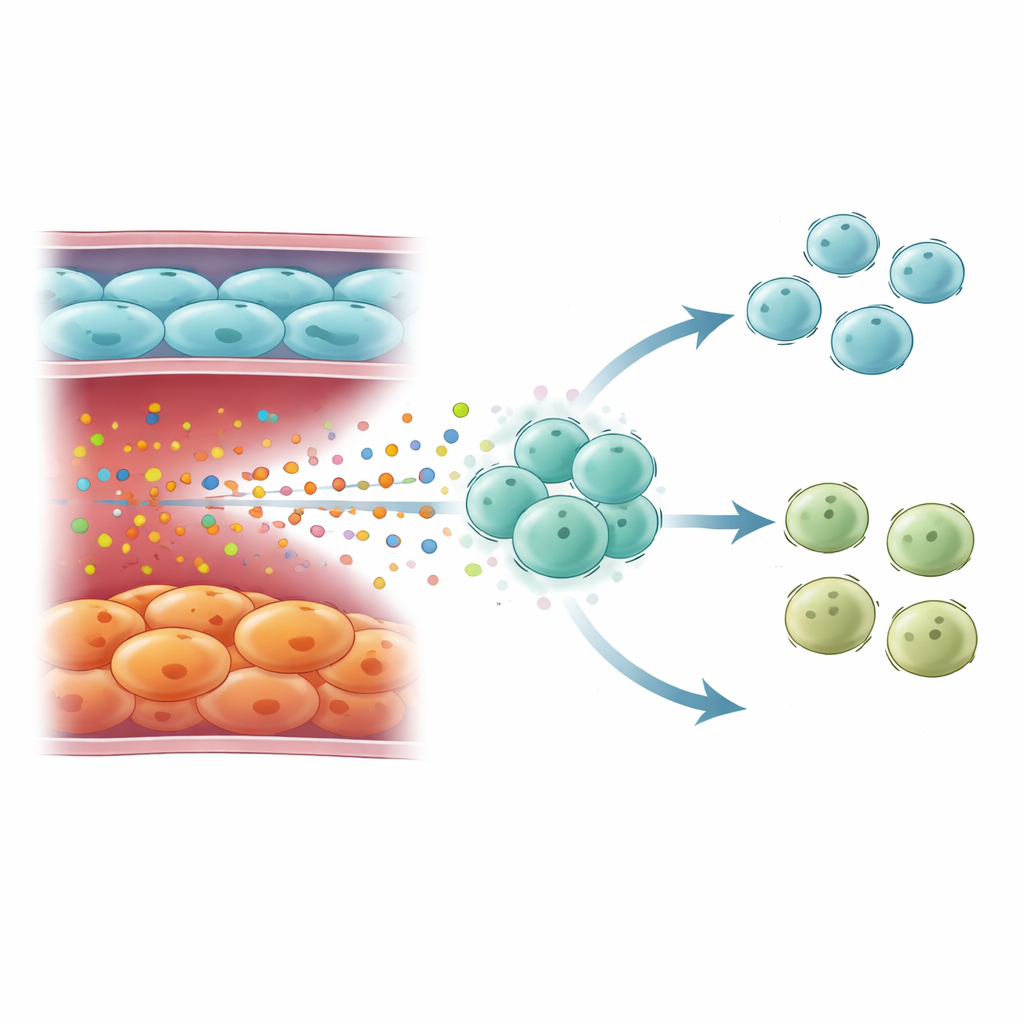
Das hohe IL6 aus seneszenten Endothelzellen wirkte nicht isoliert. Einzelzellkarten des Immunsystems zeigten, dass diese Signale vor allem auf naive T‑Zellen zielten, die vielseitigen weißen Blutzellen, die sich zu verschiedenen Helferuntertypen differenzieren können. In schwerer COPD verschoben sich die T‑Zell‑Populationen: Naive CD4‑T‑Zellen häuften sich, während Typ‑1‑Helfer‑T‑Zellen (Th1) — wichtig für die Abwehr von Viren und Bakterien über das Zytokin Interferon‑gamma — verringert waren. Gen‑Signaturen von Interferon‑gamma‑Reaktionen nahmen im schweren Krankheitsstadium ab, auch wenn sie bei COPD insgesamt in milden und moderaten Stadien erhöht sein können. T‑Zellen im Spätstadium der COPD zeigten starke Aktivierung IL6‑reaktiver Pfade und von STAT3, was zu einem langfristigen IL6‑Einfluss passt, der sie von einem robusten Th1‑Schicksal weg und in einen weniger protektiven Zustand lenkt.
Was das für zukünftige Therapien bedeutet
Für Menschen mit COPD bieten diese Befunde eine neue Perspektive darauf, warum sich die Erkrankung mit der Zeit schlechter kontrollieren lässt. Die Studie legt nahe, dass in Spätstadien der COPD gealterte Endothelzellen in den Lungengefäßen wie chronische Signalgeber wirken und IL6 freisetzen, das einen wichtigen Arm der Immunabwehr dämpft. Das könnte erklären, warum Patientinnen und Patienten mit schwerer Erkrankung anfälliger für Infektionen und häufigere Exazerbationen sind. Die Arbeit deutet außerdem an, dass Medikamente, die IL6 oder seneszente Zellen anvisieren, nur dann wirksam sein könnten, wenn sie gezielt bei fortgeschrittener COPD eingesetzt werden, statt über alle Stadien hinweg einheitlich angewandt zu werden. Kurz gesagt: Die Studie rückt schwere COPD nicht lediglich als zunehmende Entzündung in den Fokus, sondern als ein Stadium, das durch gealterte Blutgefäße gekennzeichnet ist, die das Immunsystem stillschweigend schwächen.
Zitation: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
Schlüsselwörter: COPD, endotheliale Seneszenz, IL6‑Signalgebung, T‑Zell‑Immunität, chronische Lungenerkrankung