Clear Sky Science · es
La senescencia de las células endoteliales modula la actividad de los linfocitos T en estadios avanzados de la enfermedad pulmonar obstructiva crónica
Por qué esto importa para las personas con enfermedad pulmonar
La enfermedad pulmonar obstructiva crónica (EPOC) es una causa principal de dificultad respiratoria, ingresos hospitalarios y muerte prematura en todo el mundo; sin embargo, los tratamientos actuales en su mayoría alivian los síntomas en lugar de detener la progresión de la enfermedad. Este estudio plantea una pregunta más profunda: ¿qué cambia realmente dentro de los pulmones a medida que la EPOC avanza de leve a grave? Combinando grandes datos de biobancos, análisis de células individuales de vanguardia y aprendizaje automático, los autores descubren una interacción oculta entre los vasos sanguíneos envejecidos del pulmón y las células inmunitarias que deberían protegernos de las infecciones.
Cómo los investigadores buscaron señales en la sangre
Para identificar moléculas vinculadas con la gravedad de la EPOC, el equipo partió de muestras de sangre de decenas de miles de personas del Biobanco del Reino Unido. Usando aprendizaje automático, compararon los patrones de proteínas en personas sin EPOC, con la enfermedad y con distintos niveles de función pulmonar. Este enfoque destacó un pequeño grupo de proteínas cuyos niveles aumentaban a medida que aparecía y empeoraba la EPOC. Dos en particular, IL6 y MMP12, llamaron la atención: niveles más altos se asociaron no solo con la presencia de EPOC, sino también con enfermedad más grave y peor supervivencia a lo largo del tiempo. De ellas, IL6 emergió como la señal más específica de estadio cuando los investigadores posteriormente examinaron el tejido pulmonar.
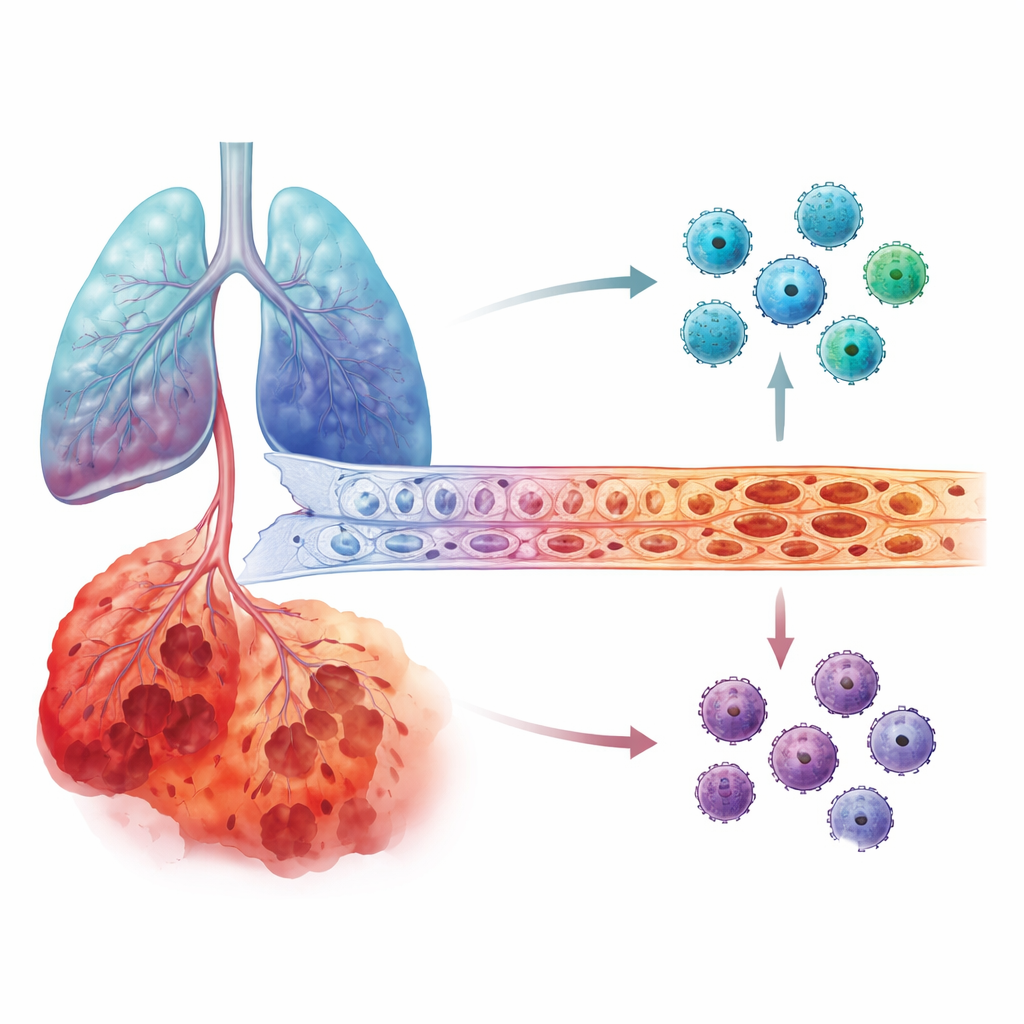
Lo que observaron dentro de los pulmones dañados
Los investigadores se volcaron luego a conjuntos de datos de tejido pulmonar, que incluyeron tanto medidas globales de actividad génica como secuenciación de ARN a nivel de célula única, capaz de seguir qué hace cada tipo celular. Encontraron que la actividad génica de IL6 era claramente mayor en pulmones con EPOC que en pulmones sanos. Lo más llamativo fue que, en los casos más graves, IL6 se concentraba en las células que recubren los vasos sanguíneos pulmonares, conocidas como células endoteliales, así como en las células de los delicados alvéolos. En contraste, MMP12 no mostró un salto tan marcado y específico por estadio. A través de varias cohortes independientes de pacientes emergió el mismo patrón: conforme la EPOC avanzaba, las células endoteliales en estadios tardíos se convertían en una fuente dominante de IL6.
Cuando las células de los vasos sanguíneos envejecen y se alteran
Indagando más, el equipo preguntó por qué las células endoteliales en EPOC severa producen tanto IL6. Sus patrones génicos mostraban las huellas de la senescencia celular: una forma de paro de crecimiento permanente descrita como células “envejecidas” o “agotadas”. Estas células expresaban genes clásicos de senescencia, activaban interruptores regulatorios vinculados a la senescencia y producían un cóctel de moléculas inflamatorias conocido como fenotipo secretor asociado a la senescencia. La transcriptómica espacial, que preserva la localización de las células en cortes reales de pulmón, mostró que las células endoteliales con marcadores de senescencia también liberaban más IL6. La sangre de pacientes con EPOC grave presentaba de igual modo firmas proteicas relacionadas con la senescencia más intensas, lo que sugiere que este proceso de envejecimiento no es solo local sino que se refleja en todo el organismo.
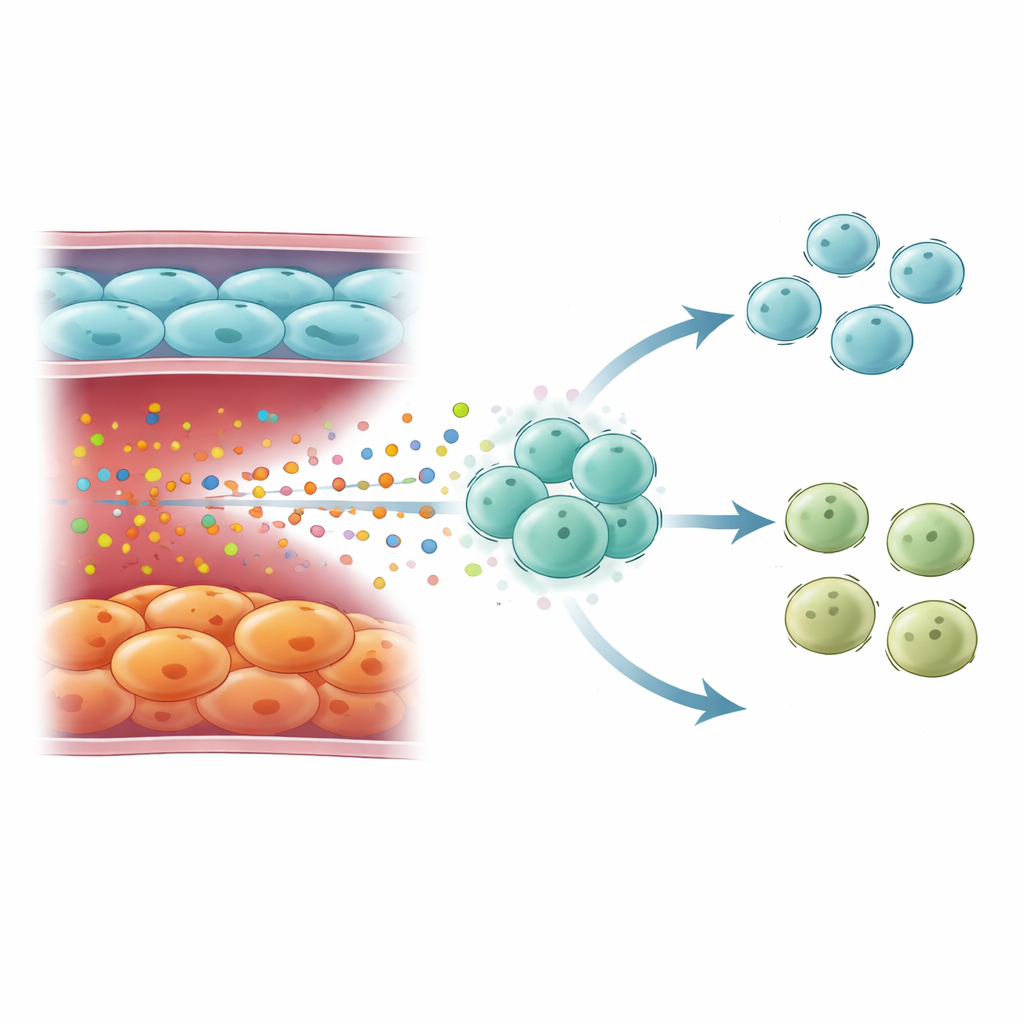
Cómo los vasos envejecidos remodelan las defensas inmunitarias
El alto IL6 procedente de células endoteliales senescentes no actuaba de forma aislada. Mapas de células inmunitarias a nivel de célula única revelaron que estas señales se dirigían principalmente a las células T naïve, los glóbulos blancos versátiles que pueden diferenciarse en varios tipos de ayudantes. En la EPOC severa, las poblaciones de células T cambiaron: las células T CD4 naïve se acumularon, mientras que las células T helper tipo 1 (Th1)—importantes para combatir virus y bacterias mediante la citocina interferón gamma—se vieron disminuidas. Las firmas génicas de respuestas mediadas por interferón gamma cayeron en enfermedad severa, aunque podían estar elevadas en la EPOC en conjunto cuando se incluían los estadios leves y moderados. Las células T en EPOC avanzada mostraron fuerte activación de vías dependientes de IL6 y de STAT3, consistente con una exposición prolongada a IL6 que las desvía de un destino Th1 robusto hacia un estado menos protector.
Qué significa esto para futuros tratamientos
Para las personas con EPOC, estos hallazgos ofrecen una nueva manera de entender por qué la enfermedad se vuelve más difícil de controlar con el tiempo. El estudio sugiere que en la EPOC avanzada, las células endoteliales envejecidas de los vasos pulmonares actúan como faros de señal crónica, liberando IL6 que atenúa un brazo clave de la defensa inmunitaria. Esto podría ayudar a explicar por qué los pacientes con enfermedad grave son más propensos a infecciones y a brotes frecuentes. El trabajo también implica que los fármacos dirigidos contra IL6 o contra las células senescentes podrían ser efectivos solo si se orientan a quienes tienen EPOC avanzada, en lugar de aplicarse de forma uniforme en todos los estadios. En suma, el artículo replantea la EPOC severa no solo como una inflamación creciente, sino como un estadio marcado por vasos sanguíneos envejecidos que silenciosamente desarman al sistema inmunitario.
Cita: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
Palabras clave: EPOC, senescencia endotelial, señalización IL6, inmunidad de células T, enfermedad pulmonar crónica