Clear Sky Science · pl
Starzenie komórek śródbłonka kształtuje aktywność limfocytów T w późnym stadium przewlekłej obturacyjnej choroby płuc
Dlaczego to ma znaczenie dla osób z chorobami płuc
Przewlekła obturacyjna choroba płuc (POChP) jest jedną z głównych przyczyn duszności, hospitalizacji i przedwczesnych zgonów na świecie, a istniejące leki w dużej mierze łagodzą objawy, zamiast zatrzymać postęp choroby. To badanie stawia głębsze pytanie: co naprawdę zmienia się w płucach, gdy POChP przechodzi ze stadium łagodnego do ciężkiego? Łącząc duże zasoby biobankowe, nowoczesne analizy pojedynczych komórek i uczenie maszynowe, autorzy odkrywają ukrytą interakcję między starzejącymi się naczyniami krwionośnymi w płucu a komórkami odpornościowymi, które powinny nas chronić przed infekcjami.
Jak badacze szukali ostrzegawczych sygnałów we krwi
Aby odnaleźć molekuły związane z ciężkością POChP, zespół zaczął od próbek krwi dziesiątek tysięcy osób z UK Biobank. Korzystając z uczenia maszynowego, porównali wzorce białek u osób bez POChP, chorych oraz osób o różnym stopniu sprawności płuc. Takie podejście wyodrębniło niewielką grupę białek, których poziomy wzrastały wraz z pojawieniem się i postępem POChP. Dwa z nich — IL6 i MMP12 — szczególnie się wyróżniały: wyższe stężenia wiązały się nie tylko z obecnością POChP, lecz także z cięższym przebiegiem choroby i gorszym przeżyciem w czasie. Spośród nich IL6 okazało się sygnałem bardziej specyficznym dla stadium choroby, gdy badacze przyjrzeli się później tkance płucnej.
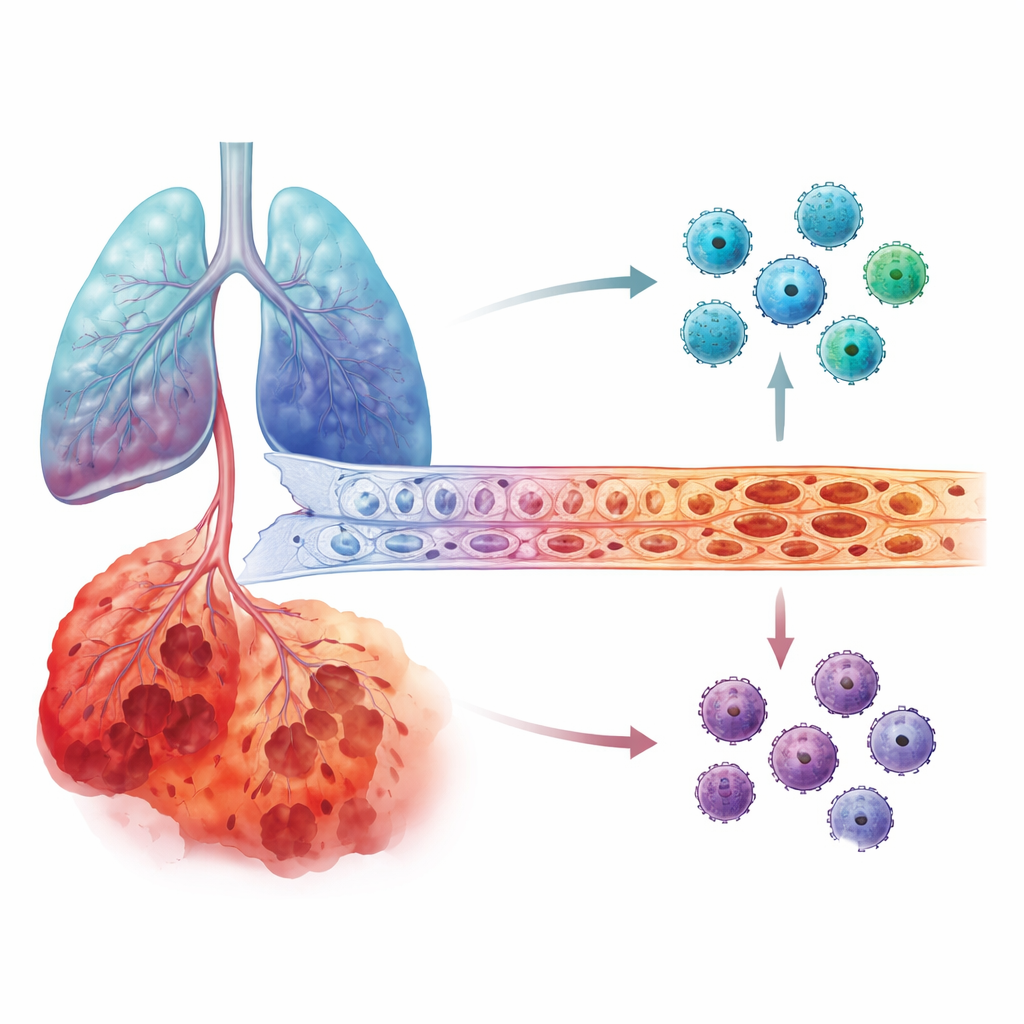
Co zobaczyli w uszkodzonych płucach
Następnie badacze zwrócili się do zbiorów danych tkanki płucnej, obejmujących zarówno pomiary ogólne aktywności genów, jak i sekwencjonowanie RNA pojedynczych komórek, które pozwala śledzić zachowanie poszczególnych typów komórek. Stwierdzili, że aktywność genu IL6 była wyraźnie wyższa w płucach osób z POChP niż u zdrowych. Co najbardziej uderzało, w najcięższych przypadkach IL6 skupiało się w komórkach wyściełających naczynia krwionośne płuc, zwanych komórkami śródbłonka, oraz w delikatnych komórkach pęcherzyków płucnych. W przeciwieństwie do tego MMP12 nie wykazywało tak wyraźnego, zależnego od stadium skoku. W kilku niezależnych kohortach pacjentów pojawiał się ten sam wzór: w miarę postępu POChP komórki śródbłonka w płucach w późnym stadium stawały się dominującym źródłem IL6.
Gdy komórki naczyń krwionośnych się starzeją i zbuntują
Zagłębiając się dalej, zespół pytał, dlaczego komórki śródbłonka w ciężkim POChP produkują tak dużo IL6. Ich wzorce genowe nosiły cechy senescencji komórkowej — formy trwałego zatrzymania wzrostu często opisywanej jako „starzejące się” lub „zużyte” komórki. Komórki te wykazywały ekspresję klasycznych genów senescencji, aktywację powiązanych przełączników regulacyjnych i produkowały koktajl zapalnych molekuł znanych jako sekretom senescencyjny (senescence-associated secretory phenotype). Transkryptomika przestrzenna, która zachowuje położenie komórek w rzeczywistych plasterkach płuca, pokazała, że komórki śródbłonka bogate w markery senescencji również wydzielają więcej IL6. Krew pacjentów z ciężkim POChP zawierała podobnie silniejsze sygnatury białkowe związane z senescencją, co sugeruje, że ten proces starzenia nie jest jedynie lokalny, lecz odzwierciedla się w całym organizmie.
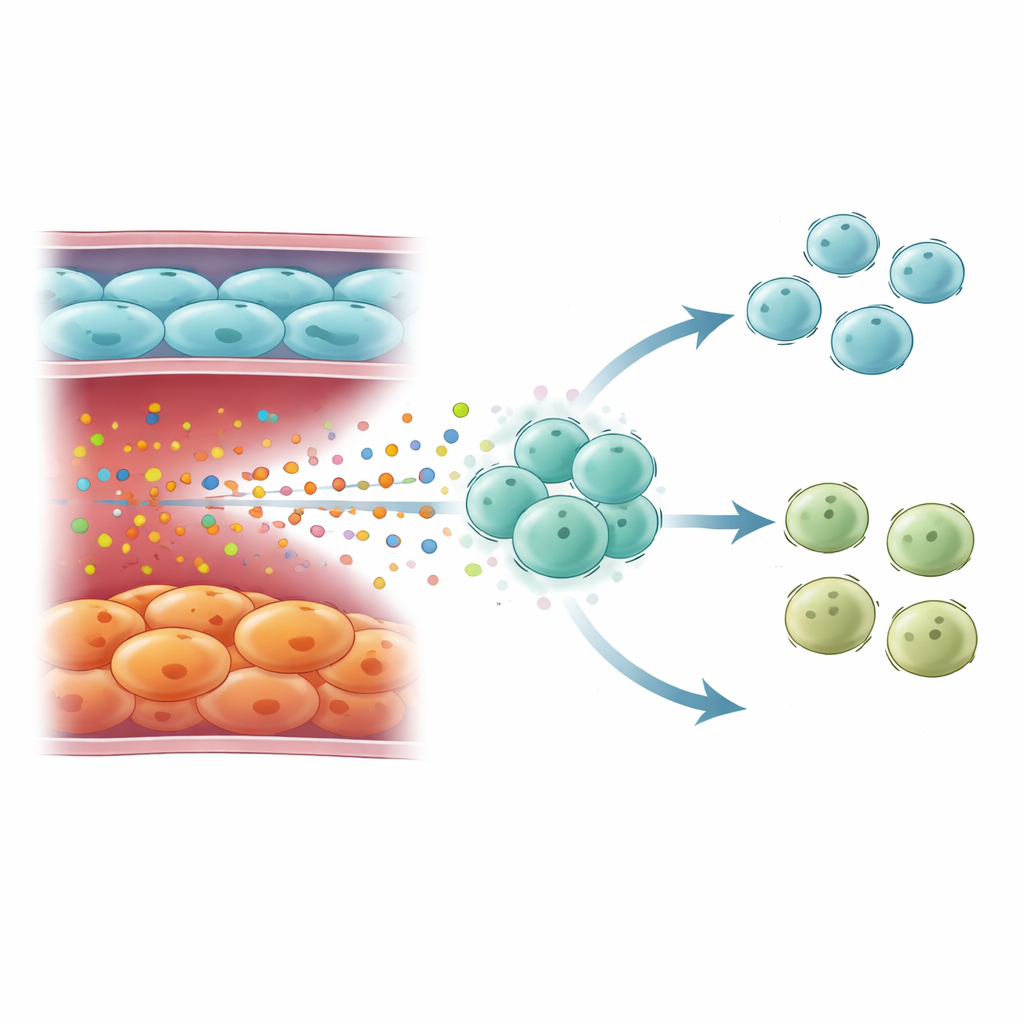
Jak starzejące się naczynia zmieniają obronę immunologiczną
Wysokie stężenie IL6 pochodzące od senescentnych komórek śródbłonka nie działało w izolacji. Mapy pojedynczych komórek układu odpornościowego ujawniły, że te sygnały kierowane były głównie do naiwnych limfocytów T — wszechstronnych białych krwinek, które mogą różnicować się w wiele podtypów pomocniczych. W zaawansowanym POChP zasoby limfocytów T uległy przesunięciu: gromadziły się naiwnie CD4 T, podczas gdy limfocyty pomocnicze typu 1 (Th1) — ważne w walce z wirusami i bakteriami poprzez interferon gamma — były zubożone. Sygnatury genowe odpowiedzi na interferon gamma spadały w ciężkiej chorobie, choć gdy brano pod uwagę cały przekrój od łagodnego do umiarkowanego, mogły być wyższe w POChP ogólnie. Limfocyty T w późnym stadium POChP wykazywały silną aktywację ścieżek odpowiadających na IL6 i STAT3, co jest zgodne z długotrwałą ekspozycją na IL6 kierującą je z dala od odpornej fenotypowo odpowiedzi Th1 i w stronę mniej ochronnego stanu.
Co to znaczy dla przyszłych terapii
Dla osób żyjących z POChP te odkrycia oferują nowe spojrzenie na to, dlaczego choroba staje się trudniejsza do opanowania z czasem. Badanie sugeruje, że w późnym stadium POChP starzejące się komórki śródbłonka naczyń płucnych zachowują się jak przewlekłe „latarnie sygnałowe”, uwalniając IL6, które tłumi kluczowy element obrony immunologicznej. To może pomóc wyjaśnić, dlaczego pacjenci z ciężką chorobą częściej doświadczają infekcji i nawracających zaostrzeń. Praca wskazuje też, że leki celujące w IL6 lub komórki senescentne mogą być skuteczne jedynie wtedy, gdy są dopasowane do osób z zaawansowanym POChP, zamiast stosować je równomiernie na wszystkich etapach. Krótko mówiąc, artykuł przekształca spojrzenie na ciężką POChP — nie tylko jako nasilający się stan zapalny, lecz jako stadium naznaczone starzeniem naczyń, które po cichu osłabia układ odpornościowy.
Cytowanie: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
Słowa kluczowe: POChP, senescencja śródbłonka, sygnalizacja IL6, odporność limfocytów T, przewlekła choroba płuc