Clear Sky Science · ar
شيخوخة الخلايا الباطنية تشكّل نشاط الخلايا التائية في المراحل المتأخرة من داء الانسداد الرئوي المزمن
لماذا يهم هذا الأشخاص المصابين بأمراض الرئة
يعد داء الانسداد الرئوي المزمن (COPD) سبباً رئيسياً لصعوبة التنفّس وزيارات المستشفى والوفاة المبكرة على مستوى العالم، ومع ذلك تقتصر أدوية اليوم غالباً على تخفيف الأعراض بدلاً من إيقاف تدهور المرض. يطرح هذا البحث سؤالاً أعمق: ما الذي يتغير فعلاً داخل الرئتين مع تقدم COPD من خفيف إلى شديد؟ من خلال دمج بيانات كبيرة من بنوك عينات، وتحليلات الخلية الواحدة المتطورة، والتعلّم الآلي، يكشف الباحثون عن تفاعل خفي بين أوعية دموية مسنة في الرئة والخلايا المناعية التي يفترض أن تحمينا من العدوى.
كيف بحث الباحثون في الدم عن إشارات تحذيرية
للعثور على جزيئات مرتبطة بشدة COPD، بدأ الفريق بعينات دم من عشرات الآلاف من الأشخاص في بنك بيانات UK Biobank. باستخدام التعلّم الآلي، قارنوا أنماط البروتين لدى الأشخاص غير المصابين بـCOPD، وأولئك المصابين بالمرض، ومن لديهم مستويات متباينة من وظيفة الرئة. أبرز هذا النهج مجموعة صغيرة من البروتينات التي ارتفعت مستوياتها مع ظهور COPD وتدهوره. تميّزا منها اثنان، IL6 وMMP12: كانت المستويات الأعلى مرتبطة ليس فقط بوجود COPD بل أيضاً بشدّة أكبر للمرض وببقاء أسوأ بمرور الوقت. ومن بين هذين، برز IL6 كإشارة أكثر تخصيصاً للمرحلة عندما نظر الباحثون لاحقاً داخل نسيج الرئة نفسه.
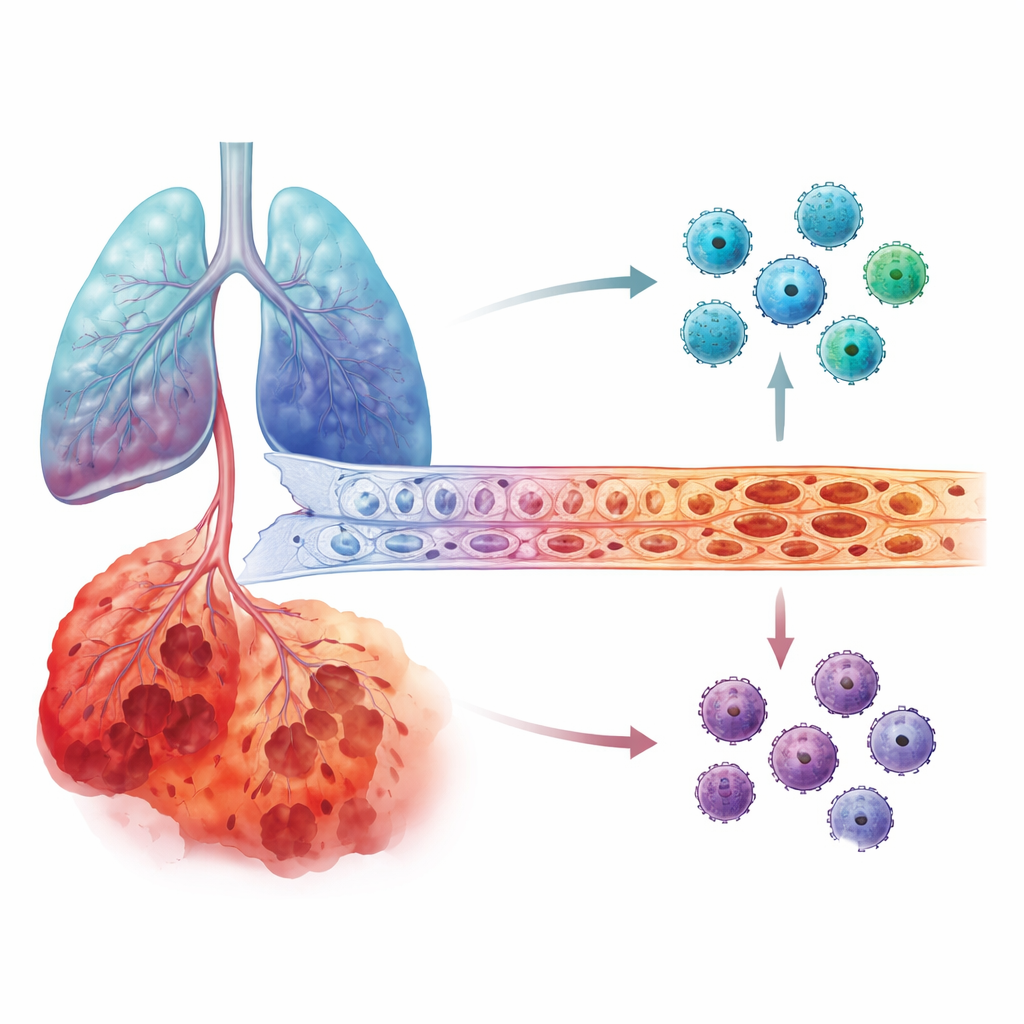
ما رأوه داخل الرئات المتضررة
تجه الباحثون بعد ذلك إلى مجموعات بيانات نسيج الرئة، بما في ذلك قياسات جينية مجمعة ونمطية RNA لكل خلية مفردة، التي تتتبّع ما تفعله كل نوع خلية على حدة. وجدوا أن نشاط جين IL6 أعلى بوضوح في رئات المصابين بـCOPD مقارنة بالرئات السليمة. والأبرز أن IL6 في الحالات الأكثر شدة تمركزت في الخلايا المبطنة للأوعية الدموية الرئوية، المعروفة بالخلايا الباطنية، وكذلك في خلايا الحويصلات الهوائية الهشة. بالمقابل، لم يظهر MMP12 قفزة مرحلية حادة مماثلة. عبر عدة مجموعات مرضى مستقلة، ظهر نمط مماثل: مع تقدم COPD، أصبحت الخلايا الباطنية في الرئات المتأخرة مصدراً مهيمنًا لـIL6.
عندما تكبر خلايا الأوعية الدموية وتصبح قلقة
بالغوص أعمق، تساءل الفريق لماذا تصنع الخلايا الباطنية في COPD الشديد هذا الكمّ من IL6. حملت أنماط الجينات لديها سمات الشيخوخة الخلوية — شكل من أشكال التوقّف الدائم عن الانقسام يوصف غالباً بأنه خلايا «هرمة» أو «مهترئة». عبّرت هذه الخلايا عن جينات شيخوخة كلاسيكية، وفعتلت مفاتيح تحكم مرتبطة بالشيخوخة، وأنتجت مزيجاً من الجزيئات الالتهابية المعروفة بظاهرة الإفراز المرتبطة بالشيخوخة (SASP). أظهرت النسخ المكانية، التي تحافظ على مواضع الخلايا في شرائح رئة حقيقية، أن الخلايا الباطنية الغنية بعلامات الشيخوخة أيضاً تفرز مزيداً من IL6. وحمَلت عينات الدم من مرضى COPD الشديد كذلك تواقيع بروتينية أقوى ذات صلة بالشيخوخة، مما يوحي بأن هذه العملية الشيخوخية ليست محلية فقط بل تنعكس في كامل الجسم.
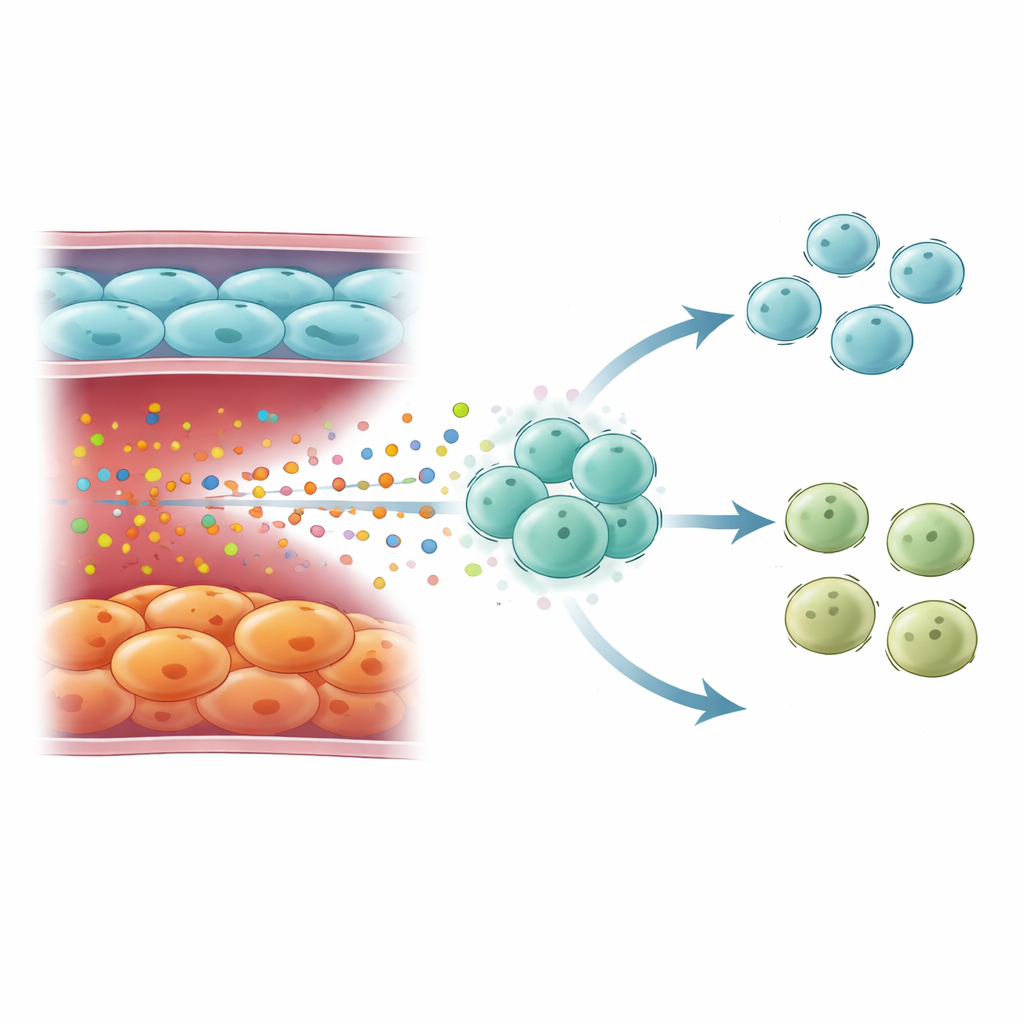
كيف تعيد الأوعية المسنة تشكيل الدفاعات المناعية
لم تعمل مستويات IL6 المرتفعة من الخلايا الباطنية المسنة بمعزل عن غيرها. أظهرت خرائط الخلايا المفردة للخلايا المناعية أن هذه الإشارات كانت موجهة أساساً نحو الخلايا التائية الساذجة، وهي خلايا دم بيضاء متعددة الاستخدامات قادرة على التحوّل إلى أنواع مساعدة مختلفة. في COPD الشديد تحوّلت مجموعات الخلايا التائية: تراكمت الخلايا التائية CD4 الساذجة، بينما تقلصت خلايا المساعدة من النوع 1 (Th1) — الضرورية لمكافحة الفيروسات والبكتيريا عبر السيتوكين إنترفيرون غاما. انخفضت تواقيع جينيات استجابات إنترفيرون غاما في المرض الشديد، رغم أنها قد تكون أعلى في COPD الإجمالي عند احتساب المراحل الخفيفة والمتوسطة. أظهرت الخلايا التائية في COPD المتأخر تفعيلًا قويًا للمسارات المستجيبة لـIL6 وSTAT3، ما يتوافق مع تعرض طويل الأمد لـIL6 يوجّهها بعيداً عن مصير Th1 القوي ونحو حالة أقل حماية.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة للأشخاص الذين يعيشون مع COPD، تقدّم هذه النتائج طريقة جديدة للتفكير في سبب صعوبة السيطرة على المرض مع مرور الوقت. يقترح البحث أن في COPD المتأخر، تتصرف الخلايا الباطنية المسنة في أوعية الدم الرئوية كمنارات إشارية مزمنة، تطلق IL6 التي تكبح ذراعاً رئيسية من الدفاع المناعي. قد يساعد هذا في تفسير لماذا يكون المرضى ذوو الحالات الشديدة أكثر عرضة للعدوى والنوبات المتكررة. كما يوحي العمل أن الأدوية المستهدفة لـIL6 أو الخلايا المسنة قد تكون فعّالة فقط إذا تم توجيهها للأشخاص ذوي COPD المتقدم، بدلاً من تطبيقها بشكل موحّد على جميع المراحل. باختصار، يعيد البحث صياغة COPD الشديد ليس فقط كالتهاب متفاقم، بل كمرحلة تتميز بأوعية دموية مسنة تعطل الجهاز المناعي بهدوء.
الاستشهاد: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
الكلمات المفتاحية: داء الانسداد الرئوي المزمن, شيخوخة الخلايا الباطنية, إشارة IL6, مناعة الخلايا التائية, أمراض الرئة المزمنة