Clear Sky Science · fr
La sénescence des cellules endothéliales module l’activité des lymphocytes T au stade avancé de la maladie pulmonaire obstructive chronique
Pourquoi cela importe pour les personnes atteintes de maladie pulmonaire
La maladie pulmonaire obstructive chronique (MPOC) est une cause majeure d’essoufflement, d’hospitalisations et de décès prématuré dans le monde. Pourtant, les traitements actuels soulagent surtout les symptômes sans empêcher la progression de la maladie. Cette étude pose une question plus fondamentale : que change réellement à l’intérieur des poumons lorsque la MPOC passe d’un stade léger à un stade sévère ? En combinant de larges bases de données, des analyses unicellulaires de pointe et l’apprentissage automatique, les auteurs mettent au jour une interaction cachée entre le vieillissement des vaisseaux sanguins pulmonaires et les cellules immunitaires censées nous protéger des infections.
Comment les chercheurs ont cherché des signaux d’alerte dans le sang
Pour identifier des molécules liées à la gravité de la MPOC, l’équipe a commencé par des échantillons sanguins de dizaines de milliers de participants de l’UK Biobank. À l’aide de l’apprentissage automatique, ils ont comparé les profils protéiques chez des personnes sans MPOC, chez des malades et selon différents niveaux de fonction pulmonaire. Cette approche a mis en évidence un petit groupe de protéines dont les concentrations augmentaient avec l’apparition et l’aggravation de la MPOC. Deux d’entre elles, en particulier, IL6 et MMP12, se sont distinguées : des taux plus élevés étaient liés non seulement à la présence de MPOC mais aussi à une maladie plus sévère et à une survie réduite au fil du temps. Parmi elles, IL6 est apparue comme le signal le plus spécifique au stade lorsque les chercheurs ont ensuite examiné le tissu pulmonaire lui-même.
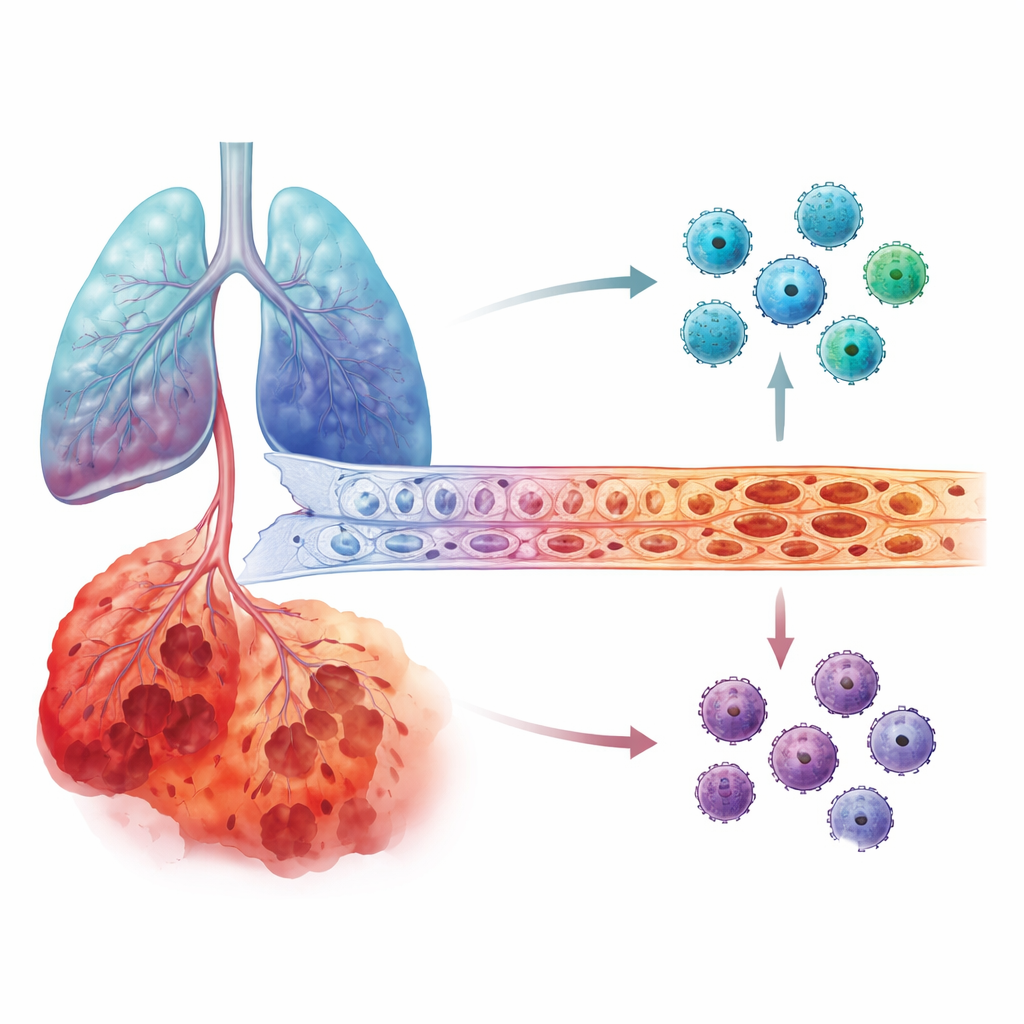
Ce qu’ils ont observé dans les poumons endommagés
Les investigateurs se sont ensuite tournés vers des jeux de données de tissu pulmonaire, incluant des mesures globales d’activité génique et du séquençage ARN unicellulaire, qui permet de suivre l’activité de chaque type cellulaire. Ils ont constaté que l’expression du gène IL6 était nettement plus élevée dans les poumons des patients MPOC que dans ceux en bonne santé. Plus frappant, dans les cas les plus sévères, IL6 était concentrée dans les cellules qui tapissent les vaisseaux sanguins pulmonaires, appelées cellules endothéliales, ainsi que dans les cellules des alvéoles. En revanche, MMP12 n’affichait pas un saut aussi marqué selon le stade. À travers plusieurs cohortes indépendantes, le même schéma est apparu : à mesure que la MPOC progressait, les cellules endothéliales des poumons au stade avancé devenaient une source dominante d’IL6.
Quand les cellules vasculaires vieillissent et deviennent agitées
En approfondissant, l’équipe s’est demandé pourquoi les cellules endothéliales dans la MPOC sévère produisent autant d’IL6. Leurs profils géniques portaient les marques de la sénescence cellulaire — une forme d’arrêt permanent de la prolifération souvent décrite comme des cellules « vieillies » ou « usées ». Ces cellules exprimaient des gènes classiques de sénescence, activaient des bascules de contrôle liées à la sénescence et produisaient un cocktail de molécules inflammatoires connu sous le nom de phénotype sécrétoire associé à la sénescence. La transcriptomique spatiale, qui conserve la position des cellules dans de vraies coupes pulmonaires, a montré que les cellules endothéliales riches en marqueurs de sénescence sécrétaient également davantage d’IL6. Le sang des patients atteints de MPOC sévère portait lui aussi des signatures protéiques renforcées liées à la sénescence, suggérant que ce processus de vieillissement n’est pas seulement local mais se reflète dans tout l’organisme.
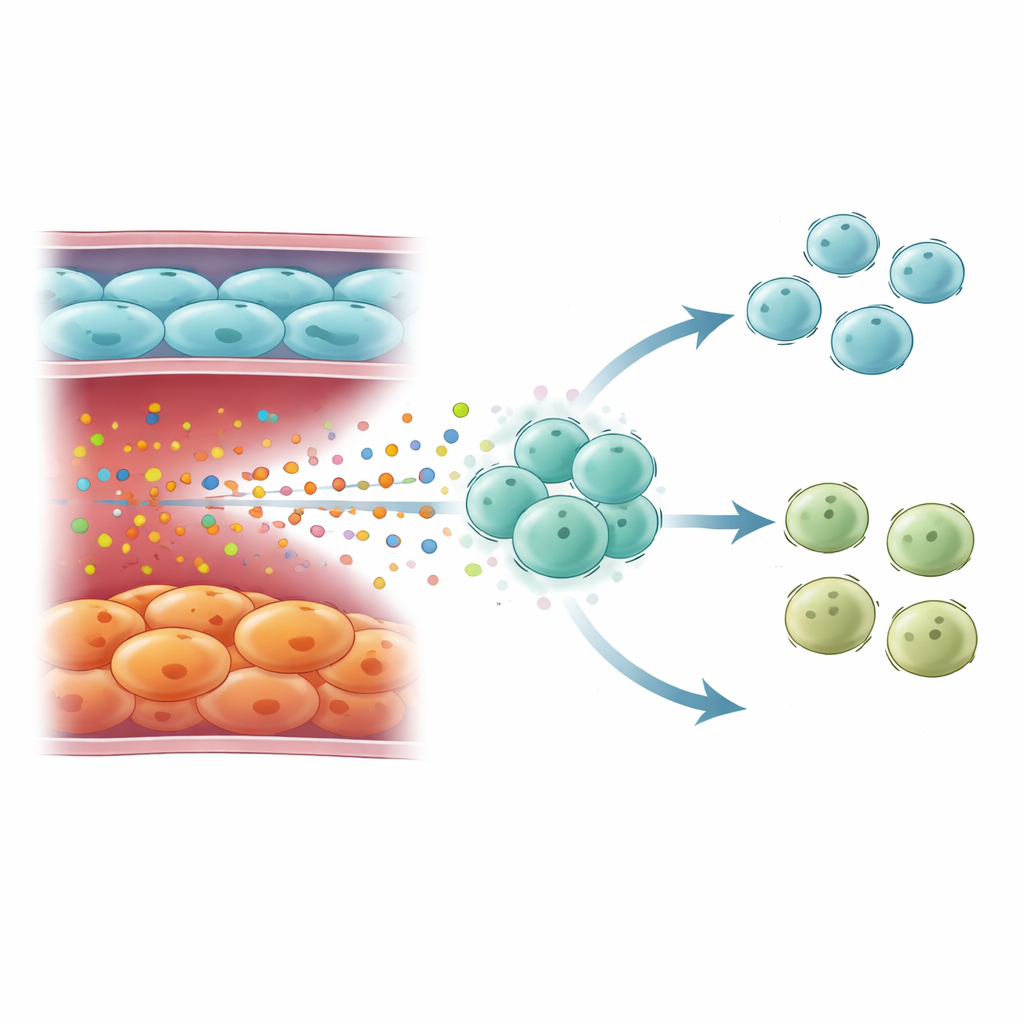
Comment les vaisseaux vieillissants reshappent les défenses immunitaires
La forte production d’IL6 par des cellules endothéliales sénescentes n’agissait pas isolément. Les cartographies unicellulaires des cellules immunitaires ont révélé que ces signaux visaient principalement les lymphocytes T naïfs, ces globules blancs polyvalents capables de se différencier en plusieurs sous-types auxiliaires. Dans la MPOC sévère, les populations de lymphocytes T évoluaient : les cellules T CD4 naïves s’accumulaient, tandis que les cellules T auxiliaires de type 1 (Th1) — importantes pour lutter contre virus et bactéries via l’interféron gamma — étaient réduites. Les signatures géniques des réponses à l’interféron gamma décroissaient dans la maladie avancée, même si elles pouvaient être plus élevées dans la MPOC globale quand les stades légers et modérés étaient inclus. Les lymphocytes T des poumons au stade avancé présentaient une activation marquée des voies dépendantes d’IL6 et de STAT3, cohérente avec une exposition prolongée à l’IL6 qui les détourne d’un destin Th1 robuste vers un état moins protecteur.
Ce que cela implique pour les traitements futurs
Pour les personnes vivant avec la MPOC, ces résultats offrent une nouvelle manière d’expliquer pourquoi la maladie devient plus difficile à maîtriser avec le temps. L’étude suggère que, dans la MPOC avancée, les cellules endothéliales vieillissantes des vaisseaux pulmonaires agissent comme des balises de signalisation chroniques, libérant de l’IL6 qui affaiblit un volet clé de la défense immunitaire. Cela pourrait aider à expliquer pourquoi les patients sévèrement atteints sont plus susceptibles d’avoir des infections et des exacerbations fréquentes. Le travail implique aussi que les médicaments ciblant l’IL6 ou les cellules sénescentes pourraient n’être efficaces que s’ils sont adaptés aux patients atteints d’une MPOC avancée, plutôt que d’être appliqués uniformément à tous les stades. En résumé, l’article requalifie la MPOC sévère non seulement comme une inflammation accrue, mais comme un stade marqué par des vaisseaux vieillissants qui désarment silencieusement le système immunitaire.
Citation: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
Mots-clés: MPOC, sénescence endothéliale, signalisation IL6, immunité T, maladie pulmonaire chronique