Clear Sky Science · pt
A senescência de células endoteliais molda a atividade de células T em estágios avançados da doença pulmonar obstrutiva crônica
Por que isso importa para pessoas com doença pulmonar
A doença pulmonar obstrutiva crônica (DPOC) é uma importante causa de falta de ar, internações e morte prematura no mundo todo, entretanto os tratamentos atuais aliviam sobretudo os sintomas em vez de deter a progressão da doença. Este estudo faz uma pergunta mais profunda: o que realmente muda dentro dos pulmões quando a DPOC evolui de leve para grave? Ao combinar grandes dados de biobancos, análises de ponta em célula única e aprendizado de máquina, os autores revelam uma interação oculta entre o envelhecimento dos vasos sanguíneos pulmonares e as células imunes que deveriam nos proteger de infecções.
Como os pesquisadores procuraram sinais de alerta no sangue
Para encontrar moléculas ligadas à gravidade da DPOC, a equipe começou com amostras de sangue de dezenas de milhares de pessoas no UK Biobank. Usando aprendizado de máquina, compararam padrões de proteínas em pessoas sem DPOC, com a doença e com diferentes níveis de função pulmonar. Essa abordagem destacou um pequeno grupo de proteínas cujos níveis aumentavam conforme a DPOC surgia e piorava. Duas, em particular, IL6 e MMP12, sobressaíram: níveis mais altos estavam associados não apenas à presença de DPOC, mas também a doença mais severa e pior sobrevida ao longo do tempo. Entre elas, a IL6 emergiu como o sinal mais específico de estágio quando os pesquisadores depois olharam diretamente o tecido pulmonar.
O que viram dentro de pulmões danificados
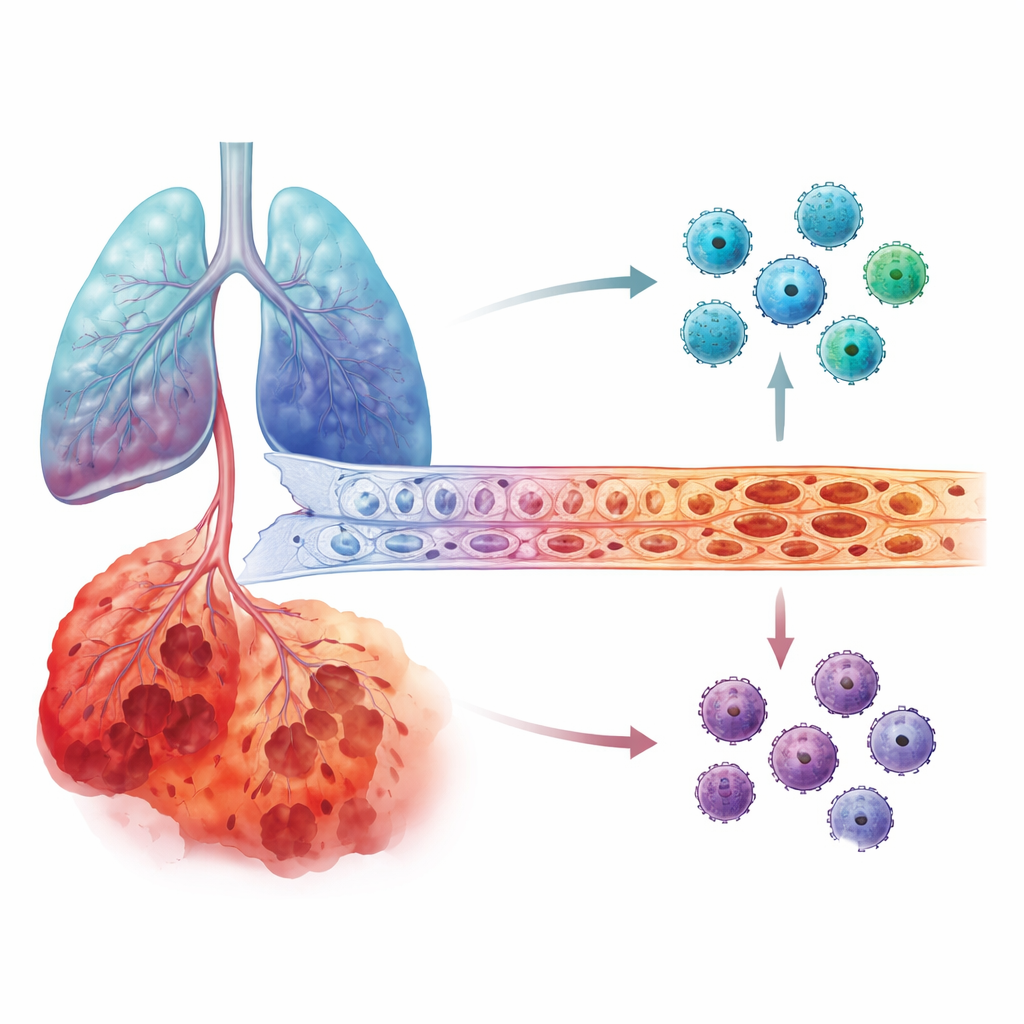
Os investigadores seguiram para conjuntos de dados de tecido pulmonar, incluindo tanto medidas em larga escala da atividade gênica quanto sequenciamento de RNA em célula única, que permite rastrear o que cada tipo celular está fazendo. Eles descobriram que a atividade do gene IL6 era claramente maior em pulmões com DPOC do que em pulmões saudáveis. Mais notavelmente, nos casos mais graves, a IL6 estava concentrada nas células que revestem os vasos sanguíneos pulmonares, conhecidas como células endoteliais, além de em células dos delicados alvéolos. Em contraste, a MMP12 não mostrou um salto tão específico por estágio. Em várias coortes independentes de pacientes, o mesmo padrão emergiu: conforme a DPOC avançava, as células endoteliais em pulmões em estágio terminal tornavam-se uma fonte dominante de IL6.
Quando as células dos vasos sanguíneos envelhecem e ficam inquietas
Aprofundando, a equipe perguntou por que as células endoteliais na DPOC grave produzem tanto IL6. Seus padrões gênicos mostravam marcas de senescência celular — uma forma de parada permanente do crescimento frequentemente descrita como células “envelhecidas” ou “gastas”. Essas células expressavam genes clássicos de senescência, ativavam chaves regulatórias associadas à senescência e produziam um coquetel de moléculas inflamatórias conhecido como fenótipo secretório associado à senescência. Transcriptômica espacial, que preserva a localização das células em fatias reais de pulmão, mostrou que células endoteliais ricas em marcadores de senescência também liberavam mais IL6. Sangue de pacientes com DPOC grave igualmente carregava assinaturas proteicas mais fortes relacionadas à senescência, sugerindo que esse processo de envelhecimento não é apenas local, mas refletido por todo o organismo.
Como vasos envelhecidos remodelam as defesas imunes
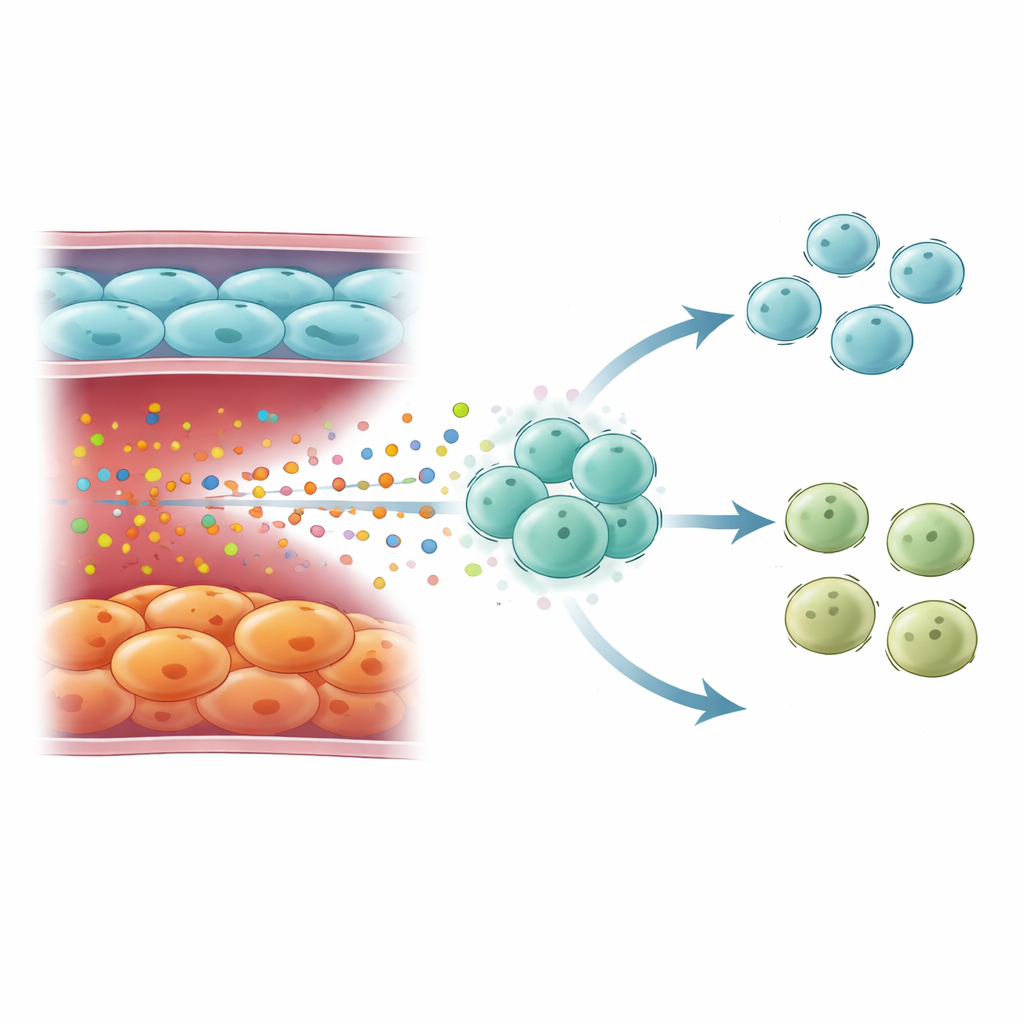
A elevada IL6 oriunda de células endoteliais senescentes não atuou isoladamente. Mapas de célula única das células imunes revelaram que esses sinais eram direcionados principalmente a células T naïve, os versáteis leucócitos que podem se diferenciar em vários subtipos auxiliares. Na DPOC grave, as populações de células T mudaram: células T CD4 naïve se acumularam, enquanto células T helper do tipo 1 (Th1) — importantes no combate a vírus e bactérias por meio da citocina interferon-gama — foram reduzidas. Assinaturas gênicas de respostas ao interferon-gama caíram na doença grave, mesmo que pudessem ser mais altas na DPOC quando estáveis em estágios leves e moderados. Células T em DPOC avançada mostraram forte ativação de vias responsivas à IL6 e de STAT3, consistente com a exposição prolongada à IL6 direcionando-as para longe de um destino robusto Th1 e em direção a um estado menos protetor.
O que isso significa para tratamentos futuros
Para pessoas que vivem com DPOC, essas descobertas oferecem uma nova forma de entender por que a doença se torna mais difícil de controlar com o tempo. O estudo sugere que, na DPOC em estágio avançado, células endoteliais envelhecidas nos vasos pulmonares agem como faróis de sinalização crônica, liberando IL6 que suprime um braço chave da defesa imune. Isso pode ajudar a explicar por que pacientes com doença grave são mais suscetíveis a infecções e exacerbações frequentes. O trabalho também implica que fármacos que miram IL6 ou células senescentes podem ser eficazes apenas se direcionados a indivíduos com DPOC avançada, em vez de aplicados uniformemente em todos os estágios. Em suma, o artigo reposiciona a DPOC grave não apenas como inflamação crescente, mas como um estágio marcado por vasos sanguíneos envelhecidos que silenciosamente desarmam o sistema imune.
Citação: Lee, C.M., Kim, J., Song, J. et al. Endothelial cell senescence shapes T cell activity in late-stage of chronic obstructive pulmonary disease. Cell Death Discov. 12, 160 (2026). https://doi.org/10.1038/s41420-026-03020-2
Palavras-chave: DPOC, senescência endotelial, sinalização IL6, imunidade de células T, doença pulmonar crônica