Clear Sky Science · zh
子宫内膜异位症中的可变剪接失调:异常mRNA变体在异位细胞生长中的作用
隐匿的基因信息为何与女性健康相关
子宫内膜异位症约影响十位育龄女性中的一位,但诊断常需数年,且可导致剧烈疼痛和不孕。本研究探查疾病表象之下的一层微妙基因调控——RNA 剪接,即细胞在将基因信息翻译为蛋白质前如何编辑这些信息。通过揭示这种编辑过程在子宫内膜异位症中如何出错,研究者发现了病灶生长的隐性驱动因素,并指出了未来可能用于检测和治疗该病的新方向。
组织在不该出现的地方生长
在子宫内膜异位症中,类似子宫内膜的组织出现在卵巢、盆腔壁及其他邻近器官上。这些错位的斑块或病灶会对激素产生反应,引发炎症,并能侵袭周围组织,导致慢性疼痛和生育问题。但并非所有月经回流入盆腔的人都会发展为子宫内膜异位症,这提示细胞内部还存在额外的分子变化,决定谁会得病以及病情严重程度。科学家们已列出许多在异位病灶中总体活性改变的基因,但缺少的是对这些基因信息在细胞内被使用前如何被编辑的更细致观察。
编辑基因信息:关键的额外步骤
基因首先被转录为长链 RNA,这些 RNA 必须被切割并重新连接——这一过程称为剪接——才能作为构建蛋白质的指令。细胞可以以不同方式剪接同一基因,产生功能各异的多种蛋白质版本。这种灵活性让组织能够微调自身行为,但也带来了出错的机会。作者分析了来自卵巢型和腹膜型子宫内膜异位症患者及未患病女性的 RNA 测序数据。借助强大的计算工具,他们检视了五类主要的剪接事件,发现病灶与健康子宫内膜在基因信息编辑上存在数百处差异。其中两类变化尤为突出:外显子跳跃(跳过了重要片段)和内含子滞留(应被去除的额外序列被错误保留在信息中)。
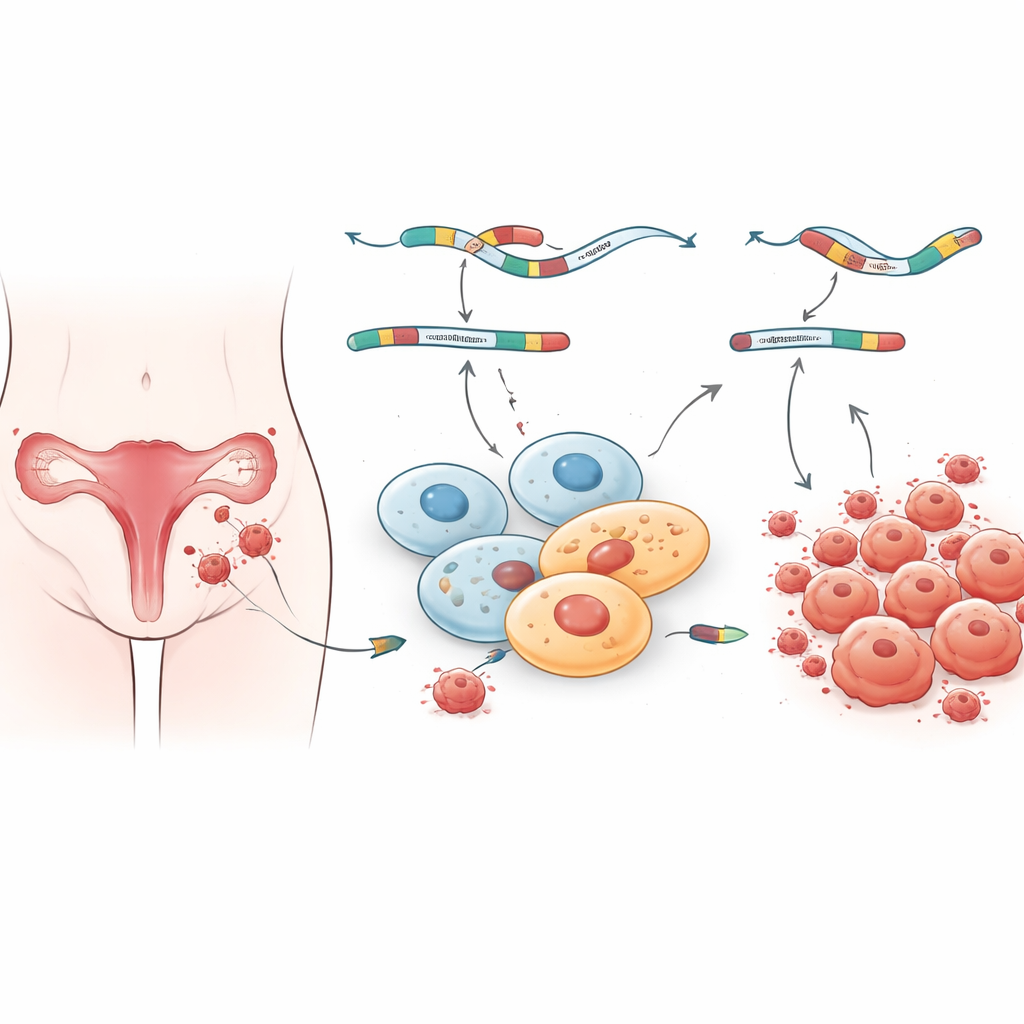
不同病灶部位的独特分子指纹
研究团队接着探问哪些类型的基因更易受这些异常编辑模式影响。富集分析显示,病灶中的总体基因活性以及异常剪接都集中在与蛋白结合、细胞信号传导和细胞周围结构支架相关的通路上。这些通路控制细胞如何感知环境、彼此黏附以及对激素和炎性信号的响应——这些过程在子宫内膜异位症中已知会被破坏。有趣的是,卵巢型和腹膜型病灶共享某些剪接改变,但也各自拥有许多独特变化,表明不同部位的病灶带有不同的分子指纹。这或可解释为何患者即便在显微镜下病变相似,症状模式和治疗反应也可能大相径庭。
两种抑制增殖的保护基因
为将模式与机制联系起来,研究者聚焦于两种基因 GALNT7 和 ZNF28,其 RNA 信息在病灶中持续出现关键片段缺失。使用体外培养的人子宫内膜上皮细胞,他们实验性降低了这两基因的表达或去除了患者中被跳过的特定外显子。在两种情形下,细胞增殖加快并随时间形成更多集落,类似子宫内膜异位组织中观察到的失控生长。额外的单细胞数据表明,在健康组织中,这些基因在上皮细胞中特别活跃——正是构成内膜病灶腺体的细胞——但在病灶中其表达明显下降。综合结果提示,正常剪接的 GALNT7 和 ZNF28 通常充当抑制细胞生长的刹车,而其 RNA 被错误编辑会削弱这些制动机制。
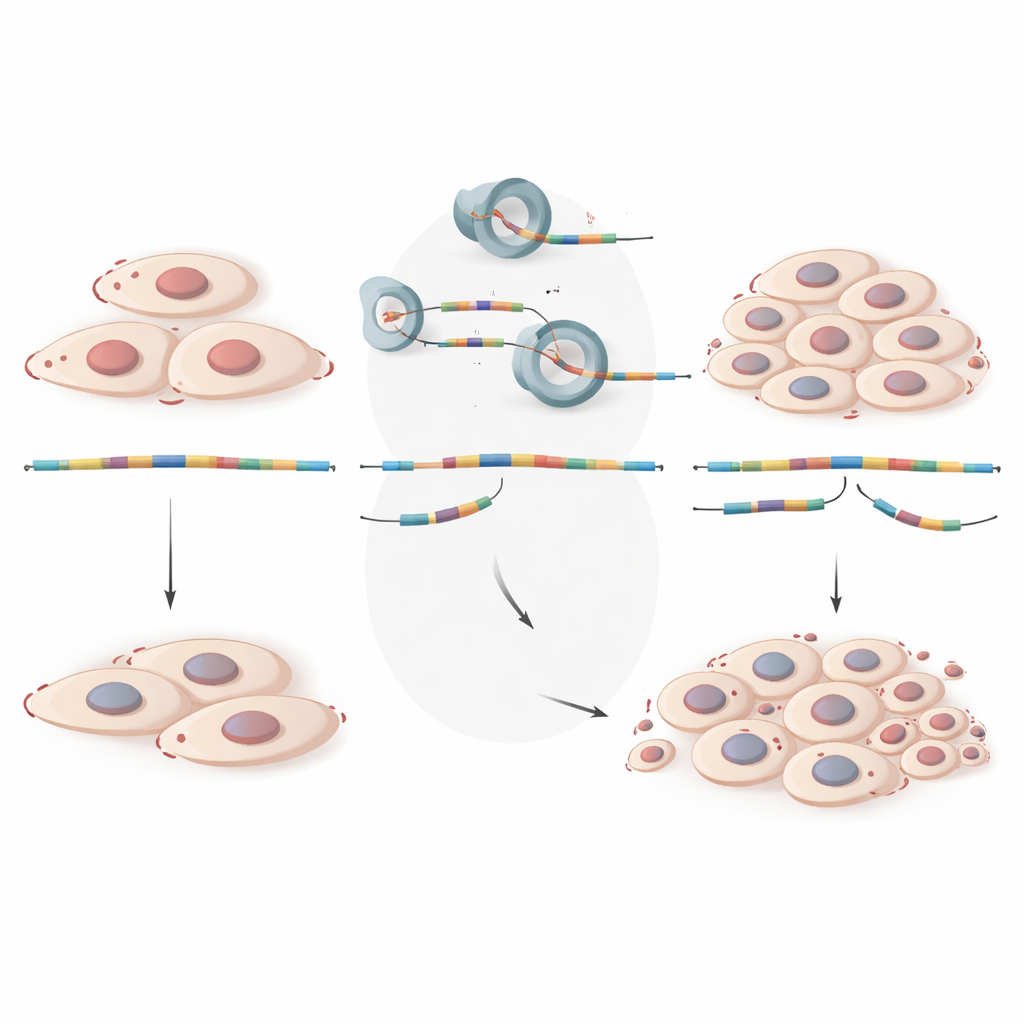
从被错误编辑的信息到增长的病灶
通过非技术性的视角来看,这项工作表明子宫内膜异位症不仅仅是组织生长在错误位置;还涉及细胞使用扭曲的遗传指令。当细胞的编辑机器错误地处理某些 RNA 信息时,像 GALNT7 和 ZNF28 这样的生长控制基因会被实质性地关闭,使病灶中的细胞更易增殖。通过描绘这层被错误调控的剪接,研究提出了新的分子标志,未来有望帮助更早诊断并识别高风险女性。研究也暗示,未来的治疗或许不仅通过阻断激素或外科切除组织来发挥作用,还可能通过校正或绕过有缺陷的 RNA 编辑以恢复细胞的天然生长控制。
引用: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
关键词: 子宫内膜异位症, 可变剪接, RNA 调控, 细胞增殖, 女性健康