Clear Sky Science · fr
Épissage alternatif dérégulé dans l’endométriose : un rôle des variants d’ARNm aberrants dans la croissance des cellules endométriosiques
Pourquoi les messages génétiques cachés comptent pour la santé des femmes
L’endométriose touche environ une femme sur dix en âge de procréer, mais le diagnostic prend souvent des années et la maladie peut provoquer des douleurs invalidantes et de l’infertilité. Cette étude explore un niveau subtil de contrôle génétique appelé épissage de l’ARN — la façon dont les cellules modifient leurs messages génétiques avant de les traduire en protéines. En révélant comment ce processus d’édition se dérègle dans l’endométriose, les chercheurs mettent au jour un moteur caché de la croissance des lésions et ouvrent la voie à de nouvelles approches pour dépister et, potentiellement, traiter la maladie à l’avenir.
Quand le tissu se développe là où il ne devrait pas
Dans l’endométriose, des tissus ressemblant à la muqueuse utérine apparaissent sur les ovaires, la paroi pelvienne et d’autres organes voisins. Ces foyers anormaux, ou lésions, répondent aux hormones, déclenchent une inflammation et peuvent envahir les tissus environnants, entraînant des douleurs chroniques et des problèmes de fertilité. Mais toutes les personnes ayant un reflux menstruel vers le bassin ne développent pas d’endométriose, ce qui suggère que des changements moléculaires supplémentaires à l’intérieur des cellules influencent qui développera la maladie et son degré de gravité. Les scientifiques ont déjà catalogué de nombreux gènes dont l’activité globale est modifiée dans les lésions endométriosiques. Ce qui manquait, c’était un examen plus détaillé de la façon dont ces messages génétiques sont édités à l’intérieur des cellules avant d’être utilisés.
Éditer les messages génétiques : une étape supplémentaire cruciale
Les gènes sont d’abord copiés en longues molécules d’ARN qui doivent être découpées et recollées — un processus appelé épissage — avant de servir d’instructions pour fabriquer des protéines. Les cellules peuvent épisser un même gène de différentes manières, créant plusieurs variantes d’une protéine aux fonctions distinctes. Cette flexibilité permet aux tissus d’ajuster finement leur comportement, mais elle ouvre aussi la porte aux erreurs. Les auteurs ont analysé des données de séquençage d’ARN provenant de femmes atteintes d’endométriose ovarienne et péritonéale et de femmes sans la maladie. À l’aide d’outils informatiques puissants, ils ont examiné cinq grands types d’événements d’épissage et trouvé des centaines de différences dans la manière dont les messages génétiques sont édités dans les lésions par rapport à la muqueuse utérine saine. Deux types de changements ressortent particulièrement : les exons sautés, où un segment important est omis, et les introns retenus, où du matériel supplémentaire qui devrait être éliminé est conservé par erreur dans le message.
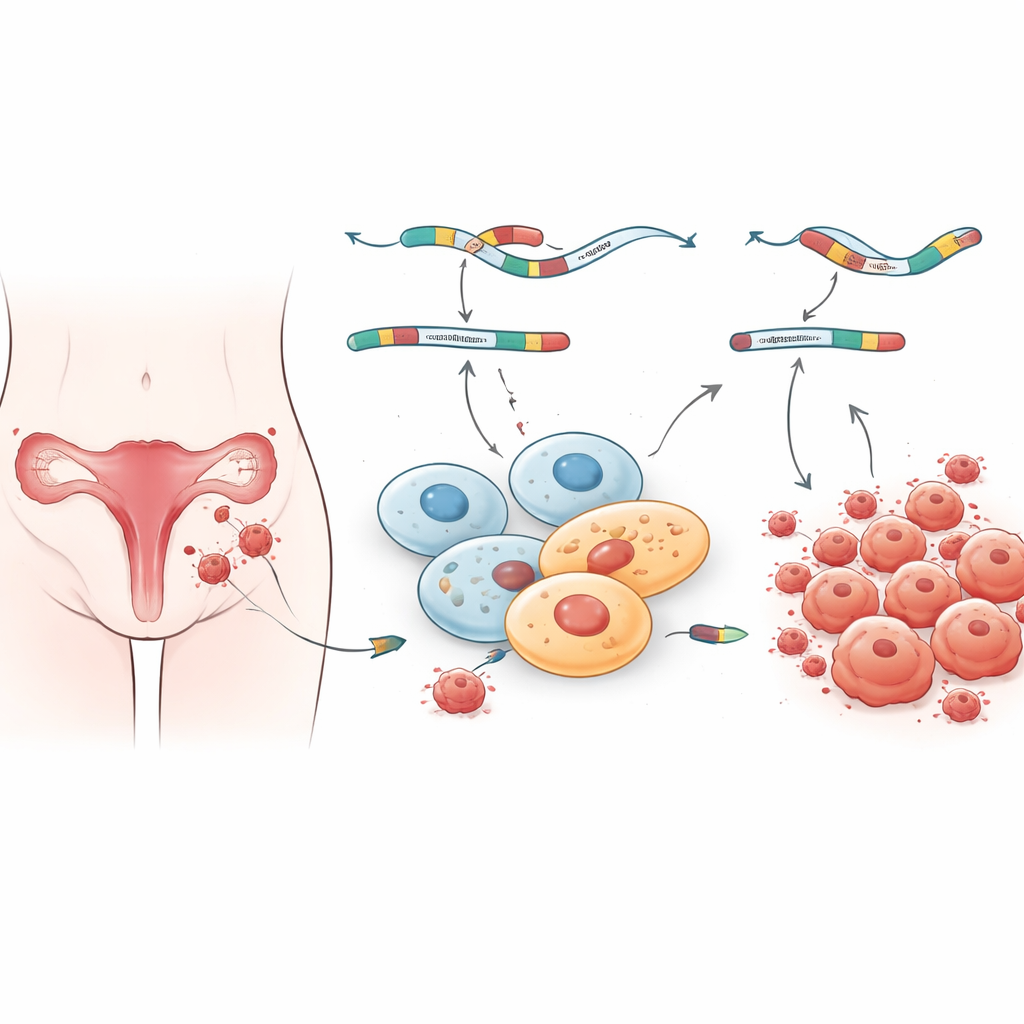
Empreintes moléculaires distinctes selon le site des lésions
L’équipe s’est ensuite demandé quels types de gènes étaient les plus affectés par ces schémas d’édition altérés. Leur analyse d’enrichissement montre que l’activité génique globale et l’épissage anormal dans les lésions se regroupent dans des voies liées à la liaison protéine-protéine, à la signalisation cellulaire et au réseau structural entourant les cellules. Ces voies contribuent à contrôler la façon dont les cellules perçoivent leur environnement, adhèrent les unes aux autres et répondent aux hormones et aux signaux inflammatoires — des processus connus pour être perturbés dans l’endométriose. Fait intéressant, les lésions ovariennes et péritonéales partagent certaines modifications d’épissage mais présentent aussi de nombreuses différences spécifiques, ce qui suggère que les lésions selon leur localisation portent des empreintes moléculaires distinctes. Cela peut expliquer pourquoi les patientes présentent des profils de symptômes et des réponses aux traitements très variés, même lorsque la maladie semble similaire au microscope.
Deux gènes protecteurs qui freinent la croissance
Pour aller des schémas aux mécanismes, les chercheurs se sont concentrés sur deux gènes, GALNT7 et ZNF28, dont les messages ARN montraient une perte constante de segments clés dans les lésions. En utilisant des cellules épithéliales endométriales humaines cultivées en laboratoire, ils ont réduit expérimentalement le niveau de ces gènes ou supprimé les exons spécifiques sautés chez les patientes. Dans les deux cas, les cellules ont commencé à se multiplier plus rapidement et ont formé davantage de colonies au fil du temps, reproduisant la croissance non contrôlée observée dans le tissu endométriosique. Des données complémentaires en simple cellule ont montré que dans le tissu sain, ces gènes sont particulièrement actifs dans les cellules épithéliales — les mêmes cellules qui composent les glandes des lésions endométriosiques — mais leur expression chute nettement dans les lésions. Ensemble, ces résultats suggèrent que GALNT7 et ZNF28 correctement épissés jouent normalement le rôle de freins à la croissance cellulaire, et que l’édition défectueuse de leurs ARN affaiblit ces freins.
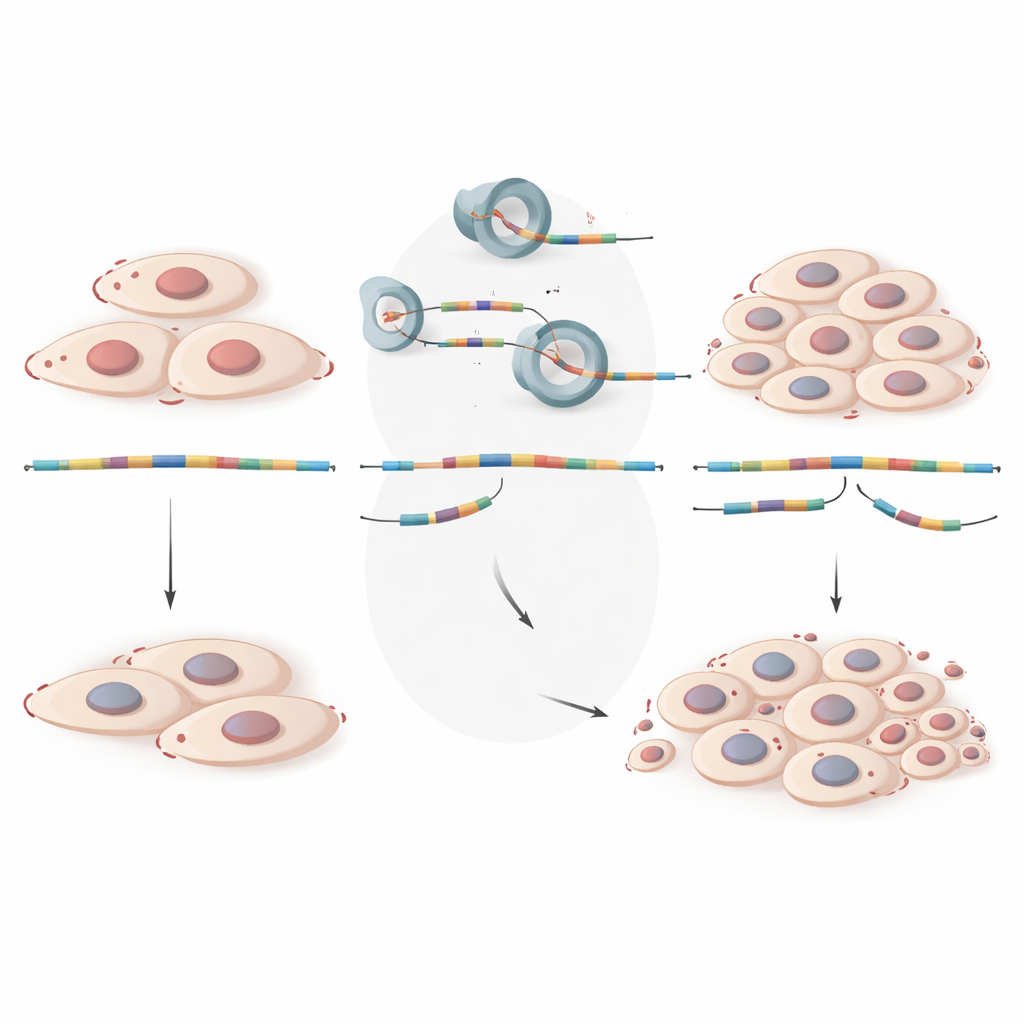
Des messages mal édités aux lésions en croissance
D’un point de vue non technique, ce travail montre que l’endométriose ne se résume pas au simple développement de tissu au mauvais endroit ; il s’agit aussi de cellules qui utilisent des instructions génétiques déformées. Lorsque la machinerie d’édition cellulaire maltraite certains messages ARN, des gènes qui contrôlent la croissance comme GALNT7 et ZNF28 voient leur activité réduite, permettant aux cellules des lésions de se multiplier plus facilement. En cartographiant cette couche cachée d’épissage dérégulé, l’étude met en lumière de nouveaux profils moléculaires qui pourraient, à terme, aider à un diagnostic plus précoce et à l’identification des femmes à risque accru. Elle soulève aussi la possibilité que des thérapies futures n’agissent pas seulement en bloquant les hormones ou en retirant les tissus chirurgicalement, mais en corrigeant ou en contournant l’épissage défectueux de l’ARN pour rétablir les contrôles naturels de la croissance cellulaire.
Citation: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
Mots-clés: endométriose, épissage alternatif, régulation de l’ARN, prolifération cellulaire, santé des femmes