Clear Sky Science · de
Fehlreguliertes alternatives Spleißen bei Endometriose: eine Rolle aberranter mRNA-Varianten beim Wachstum endometriotischer Zellen
Warum versteckte Genbotschaften für die Gesundheit von Frauen wichtig sind
Endometriose betrifft etwa eine von zehn Frauen im gebärfähigen Alter, wird jedoch oft erst nach Jahren diagnostiziert und kann starke Schmerzen sowie Unfruchtbarkeit verursachen. Diese Studie blickt unter die Oberfläche der Erkrankung auf eine subtile Ebene genetischer Kontrolle namens RNA-Spleißen — wie Zellen ihre Genbotschaften vor der Proteinbildung bearbeiten. Indem die Forschenden zeigen, wie dieser Bearbeitungsprozess bei Endometriose fehlreguliert ist, offenbaren sie einen verborgenen Treiber des Läsionswachstums und weisen auf neue Möglichkeiten hin, die Krankheit künftig zu erkennen und möglicherweise zu behandeln.
Wenn Gewebe wächst, wo es nicht hingehört
Bei Endometriose findet sich Gewebe, das der Gebärmutterschleimhaut ähnelt, an Eierstöcken, an der Beckenwand und anderen benachbarten Organen. Diese fehlplatzierten Herde oder Läsionen reagieren auf Hormone, lösen Entzündungen aus und können in umliegendes Gewebe eindringen, was zu chronischen Schmerzen und Fruchtbarkeitsstörungen führt. Nicht jede Frau mit Rückfluss von Menstruationsblut ins Becken entwickelt jedoch Endometriose, was darauf hindeutet, dass zusätzliche molekulare Veränderungen in den Zellen mitbestimmen, wer die Krankheit bekommt und wie schwer sie verläuft. Forschende haben bereits viele Gene katalogisiert, deren Gesamtexpression in endometriotischen Läsionen verändert ist. Was bislang fehlte, ist ein genauerer Blick darauf, wie diese Genbotschaften in den Zellen vor ihrer Verwendung bearbeitet werden.
Genbotschaften bearbeiten: ein wichtiger zusätzlicher Schritt
Gene werden zunächst in lange RNA-Stränge abgeschrieben, die vor ihrer Nutzung als Bauanleitung für Proteine zugeschnitten und wieder zusammengefügt werden müssen — ein Prozess, der als Spleißen bekannt ist. Zellen können dasselbe Gen auf unterschiedliche Weise spleißen und so mehrere Versionen eines Proteins mit verschiedenen Funktionen erzeugen. Diese Flexibilität erlaubt es Geweben, ihr Verhalten fein zu steuern, eröffnet aber auch Fehlerquellen. Die Autorinnen und Autoren analysierten RNA-Sequenzierungsdaten von Frauen mit ovarieller und peritonealer Endometriose sowie von Frauen ohne die Erkrankung. Mit leistungsfähigen Rechenwerkzeugen untersuchten sie fünf Haupttypen von Spleißereignissen und fanden Hunderte von Unterschieden in der Bearbeitung von Genbotschaften in Läsionen im Vergleich zur gesunden Gebärmutterschleimhaut. Zwei Arten von Veränderungen hoben sich besonders hervor: ausgelassene Exons, bei denen ein wichtiger Abschnitt fehlt, und zurückbehaltene Introns, bei denen Material, das entfernt werden sollte, fälschlicherweise in der Botschaft verbleibt.
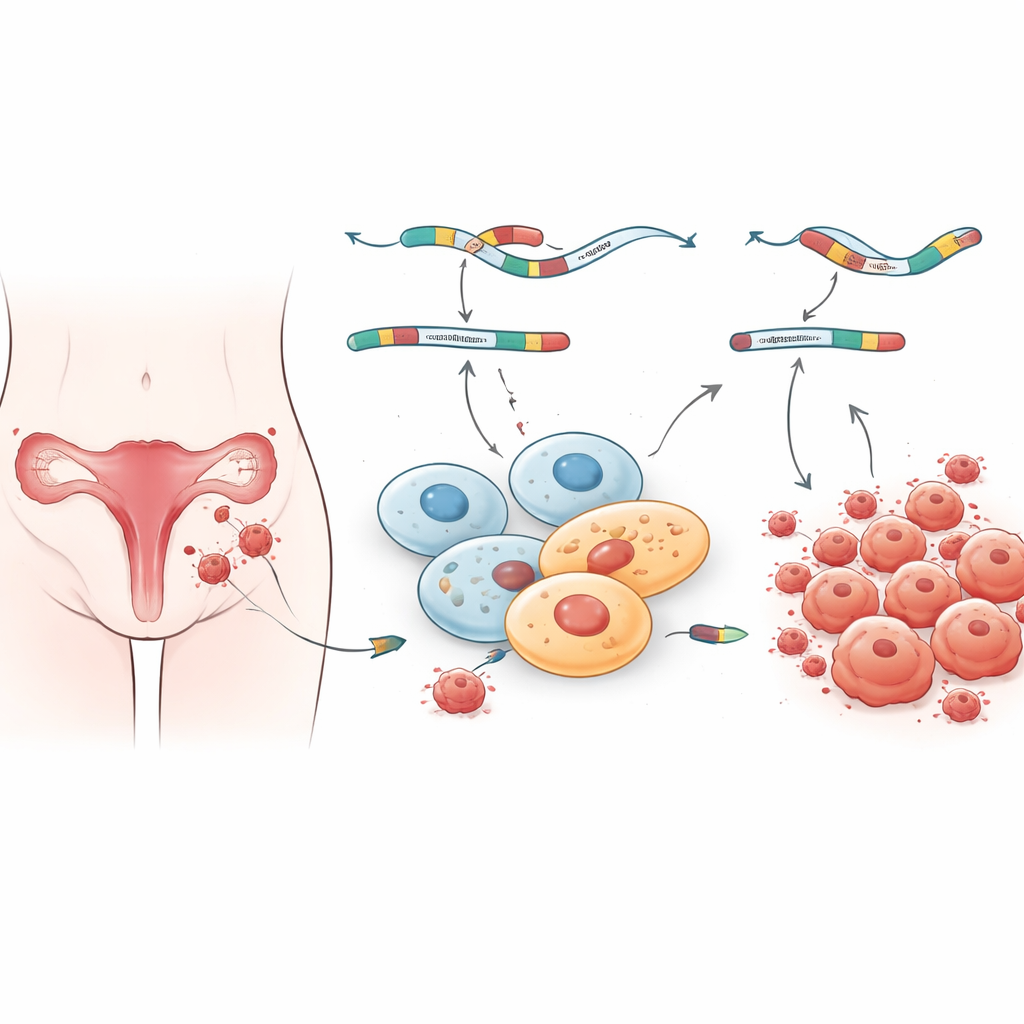
Unterschiedliche molekulare Fingerabdrücke an verschiedenen Läsionsorten
Das Team untersuchte anschließend, welche Arten von Genen am stärksten von diesen veränderten Bearbeitungsmustern betroffen waren. Ihre Anreicherungsanalyse zeigte, dass sowohl die Gesamtexpression von Genen als auch das abnorme Spleißen in Läsionen sich in Signalwegen bündelten, die mit Proteinbindung, Zellkommunikation und dem strukturellen Gerüst um Zellen herum zusammenhängen. Diese Wege steuern, wie Zellen ihre Umgebung wahrnehmen, aneinander haften und auf hormonelle sowie entzündliche Signale reagieren — Prozesse, die bei Endometriose bekanntlich gestört sind. Interessanterweise teilten ovariellen und peritonealen Läsionen einige Spleißveränderungen, zeigten aber auch viele unterschiedliche, was darauf hindeutet, dass Läsionen an verschiedenen Orten eigene molekulare Fingerabdrücke tragen. Das kann erklären, warum Patientinnen sehr unterschiedliche Symptomverläufe und Therapieansprechen haben, selbst wenn die Erkrankung histologisch ähnlich aussieht.
Zwei schützende Gene, die das Wachstum bremsen
Um von Mustern zu Mechanismen vorzudringen, konzentrierten sich die Forschenden auf zwei Gene, GALNT7 und ZNF28, deren RNA-Botschaften in Läsionen konsistent den Verlust wichtiger Segmente zeigten. In kultivierten menschlichen endometrialen Epithelzellen reduzierten sie experimentell die Spiegel dieser Gene oder entfernten gezielt die Exons, die bei Patientinnen ausgelassen wurden. In beiden Fällen begannen die Zellen schneller zu proliferieren und bildeten über die Zeit mehr Kolonien — ein Verhalten, das dem unkontrollierten Wachstum in endometriotischem Gewebe ähnelt. Zusätzliche Einzelzell-Daten zeigten, dass diese Gene im gesunden Gewebe besonders in epithelialen Zellen aktiv sind — genau den Zellen, die die Drüsen in endometrialen Läsionen bilden —, in Läsionen aber stark herunterreguliert sind. Zusammengenommen deuten diese Ergebnisse darauf hin, dass korrekt gespleißtes GALNT7 und ZNF28 normalerweise als Bremsen für das Zellwachstum wirken und dass fehlerhafte RNA-Bearbeitung diese Bremsen schwächt.
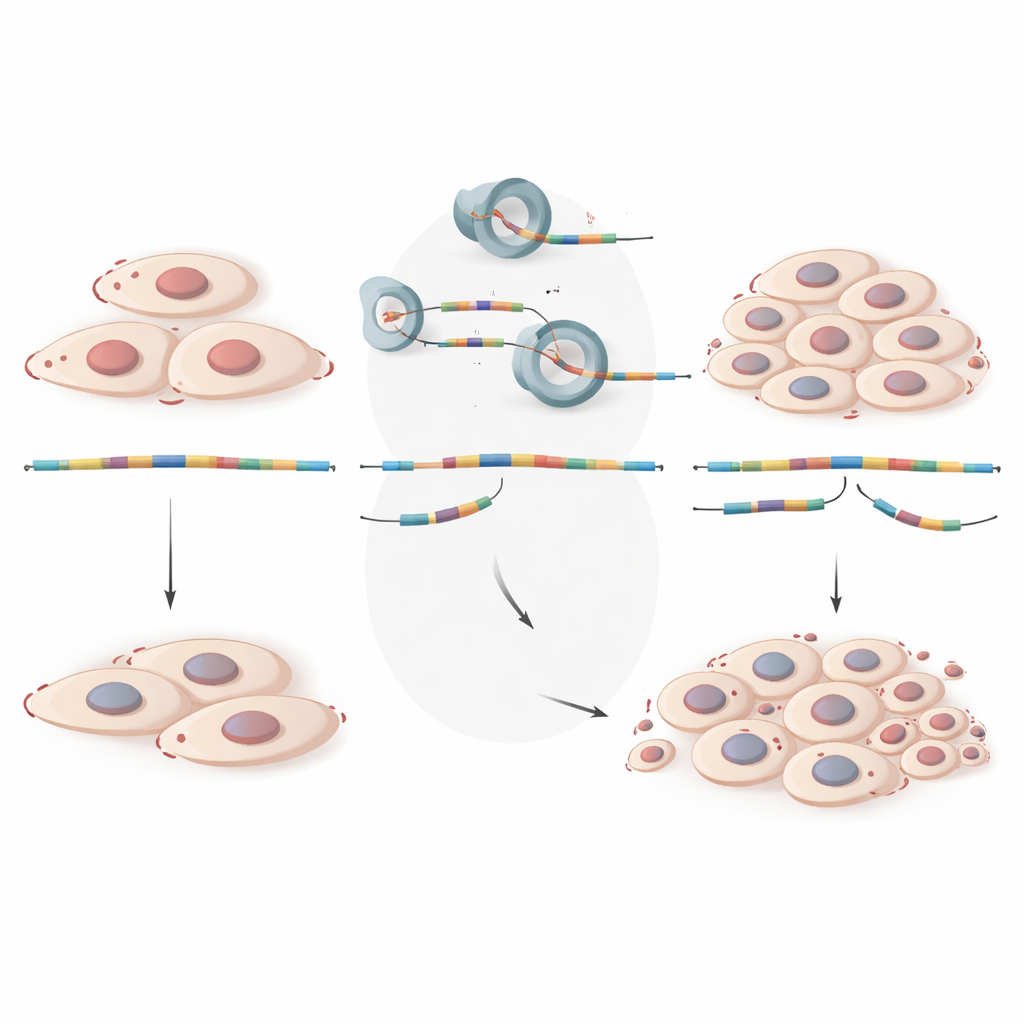
Von fehlbearbeiteten Botschaften zu wachsenden Läsionen
Aus einer nicht-technischen Perspektive zeigt diese Arbeit, dass Endometriose nicht nur dadurch gekennzeichnet ist, dass Gewebe am falschen Ort wächst; es geht auch darum, dass Zellen verzerrte genetische Anweisungen nutzen. Wenn die zelluläre Bearbeitungsmaschinerie bestimmte RNA-Botschaften fehlerhaft verarbeitet, werden wachstumskontrollierende Gene wie GALNT7 und ZNF28 effektiv herunterreguliert, sodass Zellen in Läsionen leichter proliferieren. Durch die Kartierung dieser verborgenen Ebene fehlregulierten Spleißens hebt die Studie neue molekulare Signaturen hervor, die langfristig zu früherer Diagnose und zur Identifizierung von Frauen mit erhöhtem Risiko beitragen könnten. Sie eröffnet auch die Möglichkeit, dass künftige Therapien nicht nur Hormone blockieren oder Gewebe chirurgisch entfernen, sondern fehlerhafte RNA-Bearbeitung korrigieren oder umgehen könnten, um die natürlichen Wachstumsbremsen der Zelle wiederherzustellen.
Zitation: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
Schlüsselwörter: Endometriose, alternatives Spleißen, RNA-Regulation, Zellproliferation, Frauenheilkunde