Clear Sky Science · nl
Verstoorde alternatieve splicing bij endometriose: een rol voor abnormale mRNA-varianten in de groei van endometriotische cellen
Waarom verborgen genboodschappen belangrijk zijn voor de gezondheid van vrouwen
Endometriose treft ongeveer één op de tien vrouwen in de reproductieve leeftijd, maar de diagnose duurt vaak jaren en de aandoening kan invaliderende pijn en onvruchtbaarheid veroorzaken. Deze studie kijkt onder het oppervlak van de ziekte naar een subtiele laag van genetische controle die RNA-splicing wordt genoemd — hoe cellen hun genboodschappen bewerken voordat ze worden omgezet in eiwitten. Door bloot te leggen hoe dit bewerkingsproces verstoord raakt bij endometriose, laten de onderzoekers een verborgen drijfveer van laesiegroei zien en wijzen ze op nieuwe manieren om de ziekte in de toekomst mogelijk te detecteren en te behandelen.
Wanneer weefsel groeit waar het niet hoort
Bij endometriose verschijnt weefsel dat lijkt op het baarmoederslijmvlies op de eierstokken, de bekkenwand en andere nabijgelegen organen. Deze verplaatste plekken, of laesies, reageren op hormonen, veroorzaken ontsteking en kunnen omliggend weefsel binnendringen, wat leidt tot chronische pijn en vruchtbaarheidsproblemen. Maar niet iedereen met menstrale terugvloeiing in het bekken ontwikkelt endometriose, wat suggereert dat extra moleculaire veranderingen binnen cellen meebepalen wie de ziekte krijgt en hoe ernstig die wordt. Wetenschappers hebben al veel genen in kaart gebracht waarvan de totale activiteit verandert in endometriotische laesies. Wat ontbrak, was een nauwkeuriger blik op hoe die genboodschappen in de cellen worden bewerkt voordat ze worden gebruikt.
Genboodschappen bewerken: een cruciale extra stap
Genen worden eerst gekopieerd naar lange RNA-strengen die moeten worden geknipt en weer aan elkaar gezet — een proces dat splicing wordt genoemd — voordat ze als instructies voor het bouwen van eiwitten kunnen dienen. Cellen kunnen hetzelfde gen op verschillende manieren splicen, waardoor meerdere versies van een eiwit met uiteenlopende functies ontstaan. Deze flexibiliteit stelt weefsels in staat hun gedrag fijn af te stemmen, maar creëert ook kansen voor fouten. De auteurs analyseerden RNA-sequencinggegevens van vrouwen met ovarium- en peritoneale endometriose en van vrouwen zonder de ziekte. Met krachtige computationele hulpmiddelen onderzochten ze vijf belangrijke typen splicingevenementen en vonden honderden verschillen in hoe genboodschappen in laesies worden bewerkt vergeleken met gezond baarmoederslijmvlies. Twee typen veranderingen vielen op: overgeslagen exonen, waarbij een belangrijk segment wordt weggelaten, en behouden introns, waarbij extra materiaal dat verwijderd had moeten worden per ongeluk in het bericht blijft staan.
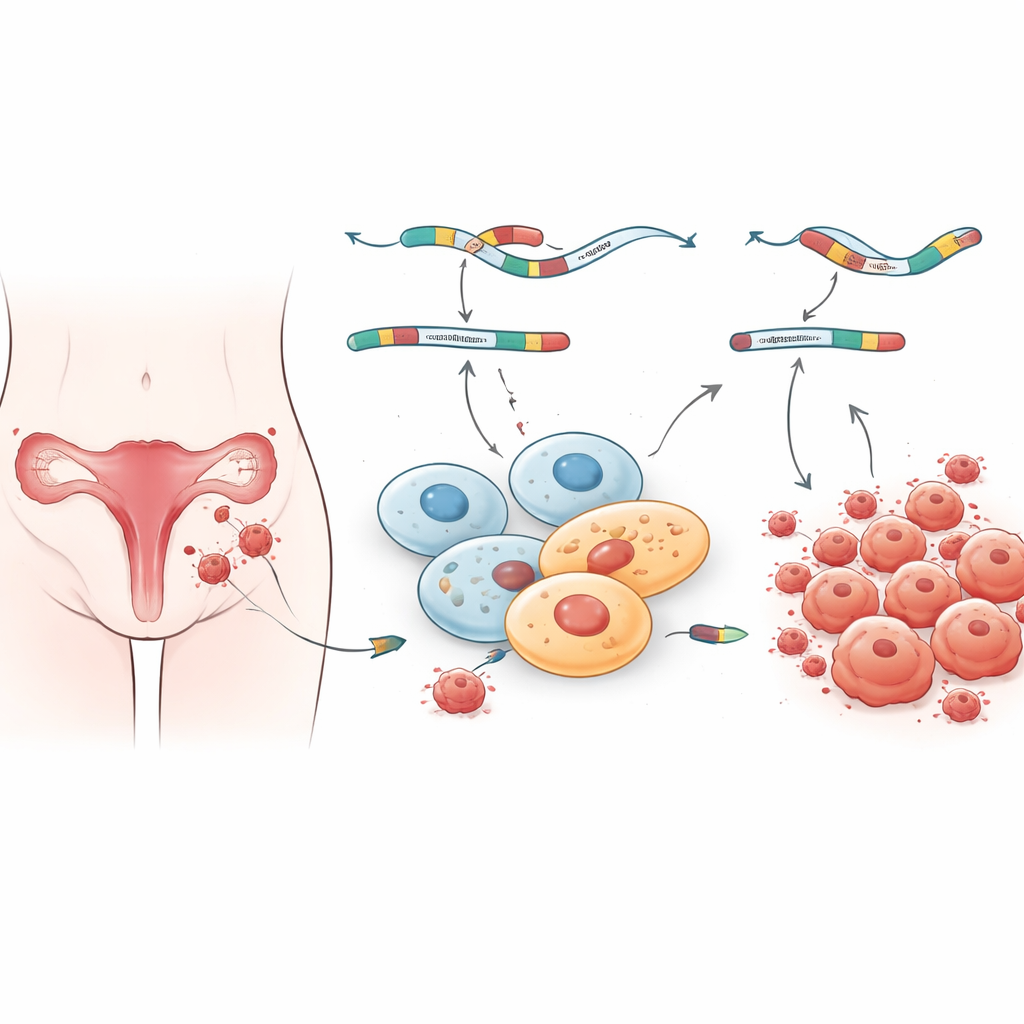
Onderscheidende moleculaire vingerafdrukken in verschillende laesieplaatsen
Het team vroeg vervolgens wat voor soort genen het meest werden getroffen door deze gewijzigde bewerkingspatronen. Hun verrijkingsanalyse toonde aan dat zowel de algemene genactiviteit als de abnormale splicing in laesies clusteren in paden die te maken hebben met eiwitbinding, celsignalering en het structurele geraamte rondom cellen. Deze paden helpen te regelen hoe cellen hun omgeving waarnemen, aan elkaar hechten en reageren op hormonen en ontstekingssignalen — allemaal processen die bekend zijn als verstoord bij endometriose. Interessant is dat ovarium- en peritoneale laesies sommige splicingveranderingen deelden maar ook veel unieke veranderingen vertoonden, wat suggereert dat laesies op verschillende locaties onderscheidende moleculaire vingerafdrukken dragen. Dit kan helpen verklaren waarom patiënten heel verschillende symptomen en behandelreacties kunnen hebben, zelfs wanneer de ziekte onder de microscoop vergelijkbaar lijkt.
Twee beschermende genen die de groei in toom houden
Om van patronen naar mechanismen te gaan, zoomden de onderzoekers in op twee genen, GALNT7 en ZNF28, waarvan de RNA-boodschappen in de laesies consequent verlies van sleutelsegmenten vertoonden. Met in het laboratorium gekweekte humane endometriumepitheelcellen verlaagden ze experimenteel het niveau van deze genen of verwijderden ze de specifieke exonen die bij patiënten werden overgeslagen. In beide gevallen begonnen de cellen sneller te vermenigvuldigen en vormden ze in de loop van de tijd meer kolonies, wat de ongecontroleerde groei nabootst die in endometriotisch weefsel wordt gezien. Aanvullende single-cell gegevens toonden dat deze genen in gezond weefsel vooral actief zijn in epitheelcellen — de cellen die de klieren in endometriumlaesies vormen — maar dat hun expressie sterk afneemt in laesies. Samen suggereren deze resultaten dat goed gesplicte GALNT7 en ZNF28 normaal functioneren als remmen op celdeling, en dat foutieve bewerking van hun RNA die remmen verzwakt.
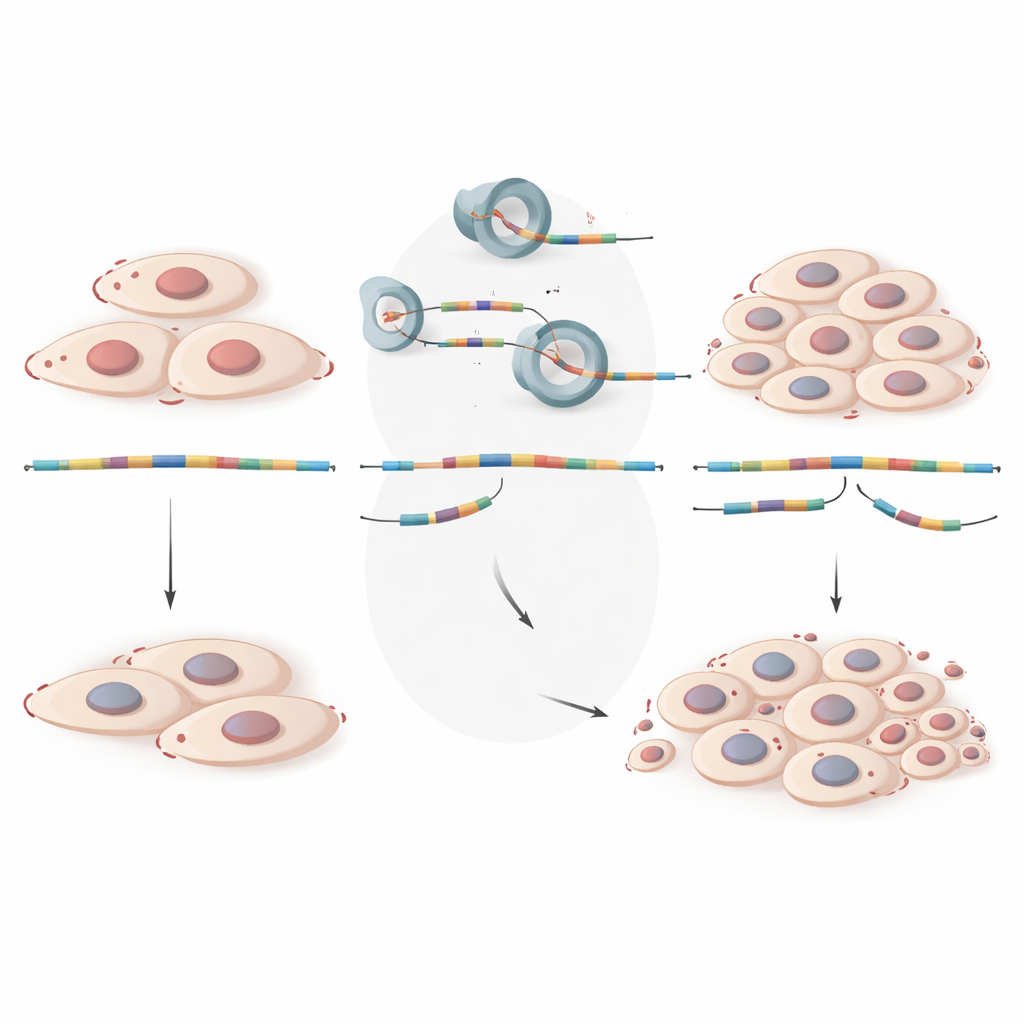
Van verkeerd bewerkte boodschappen naar groeiende laesies
In niet-technische bewoordingen laat dit werk zien dat endometriose niet alleen gaat over weefsel dat op de verkeerde plaats groeit; het gaat ook over cellen die vervormde genetische instructies gebruiken. Wanneer het bewerkingsapparaat van de cel bepaalde RNA-boodschappen fout verwerkt, worden groeiregulerende genen zoals GALNT7 en ZNF28 effectief naar beneden gereguleerd, waardoor cellen in laesies gemakkelijker kunnen vermenigvuldigen. Door deze verborgen laag van verstoorde splicing in kaart te brengen, benadrukt de studie nieuwe moleculaire signaturen die mogelijk in de toekomst kunnen bijdragen aan eerdere diagnose en het identificeren van vrouwen met een hoger risico. Het wekt ook de mogelijkheid dat toekomstige therapieën niet alleen werken door hormonen te blokkeren of weefsel operatief te verwijderen, maar door foutieve RNA-bewerking te corrigeren of te omzeilen om de natuurlijke groeiregelaars van de cel te herstellen.
Bronvermelding: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
Trefwoorden: endometriose, alternatieve splicing, RNA-regulatie, celproliferatie, gezondheid van vrouwen