Clear Sky Science · it
Splicing alternativo regolato in modo anomalo nell’endometriosi: un ruolo per varianti aberranti di mRNA nella crescita delle cellule endometriosiche
Perché i messaggi genetici nascosti contano per la salute delle donne
L’endometriosi colpisce circa una donna su dieci in età riproduttiva, ma spesso la diagnosi impiega anni e la malattia può causare dolore debilitante e infertilità. Questo studio esplora uno strato sottile di controllo genetico chiamato splicing dell’RNA — il modo in cui le cellule modificano i messaggi genici prima di trasformarli in proteine. Scoprendo come questo processo di modifica deragli nell’endometriosi, i ricercatori mettono in luce un motore nascosto della crescita delle lesioni e indicano possibili nuove strade per individuare e, potenzialmente, trattare la malattia in futuro.
Quando il tessuto cresce dove non dovrebbe
Nell’endometriosi, tessuto simile al rivestimento uterino compare sulle ovaie, sulla parete pelvica e su altri organi vicini. Queste aree spostate, o lesioni, rispondono agli ormoni, scatenano infiammazione e possono invadere i tessuti circostanti, provocando dolore cronico e problemi di fertilità. Tuttavia non tutte le persone con reflusso mestruale nella pelvi sviluppano endometriosi, il che suggerisce che cambiamenti molecolari interni alle cellule contribuiscono a determinare chi contrae la malattia e quanto grave essa diventi. Gli scienziati hanno già catalogato molti geni la cui attività complessiva è alterata nelle lesioni endometriosiche. Ciò che mancava era uno sguardo più ravvicinato su come quei messaggi genici vengono modificati all’interno delle cellule prima di essere utilizzati.
Modificare i messaggi genici: un passaggio extra cruciale
I geni vengono prima copiati in lunghi filamenti di RNA che devono essere tagliati e ricollegati — un processo noto come splicing — prima di servire come istruzioni per costruire proteine. Le cellule possono effettuare lo stesso splicing in modi diversi, creando più versioni di una proteina con funzioni distinte. Questa flessibilità permette ai tessuti di modulare il proprio comportamento, ma apre anche la strada a errori. Gli autori hanno analizzato dati di RNA-seq provenienti da donne con endometriosi ovarica e peritoneale e da donne senza la malattia. Usando potenti strumenti computazionali, hanno esaminato cinque tipi principali di eventi di splicing e hanno trovato centinaia di differenze nel modo in cui i messaggi genici vengono modificati nelle lesioni rispetto al rivestimento uterino sano. Due tipi di cambiamento sono emersi in modo preponderante: l’esclusione di esoni, in cui viene omesso un segmento importante, e la ritenzione di introni, in cui materiale in eccesso che dovrebbe essere rimosso rimane per errore nel messaggio.
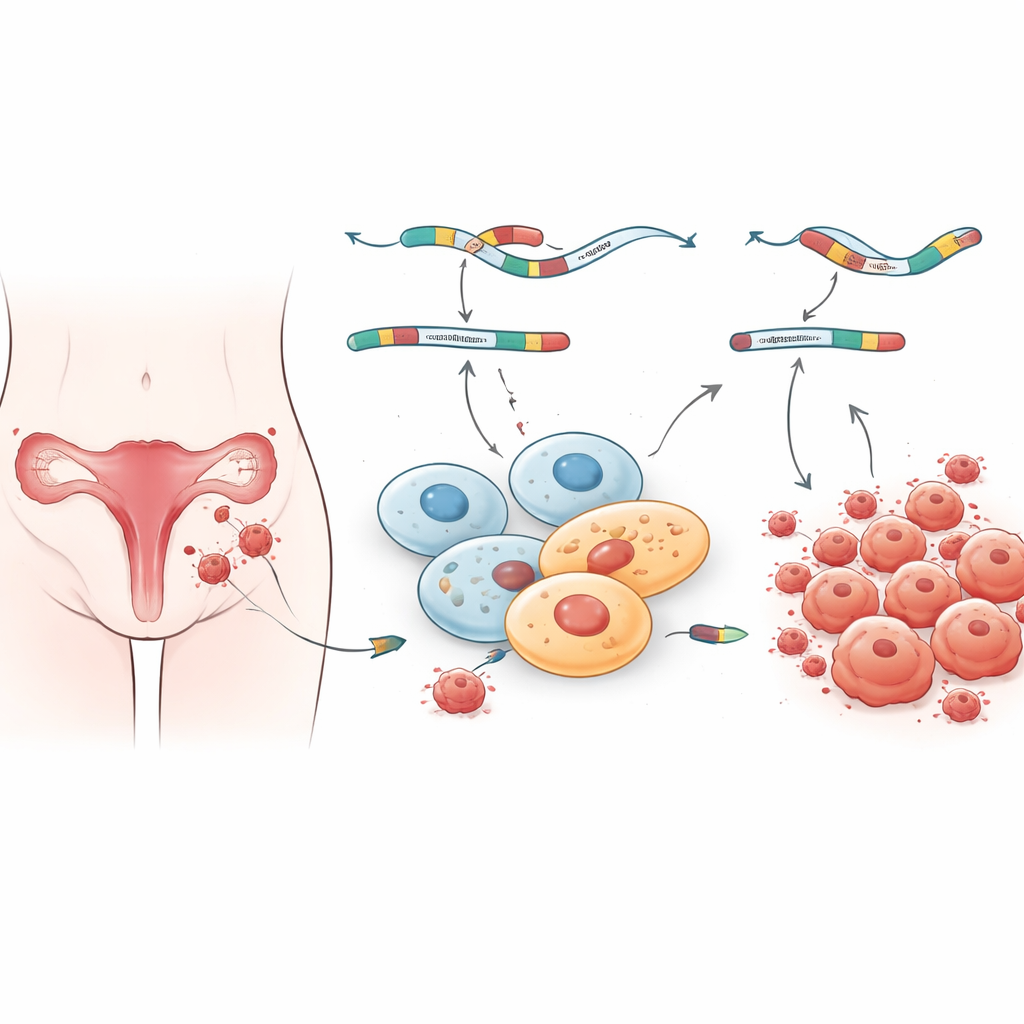
Impronte molecolari distinte in siti lesionali diversi
Il gruppo si è poi chiesto quali tipi di geni fossero maggiormente interessati da questi modelli di editing alterati. L’analisi di arricchimento ha mostrato che sia l’attività genica complessiva sia lo splicing anomalo nelle lesioni si concentrano in vie legate all’interazione con le proteine, al segnalamento cellulare e al telaio strutturale che circonda le cellule. Queste vie contribuiscono a controllare come le cellule percepiscono l’ambiente, si attaccano tra loro e rispondono a ormoni e segnali infiammatori — tutti processi noti per essere compromessi nell’endometriosi. È interessante che le lesioni ovariche e peritoneali condividano alcuni cambiamenti di splicing ma presentino anche molte differenze, suggerendo che le lesioni in sedi diverse portano impronte molecolari distinte. Questo può aiutare a spiegare perché le pazienti mostrino sintomi e risposte al trattamento molto diversi, anche quando la malattia appare simile al microscopio.
Due geni protettivi che frenano la crescita
Per passare dai modelli ai meccanismi, i ricercatori si sono concentrati su due geni, GALNT7 e ZNF28, i cui messaggi di RNA mostravano una perdita coerente di segmenti chiave nelle lesioni. Utilizzando cellule epiteliali endometriali umane coltivate in laboratorio, hanno ridotto sperimentalmente i livelli di questi geni o rimosso gli esoni specifici che risultavano saltati nei pazienti. In entrambi i casi, le cellule hanno iniziato a moltiplicarsi più rapidamente e a formare più colonie nel tempo, imitando la crescita incontrollata osservata nel tessuto endometriosico. Dati aggiuntivi a singola cellula hanno mostrato che nel tessuto sano questi geni sono particolarmente attivi nelle cellule epiteliali — le stesse cellule che compongono le ghiandole nelle lesioni endometriosiche — ma la loro espressione crolla nelle lesioni. Nel complesso, questi risultati suggeriscono che GALNT7 e ZNF28 correttamente splicati agiscono normalmente come freni sulla crescita cellulare, e che un editing difettoso del loro RNA indebolisce questi freni.
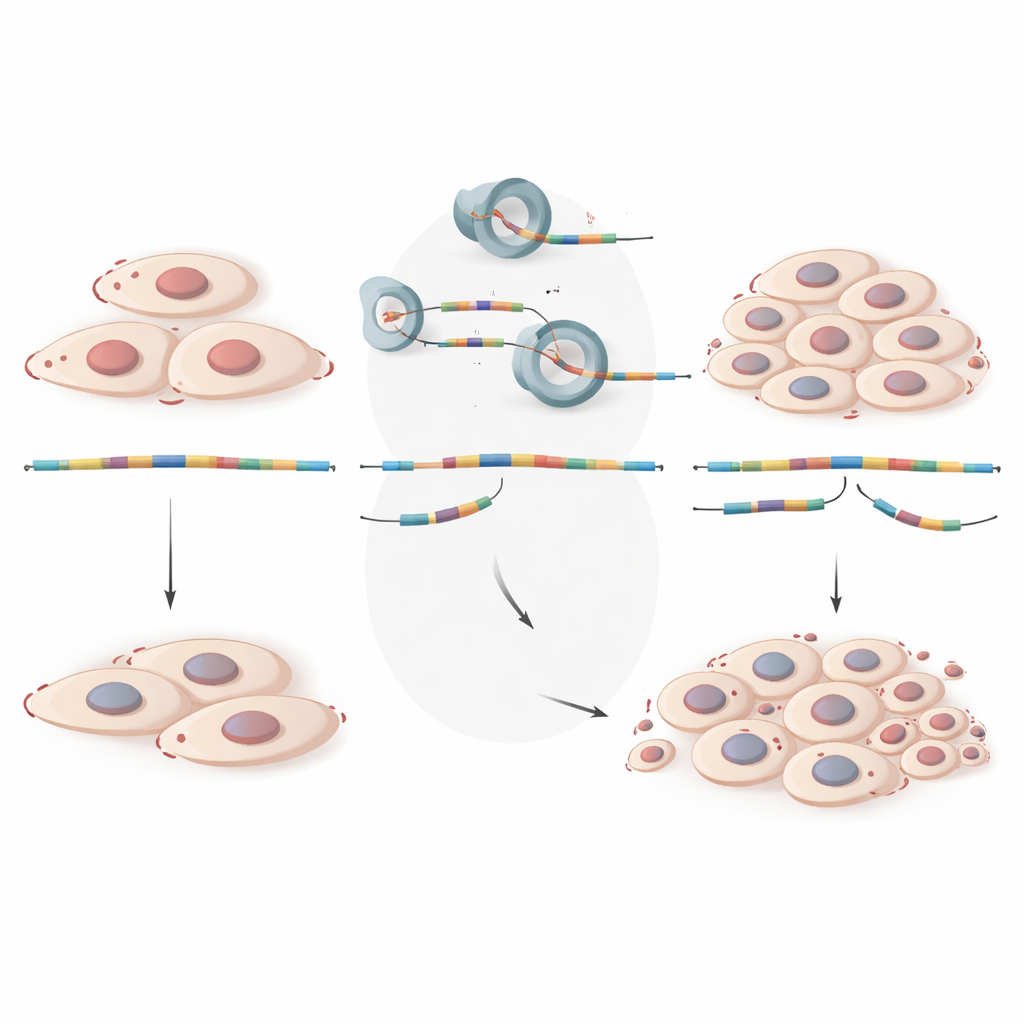
Dai messaggi mal editati alle lesioni in crescita
Visto in termini non tecnici, questo lavoro mostra che l’endometriosi non riguarda solo il tessuto che cresce nel posto sbagliato; riguarda anche cellule che utilizzano istruzioni genetiche distorte. Quando la macchina di editing della cellula elabora in modo errato certi messaggi di RNA, geni che controllano la crescita come GALNT7 e ZNF28 risultano effettivamente attenuati, permettendo alle cellule nelle lesioni di moltiplicarsi più facilmente. Mappando questo livello nascosto di splicing dysregolato, lo studio mette in evidenza nuove firme molecolari che potrebbero in futuro aiutare a una diagnosi più precoce e a identificare le donne a rischio più elevato. Apre inoltre la possibilità che terapie future possano agire non solo bloccando ormoni o rimuovendo tessuto chirurgicamente, ma correggendo o aggirando l’editing difettoso dell’RNA per ripristinare i controlli naturali della crescita cellulare.
Citazione: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
Parole chiave: endometriosi, splicing alternativo, regolazione dell'RNA, proliferazione cellulare, salute delle donne