Clear Sky Science · pt
Splicing alternativo desregulado na endometriose: um papel de variantes aberrantes de mRNA no crescimento de células endometrióticas
Por que mensagens genéticas ocultas importam para a saúde da mulher
A endometriose afeta aproximadamente uma em cada dez mulheres em idade reprodutiva, mas frequentemente leva anos para ser diagnosticada e pode causar dor incapacitante e infertilidade. Este estudo investiga abaixo da superfície da doença uma camada sutil de controle genético chamada splicing de RNA — como as células editam suas mensagens genéticas antes de transformá-las em proteínas. Ao revelar como esse processo de edição se altera na endometriose, os pesquisadores apontam um motor oculto do crescimento das lesões e indicam novas maneiras de detectar e possivelmente tratar a doença no futuro.
Quando o tecido cresce onde não deveria
Na endometriose, tecido que se assemelha ao revestimento uterino aparece nos ovários, na parede pélvica e em outros órgãos próximos. Esses pedaços deslocados, ou lesões, respondem a hormônios, provocam inflamação e podem invadir o tecido ao redor, levando a dor crônica e problemas de fertilidade. Mas nem toda pessoa com fluxo menstrual retrógrado na pelve desenvolve endometriose, o que sugere que mudanças moleculares internas adicionais nas células ajudam a determinar quem desenvolve a doença e quão grave ela se torna. Cientistas já catalogaram muitos genes cuja atividade global é alterada em lesões endometrióticas. O que faltava era uma análise mais detalhada de como essas mensagens gênicas são editadas dentro das células antes de serem usadas.
Editando mensagens gênicas: um passo extra crucial
Os genes são primeiro copiados em longas fitas de RNA que devem ser cortadas e religadas — um processo conhecido como splicing — antes de servirem como instruções para construir proteínas. As células podem emendar o mesmo gene de maneiras diferentes, criando múltiplas versões de uma proteína com funções distintas. Essa flexibilidade permite que os tecidos ajustem seu comportamento, mas também cria oportunidades para erro. Os autores analisaram dados de sequenciamento de RNA de mulheres com endometriose ovariana e peritoneal e de mulheres sem a doença. Usando ferramentas computacionais avançadas, examinaram cinco tipos principais de eventos de splicing e encontraram centenas de diferenças em como as mensagens gênicas são editadas nas lesões em comparação com o endométrio saudável. Dois tipos de alterações se destacaram: exons saltados, nos quais um segmento importante é omitido, e introns retidos, nos quais material extra que deveria ser removido é mantido por engano na mensagem.
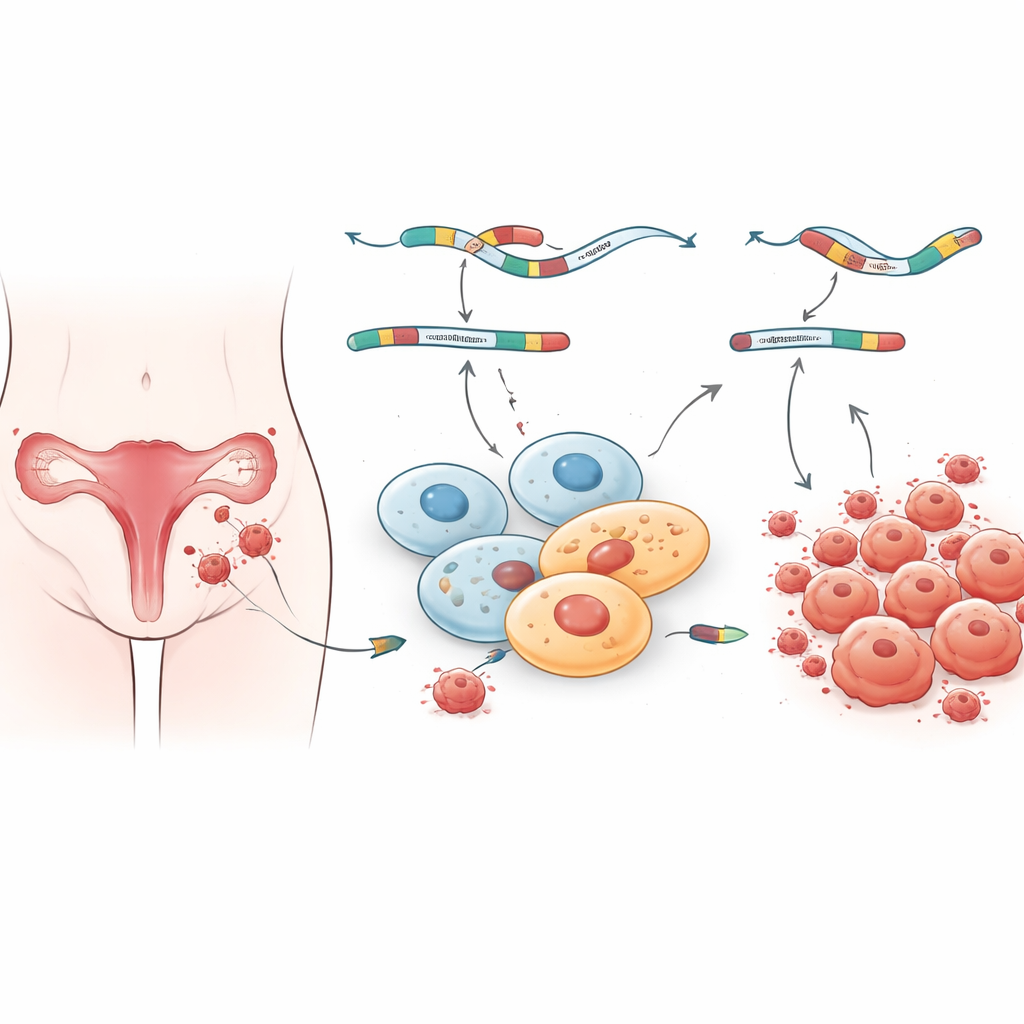
Impressões digitais moleculares distintas em diferentes sítios de lesão
A equipe então investigou que tipos de genes eram mais afetados por esses padrões alterados de edição. A análise de enriquecimento mostrou que tanto a atividade gênica geral quanto o splicing anômalo nas lesões se concentravam em vias relacionadas à ligação de proteínas, sinalização celular e à matriz estrutural que envolve as células. Essas vias ajudam a controlar como as células percebem o ambiente, aderem umas às outras e respondem a hormônios e sinais inflamatórios — todos processos conhecidos por serem perturbados na endometriose. Curiosamente, lesões ovarianas e peritoneais compartilhavam algumas alterações de splicing, mas também exibiam muitas específicas, sugerindo que lesões em locais diferentes carregam impressões digitais moleculares distintas. Isso pode ajudar a explicar por que pacientes podem apresentar padrões de sintomas e respostas ao tratamento muito diferentes, mesmo quando a doença parece similar ao microscópio.
Dois genes protetores que ajudam a conter o crescimento
Para avançar de padrões para mecanismos, os pesquisadores focaram em dois genes, GALNT7 e ZNF28, cujas mensagens de RNA mostraram perda consistente de segmentos-chave nas lesões. Usando células epiteliais endometriais humanas cultivadas em laboratório, reduziram experimentalmente os níveis desses genes ou removeram os exons específicos que eram pulados em pacientes. Em ambos os casos, as células começaram a se multiplicar mais rápido e formaram mais colônias ao longo do tempo, mimetizando o crescimento descontrolado observado no tecido endometriótico. Dados adicionais de célula única mostraram que, em tecido saudável, esses genes são especialmente ativos em células epiteliais — as próprias células que compõem as glândulas nas lesões endometriais —, mas sua expressão cai acentuadamente nas lesões. Em conjunto, esses resultados sugerem que GALNT7 e ZNF28 corretamente emendados atuam normalmente como freios ao crescimento celular, e que a edição defeituosa de seus RNAs enfraquece esses freios.
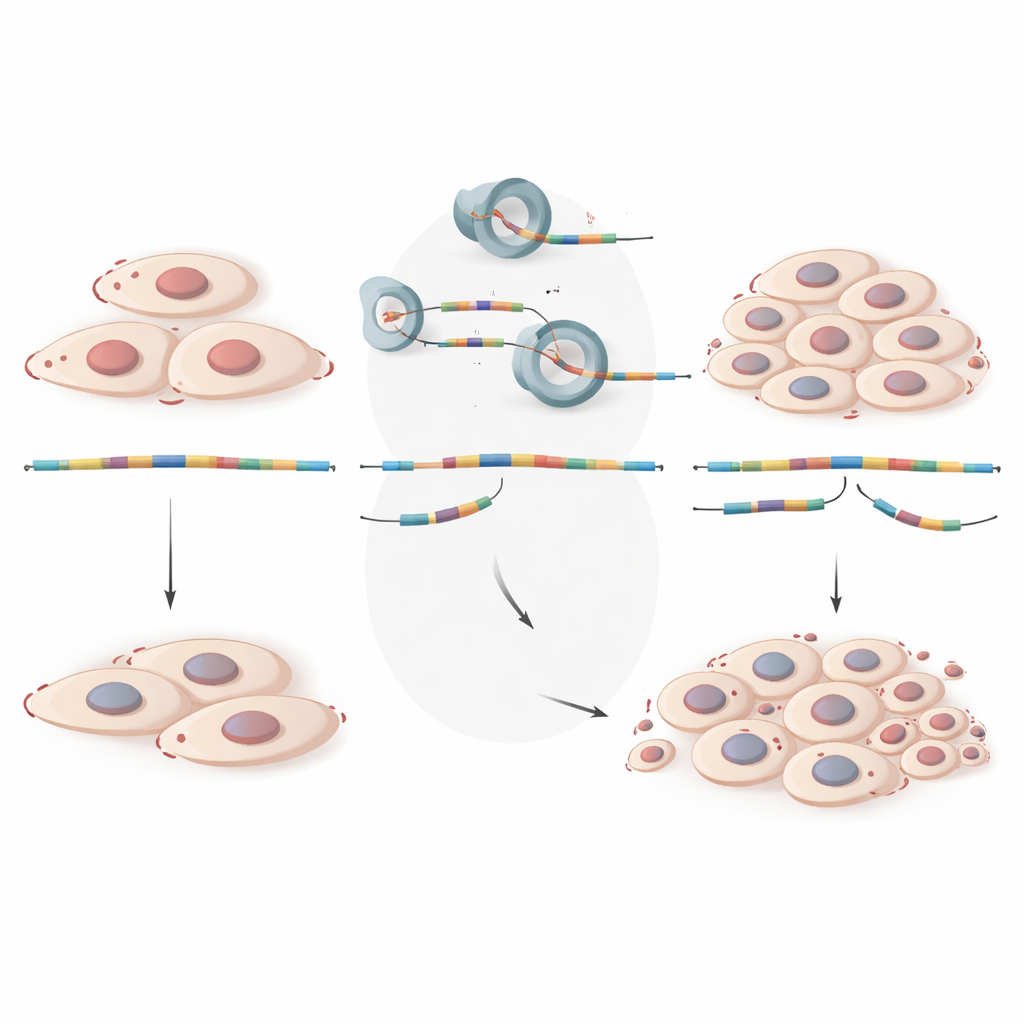
De mensagens mal editadas a lesões em crescimento
Visto por uma lente não técnica, este trabalho mostra que a endometriose não é apenas sobre tecido crescendo no lugar errado; trata-se também de células usando instruções genéticas distorcidas. Quando a maquinaria de edição da célula processa mal certas mensagens de RNA, genes que controlam o crescimento como GALNT7 e ZNF28 ficam efetivamente reduzidos, permitindo que as células nas lesões se multipliquem com mais facilidade. Ao mapear essa camada oculta de splicing desregulado, o estudo destaca novas assinaturas moleculares que, eventualmente, podem ajudar em um diagnóstico mais precoce e na identificação de mulheres com risco mais elevado. Também levanta a possibilidade de que terapias futuras possam atuar não apenas bloqueando hormônios ou removendo tecido cirurgicamente, mas corrigindo ou contornando a edição defeituosa de RNA para restaurar os controles naturais de crescimento da célula.
Citação: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
Palavras-chave: endometriose, splicing alternativo, regulação de RNA, proliferação celular, saúde da mulher