Clear Sky Science · pl
Nieprawidłowo regulowane alternatywne składanie RNA w endometriozie: rola aberrantnych wariantów mRNA w wzroście komórek endometriotycznych
Dlaczego ukryte komunikaty genów mają znaczenie dla zdrowia kobiet
Endometrioza dotyka około jednej na dziesięć kobiet w wieku rozrodczym, a mimo to często trwa latami, zanim zostanie rozpoznana, i może powodować wyniszczający ból oraz niepłodność. To badanie zagląda pod powierzchnię choroby, do subtelnej warstwy kontroli genetycznej zwanej składaniem RNA — sposobu, w jaki komórki edytują swoje komunikaty genowe zanim przekształcą je w białka. Odkrywając, jak ten proces edycji ulega zaburzeniu w endometriozie, autorzy ujawniają ukryty czynnik napędzający wzrost zmian chorobowych i wskazują nowe ścieżki do wykrywania, a być może leczenia choroby w przyszłości.
Kiedy tkanka rośnie tam, gdzie nie powinna
W endometriozie tkanka przypominająca błonę śluzową macicy pojawia się na jajnikach, ścianie miednicy i innych pobliskich narządach. Te przemieszczone ogniska, czyli zmiany, reagują na hormony, wywołują stan zapalny i mogą naciekać otaczające tkanki, prowadząc do przewlekłego bólu i problemów z płodnością. Jednak nie każda osoba z cofającą się krwią miesiączkową do jamy brzusznej rozwija endometriozę, co sugeruje, że dodatkowe zmiany molekularne wewnątrz komórek wpływają na to, kto zachoruje i jak ciężki będzie przebieg choroby. Naukowcy opracowali już katalog wielu genów, których ogólna aktywność jest zmieniona w zmianach endometriotycznych. Brakowało jednak dokładniejszego spojrzenia na to, jak te komunikaty genowe są edytowane wewnątrz komórek zanim zostaną wykorzystane.
Edytowanie komunikatów genowych: kluczowy dodatkowy krok
Geny najpierw są przepisywane na długie nici RNA, które muszą zostać pocięte i ponownie połączone — proces znany jako składanie (splicing) — zanim będą mogły służyć jako instrukcje do budowy białek. Komórki mogą składać ten sam gen w różny sposób, tworząc wiele wersji białka o odmiennych funkcjach. Ta elastyczność pozwala tkankom precyzyjnie dostosowywać swoje zachowanie, ale stwarza też możliwości popełnienia błędów. Autorzy przeanalizowali dane z sekwencjonowania RNA od kobiet z endometriozą jajnikową i otrzewnową oraz od kobiet bez choroby. Przy użyciu zaawansowanych narzędzi obliczeniowych zbadali pięć głównych typów zdarzeń składania i znaleźli setki różnic w sposobie edycji komunikatów genowych w zmianach w porównaniu ze zdrową błoną śluzową macicy. Dwa typy zmian wyróżniały się szczególnie: pomijane eksony, w których ważny fragment jest pomijany, oraz zatrzymane introny, w których dodatkowy materiał, który powinien zostać usunięty, jest błędnie zachowywany w komunikacie.
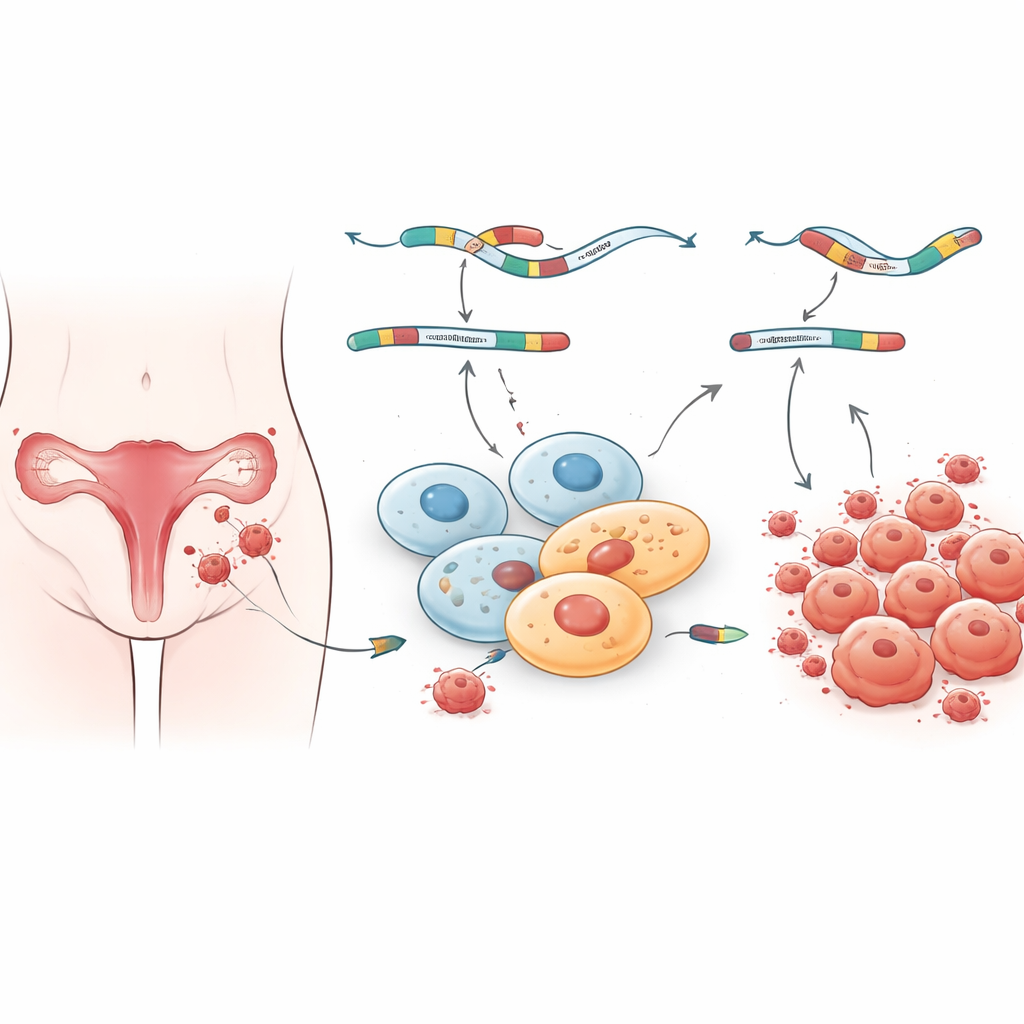
Odciśnięte odciski molekularne w różnych lokalizacjach zmian
Zespół następnie zapytał, które rodzaje genów były najbardziej dotknięte tymi zmienionymi wzorcami edycji. Ich analiza wzbogacenia wykazała, że zarówno ogólna aktywność genów, jak i nieprawidłowe składanie w zmianach skupiały się w szlakach związanych z wiązaniem białek, sygnalizacją komórkową oraz strukturą podporową otaczającą komórki. Te szlaki pomagają kontrolować, jak komórki odbierają sygnały z otoczenia, przylegają do siebie i reagują na hormony oraz sygnały zapalne — wszystkie procesy znane z zaburzeń w endometriozie. Co ciekawe, zmiany jajnikowe i otrzewnowe miały pewne wspólne modyfikacje składania, ale wykazały też wiele unikalnych zmian, co sugeruje, że ogniska w różnych miejscach niosą odrębne molekularne odciski. To może pomóc wyjaśnić, dlaczego pacjentki mogą mieć bardzo różne wzorce objawów i odpowiedzi na leczenie, nawet jeśli choroba wydaje się podobna pod mikroskopem.
Dwa geny ochronne, które hamują wzrost
Aby przejść od wzorców do mechanizmów, badacze przyjrzeli się bliżej dwóm genom, GALNT7 i ZNF28, których komunikaty RNA wykazywały konsekwentną utratę kluczowych segmentów w zmianach. Używając laboratoryjnie hodowanych ludzkich komórek nabłonkowych endometrium, eksperymentalnie zmniejszyli poziomy tych genów lub usunęli specyficzne eksony, które były pomijane u pacjentek. W obu przypadkach komórki zaczęły mnożyć się szybciej i z czasem tworzyły więcej kolonii, naśladując niekontrolowany wzrost obserwowany w tkance endometriotycznej. Dodatkowe dane z pojedynczych komórek pokazały, że w zdrowej tkance te geny są szczególnie aktywne w komórkach nabłonkowych — tych, które tworzą gruczoły w zmianach endometrialnych — lecz ich ekspresja gwałtownie spada w zmianach. Razem wyniki te sugerują, że prawidłowo składane GALNT7 i ZNF28 działają normalnie jak hamulce wzrostu komórek, a wadliwa edycja ich RNA osłabia te hamulce.
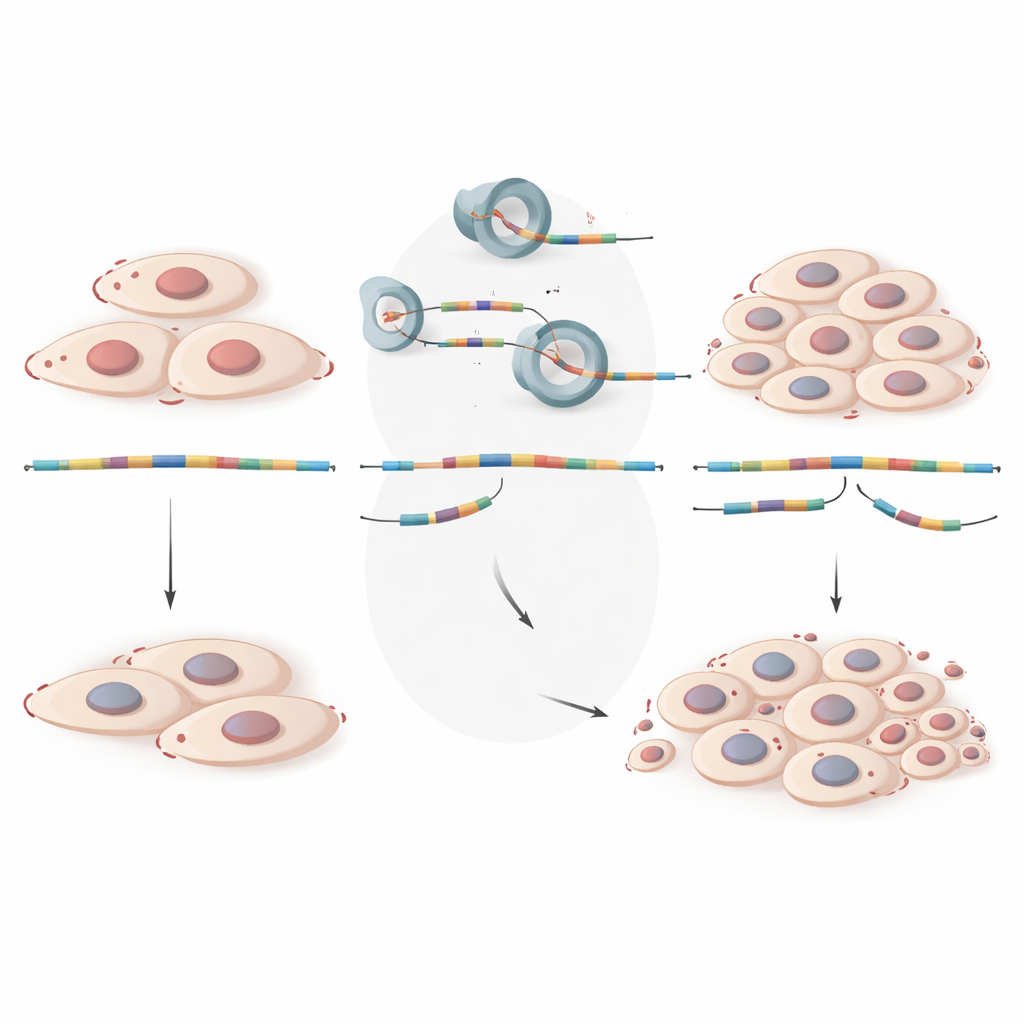
Od błędnie edytowanych komunikatów do rosnących zmian
Patrząc przez pryzmat nietechniczny, ta praca pokazuje, że endometrioza to nie tylko tkanka rosnąca w niewłaściwym miejscu; to także komórki korzystające ze zniekształconych instrukcji genetycznych. Gdy maszyny edytujące komórkowe błędnie przetwarzają niektóre komunikaty RNA, geny kontrolujące wzrost, takie jak GALNT7 i ZNF28, są de facto wyciszane, co pozwala komórkom w zmianach mnożyć się łatwiej. Mapując tę ukrytą warstwę nieprawidłowo regulowanego składania, badanie uwydatnia nowe molekularne sygnatury, które w przyszłości mogą pomóc we wcześniejszej diagnozie i identyfikacji kobiet o wyższym ryzyku. Stwarza też możliwość, że przyszłe terapie mogłyby działać nie tylko przez blokowanie hormonów lub chirurgiczne usuwanie tkanek, lecz poprzez naprawę lub obejście wadliwej edycji RNA, aby przywrócić naturalne mechanizmy kontroli wzrostu komórek.
Cytowanie: Davuluri, V.N.G., Dias, M., Llinas, R. et al. Misregulated alternative splicing in endometriosis: a role for aberrant mRNA variants in endometriotic cell growth. Cell Death Discov. 12, 149 (2026). https://doi.org/10.1038/s41420-026-03015-z
Słowa kluczowe: endometrioza, alternatywne składanie, regulacja RNA, proliferacja komórek, zdrowie kobiet