Clear Sky Science · zh
子宫内膜异位症免疫微环境的时序变迁:从免疫逃逸到免疫衰竭
为何机体防御在子宫内膜异位症中至关重要
子宫内膜异位症是一种疼痛性疾病,其特征是类似子宫内膜的组织在不该生长的部位出现,常导致剧烈痉挛、持续性盆腔疼痛和生育困难。本文探讨了该病较少为人知的一面:机体的防御系统——免疫系统,如何先未能清除这些错位细胞,随后又逐渐疲惫不堪。理解这一不断变化的“免疫景观”有助于解释为何子宫内膜异位症会持续存在、随时间加重,并在手术后常常复发。
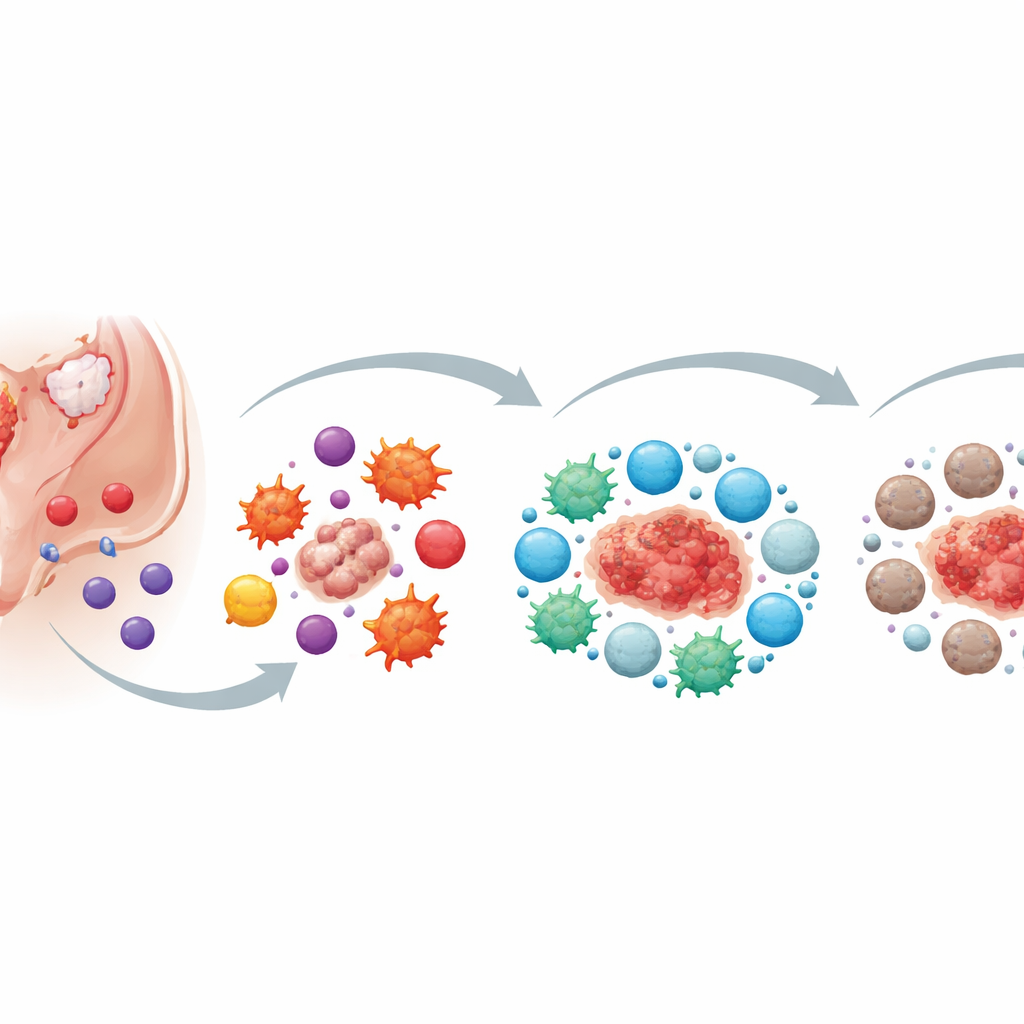
最初阶段:问题细胞如何躲过防线
作者将最早期称为“免疫逃逸”。正常情况下,专职的白细胞在体内巡逻并清除异常细胞。在子宫内膜异位症中,异位子宫内膜细胞(EECs)进入腹腔,但关键的“杀伤”细胞——自然杀伤(NK)细胞、某些T细胞和巨噬细胞——并未有效清除它们。这些杀伤细胞虽在,但它们的攻击能力被削弱。激活信号被降低,抑制信号被增强,且它们进入适当位置的能力减弱。异位细胞通过释放化学信使和微小囊泡(外泌体)主动促成这种失败,抑制杀伤细胞活性并降低巨噬细胞吞噬不需要细胞的能力。
月经周期、辅助者与炎症风暴
随着月经血与组织逆流进入腹腔,经期的其他成分也加入进来。血小板和红细胞的分解产物进一步削弱了NK细胞与巨噬细胞的杀伤力。它们不但没有清除这些流失的组织,反而帮助其附着、侵袭并生长。此时免疫环境呈强烈炎症状态:许多细胞释放警报信号,理论上这些信号应有助于对抗异常组织,但这些信号同时也促进血管生成、细胞增殖和病灶的侵袭。炎症成为一种双刃剑——既不足以消除病灶,又足以助长其扩展与所致疼痛。
从炽热炎症到看似平静却有害的宁静
随着时间推移,病灶周围的免疫细胞平衡发生转变。早期以“攻击性”巨噬细胞和辅助性T细胞为主,释放促炎信号。随着病灶增大并反复出血,它们开始吸引并重塑另一类免疫细胞——抑制反应、限制损伤的细胞。抗炎巨噬细胞、调节性T细胞及其他“安抚型”细胞数量增加,这些细胞被化学趋化因子和在反复出血时释放的“警示蛋白”吸引。血小板与局部激素(如雌激素)也促使系统转向更平静、抗炎的状态。尽管这种更平静的环境保护了周围组织免受慢性、不可控炎症的损害,但它同时掩护了病灶,促进新血管生长,并助长瘢痕样纤维组织的堆积。
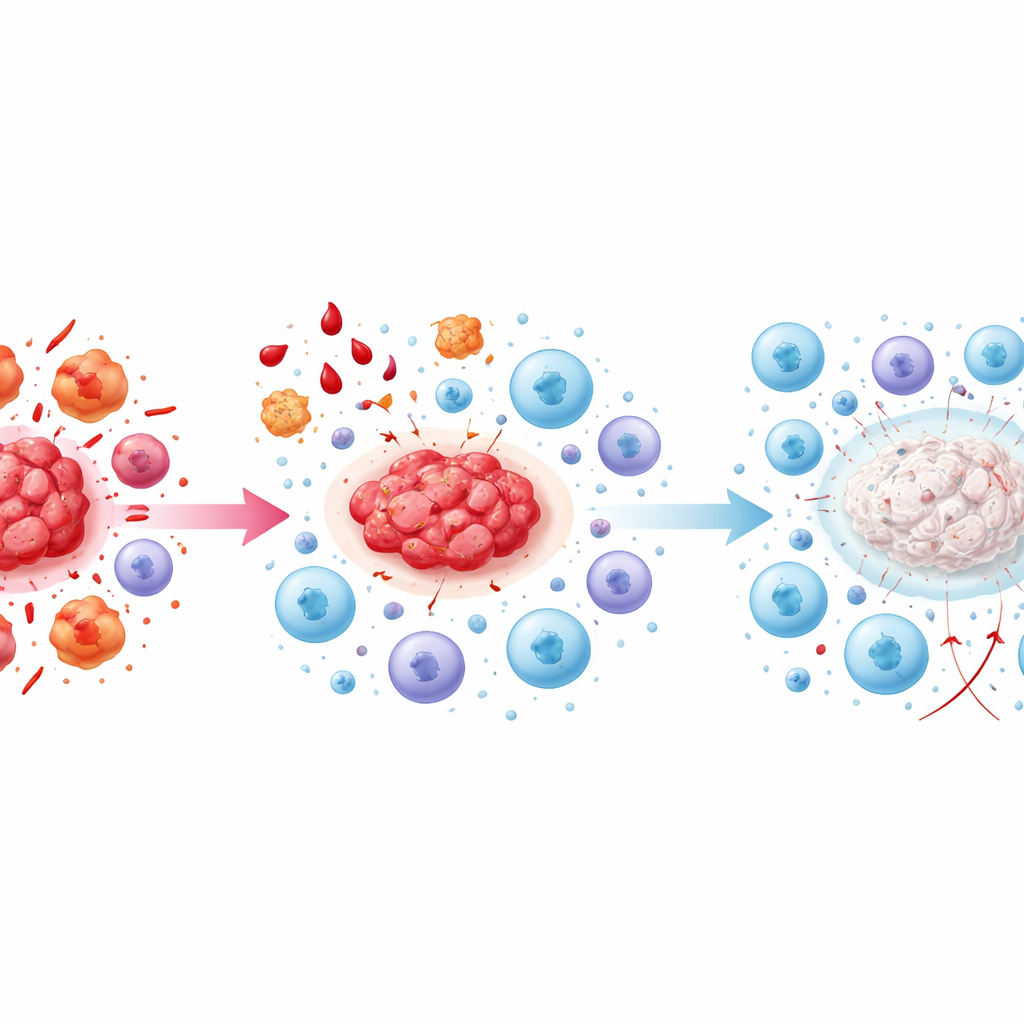
当“杀手”精疲力竭
在晚期,文章描述了一种“免疫衰竭”状态。那些曾经在原则上能够攻击病灶的杀伤细胞,如今因长期过度刺激并持续受抗炎信号抑制而疲惫不堪。它们开始表达典型的疲惫表面标志,关键攻击分子的生成下降。由抗炎细胞和血小板产生的TGF-β与IL-10等信号加强了这种衰竭。与此同时,免疫细胞上的检查点——通常用于防止过度反应的分子刹车——愈发被激活,进一步压制了反应。结果形成一种自我维持的局面:病灶持续存在、血供充足并逐渐纤维化,而本应控制它们的细胞虽然在位,却大多无能为力。
对未来治疗的启示
对非专业读者来说,关键信息是:子宫内膜异位症不仅仅是流离组织的问题,更是机体防御时序与平衡的问题。综述提出疾病经历四个免疫阶段:逃逸、早期炎症、后期抗炎,最终走向免疫衰竭。由于每一阶段涉及不同的细胞与信号组合,某一时点有效的治疗在另一时点可能失效。那些有针对性地增强杀伤细胞活性、促进合适类型的炎症,或打断血小板、激素与抑制性免疫细胞之间有害联动的策略,或许有朝一日能减缓甚至逆转病灶生长。通过描绘这一免疫时间线,作者旨在为更精确、与疾病阶段相匹配的治疗提供指导,并强调仅仅切除病灶常常并不足以解决问题的原因。
引用: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
关键词: 子宫内膜异位症, 免疫微环境, 慢性炎症, 免疫衰竭, 女性健康