Clear Sky Science · fr
Décalages temporels du microenvironnement immunitaire dans l’endométriose : de l’évasion immunitaire à l’épuisement immunitaire
Pourquoi les défenses de l’organisme comptent dans l’endométriose
L’endométriose est une affection douloureuse dans laquelle un tissu semblable à la muqueuse utérine se développe là où il n’a pas sa place, provoquant souvent de fortes crampes, des douleurs pelviennes persistantes et des difficultés à concevoir. Cet article explore un aspect moins familier de la maladie : la manière dont le système immunitaire de l’organisme d’abord échoue à éliminer ces cellules déplacées, puis finit par s’épuiser. Comprendre ce « paysage immunitaire » en évolution pourrait aider à expliquer pourquoi l’endométriose persiste, s’aggrave avec le temps et récidive souvent même après une intervention chirurgicale.
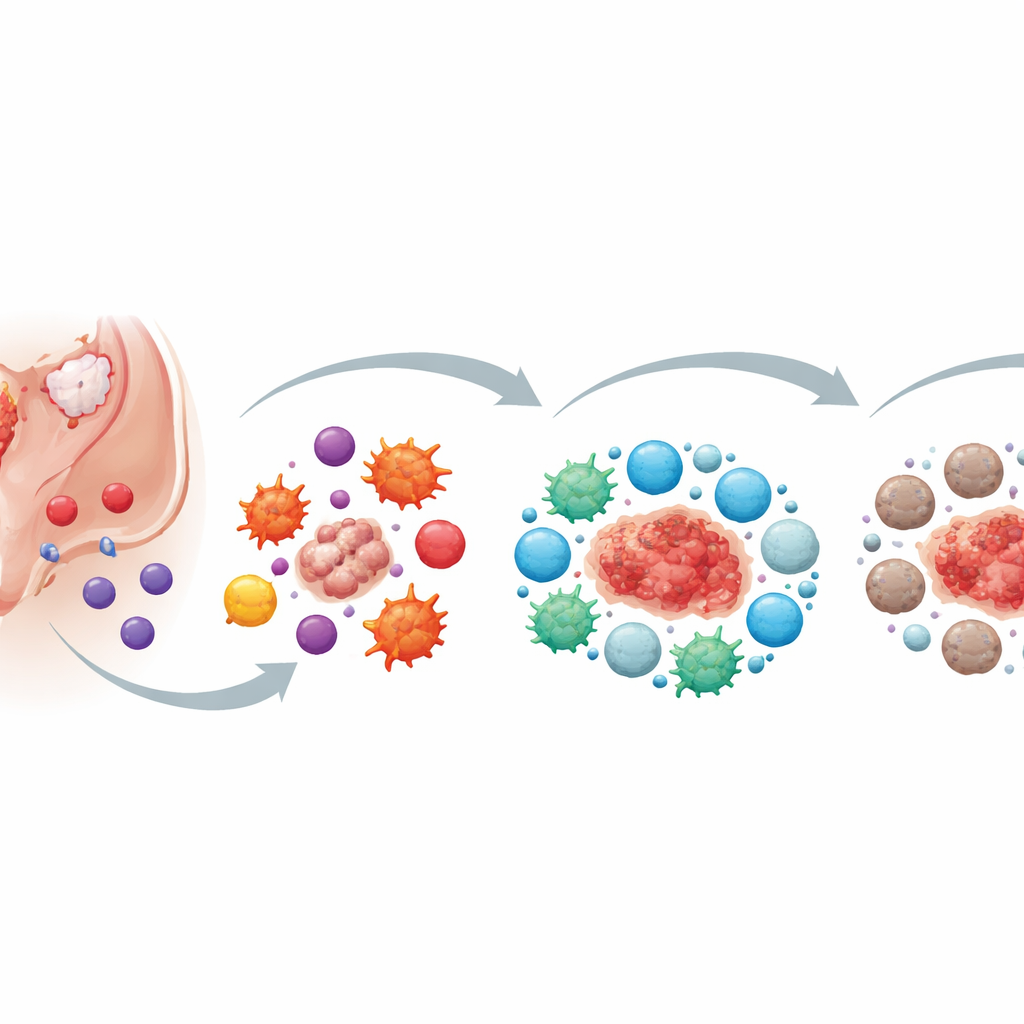
Premiers pas : comment les cellules problématiques passent la défense
Les auteurs décrivent la phase la plus précoce comme une « évasion immunitaire ». Normalement, des globules blancs spécialisés patrouillent et éliminent les cellules anormales. Dans l’endométriose, des cellules endométriales ectopiques (CEE) se retrouvent dans la cavité abdominale, mais les cellules « tueuses » clés — les cellules NK (natural killer), certaines cellules T et les macrophages — ne les éliminent pas efficacement. Ces cellules tueuses sont présentes, mais leur capacité d’attaque est affaiblie. Leurs commutateurs d’activation sont abaissés, leurs freins inhibiteurs renforcés, et elles peinent à migrer au bon endroit au bon moment. Les CEE contribuent activement à cet échec en libérant des messagers chimiques et de petites vésicules membranaires (exosomes) qui atténuent l’activité des cellules tueuses et réduisent la capacité des macrophages à « phagocyter » les cellules indésirables.
Cycles mensuels, aides involontaires et une tempête inflammatoire
Lorsque le sang et les tissus menstruels refluent dans la cavité abdominale, d’autres composantes des règles entrent en jeu. Les plaquettes et les produits de dégradation des globules rouges affaiblissent encore le pouvoir cytotoxique des cellules NK et des macrophages. Au lieu d’éliminer le tissu égaré, ils favorisent son adhérence, son invasion et sa croissance. À ce stade, le microenvironnement immunitaire est fortement inflammatoire : de nombreuses cellules libèrent des signaux d’alerte qui, en théorie, devraient aider à combattre le tissu anormal. Pourtant ces mêmes signaux encouragent aussi la formation de nouveaux vaisseaux sanguins, la division cellulaire et l’invasion par les lésions d’endométriose. L’inflammation devient une arme à double tranchant : trop faible pour éliminer les lésions, mais suffisamment forte pour alimenter leur expansion et la douleur qu’elles provoquent.
D’une inflammation “chaude” à un calme apaisant mais nuisible
Au fil du temps, l’équilibre des cellules immunitaires autour des lésions change. Au début, des macrophages « attaquants » et des cellules T auxiliaires dominent, libérant des signaux agressifs qui favorisent l’inflammation. À mesure que les lésions grossissent et saignent à répétition, elles attirent et transforment un autre type de cellules immunitaires : celles qui apaisent les réponses et limitent les dégâts. Les macrophages anti-inflammatoires, les cellules T régulatrices et d’autres types cellulaires « réparateurs » augmentent en nombre, attirés par des chimiokines et des molécules d’alarme libérées lors des saignements répétés. Les plaquettes et des hormones locales, comme les œstrogènes, poussent aussi le système vers un état plus calme et anti-inflammatoire. Bien que ce milieu plus apaisé protège les tissus environnants d’une inflammation chronique incontrôlée, il abrite simultanément les lésions, favorise la néovascularisation et encourage l’accumulation de tissu fibreux cicatriciel.
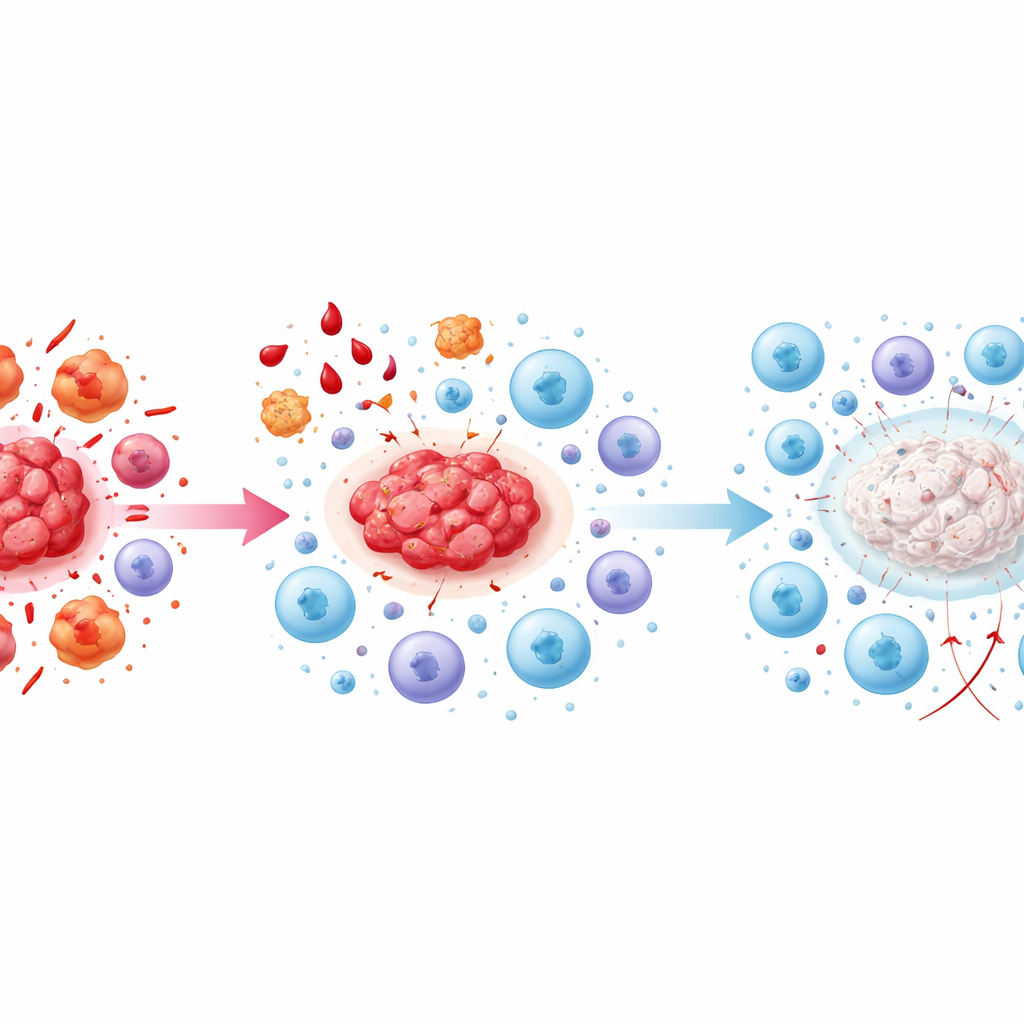
Quand les cellules tueuses manquent d’énergie
Dans les stades avancés, l’article décrit un état d’« épuisement immunitaire ». Les cellules tueuses qui auraient pu attaquer les lésions sont désormais stimulées de façon chronique et continuellement supprimées par des signaux anti-inflammatoires. Elles commencent à exprimer des marqueurs de surface typiques de cellules fatiguées et inefficaces, et leur production de molécules effectrices décline. Des signaux tels que le TGF-bêta et l’IL-10, produits par des cellules anti-inflammatoires et des plaquettes, renforcent cet épuisement. Parallèlement, les points de contrôle immunitaires — des freins moléculaires qui empêchent normalement les réactions excessives — sont de plus en plus activés, étouffant encore la réponse. Le résultat est une situation auto-entretenue dans laquelle les lésions persistent, sont abondamment irriguées et deviennent fibreuses, tandis que les cellules qui devraient les contrôler sont présentes mais en grande partie impuissantes.
Ce que cela implique pour les traitements futurs
Pour un non-spécialiste, le message est que l’endométriose n’est pas seulement un problème de tissu errant, mais de chronologie et d’équilibre des défenses de l’organisme. La revue propose que la maladie traverse quatre phases immunitaires : évasion, inflammation précoce, anti-inflammation ultérieure et enfin épuisement immunitaire. Comme chaque phase implique des mélanges différents de cellules et de signaux, des traitements efficaces à un moment donné peuvent échouer à un autre. Des stratégies visant à stimuler avec précision l’activité des cellules tueuses, à encourager le type d’inflammation approprié ou à interrompre le partenariat nuisible entre plaquettes, hormones et cellules immunitaires calmantes pourraient un jour ralentir ou même inverser la croissance des lésions. En cartographiant cette chronologie immunitaire, les auteurs cherchent à orienter des thérapies plus précises, adaptées au stade, et à expliquer pourquoi l’ablation simple des lésions n’est souvent pas suffisante en soi.
Citation: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
Mots-clés: endométriose, microenvironnement immunitaire, inflammation chronique, épuisement immunitaire, santé des femmes