Clear Sky Science · nl
Timingverschuivingen in het immuunmicrobioom bij endometriose: van immuunontsnapping naar immuunoogst
Waarom de afweer van het lichaam ertoe doet bij endometriose
Endometriose is een pijnlijke aandoening waarbij weefsel dat lijkt op het baarmoederslijmvlies groeit op plekken waar het niet thuishoort, wat vaak ernstige krampen, aanhoudende bekkenpijn en problemen met vruchtbaarheid veroorzaakt. Dit artikel belicht een minder bekende kant van de ziekte: hoe het immuunsysteem eerst faalt in het opruimen van deze verkeerd geplaatste cellen en vervolgens geleidelijk uitgeput raakt. Inzicht in dit verschuivende “immuunlandschap” kan helpen verklaren waarom endometriose aanhoudt, in de loop van de tijd verergert en vaak terugkeert zelfs na een operatie.
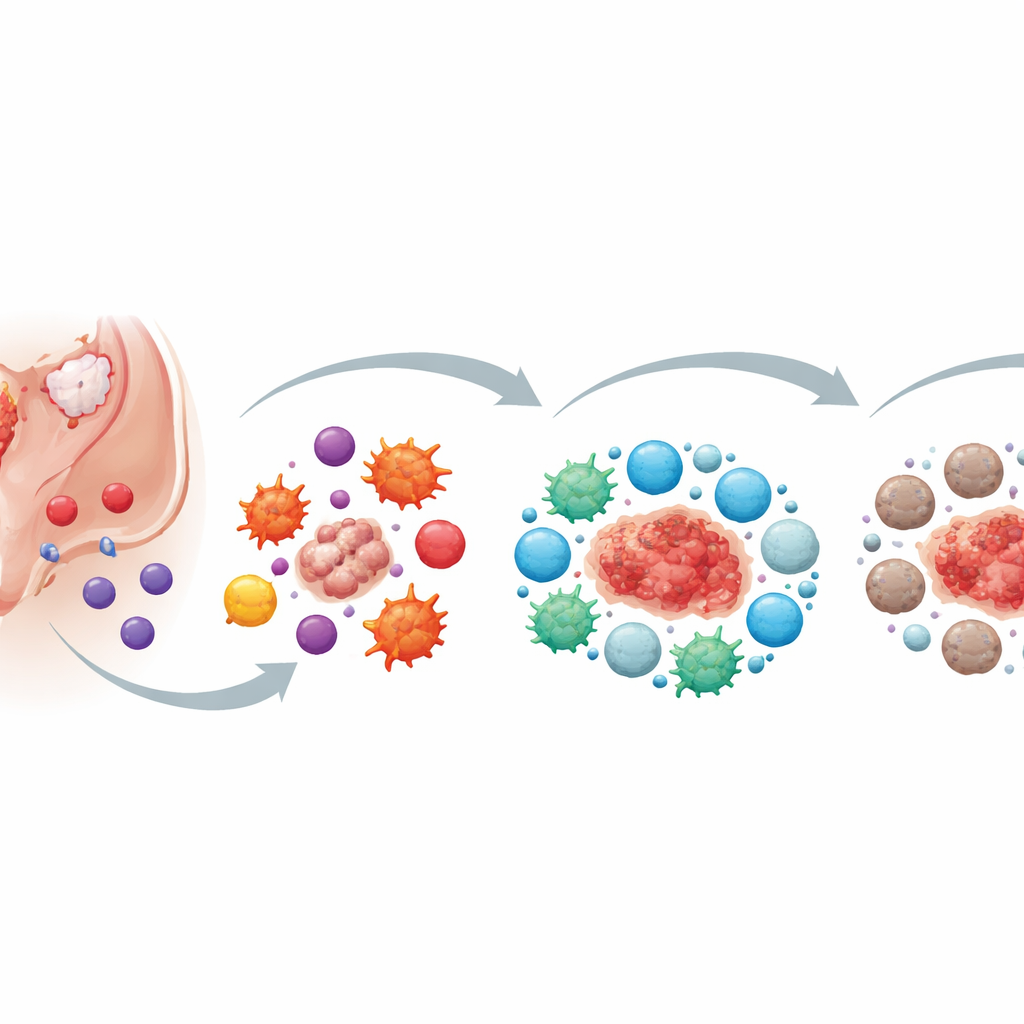
Eerste stappen: hoe problematische cellen de verdediging omzeilen
De auteurs beschrijven de vroegste fase als “immuunontsnapping.” Normaal patrouilleren gespecialiseerde witte bloedcellen het lichaam en ruimen abnormale cellen op. Bij endometriose belanden ectopische endometriumcellen (EEC’s) in de buikholte, maar belangrijke “killer”-cellen — natural killer (NK)-cellen, bepaalde T‑cellen en macrofagen — verwijderen ze niet effectief. Deze killer-cellen zijn aanwezig, maar hun aanvalscapaciteit is verzwakt. Hun activerende schakelaars staan lager, remmende schakelaars hoger, en ze kunnen minder goed naar de juiste plek migreren op het juiste moment. EEC’s dragen actief bij aan dit falen door chemische boodschappers en kleine membraanpakketjes (exosomen) vrij te geven die de activiteit van killer-cellen dempen en de fagocyterende capaciteit van macrofagen verminderen.
Maandelijkse cycli, behulpzame spelers en een storm van ontsteking
Als menstrueel bloed en weefsel terugstromen naar de buikholte, voegen andere componenten van de menstruatie zich bij het verhaal. Bloedplaatjes en afbraakproducten van rode bloedcellen verminderen verder de dodelijke kracht van NK-cellen en macrofagen. In plaats van het weggespoelde weefsel te verwijderen, helpen ze het vast te hechten, binnen te dringen en te groeien. Op dat moment is de immuunomgeving sterk ontstekingsgericht: veel cellen geven alarmsignalen af die in theorie zouden moeten helpen bij het bestrijden van het abnormale weefsel. Toch stimuleren dezelfde signalen ook de groei van bloedvaten, celdeling en invasie door endometrioselaesies. Ontsteking wordt een tweesnijdend zwaard — te zwak om de laesies te elimineren, maar sterk genoeg om hun uitbreiding en de pijn die ze veroorzaken te voeden.
Van hete ontsteking naar een verzachtende, maar schadelijke kalmte
In de loop van de tijd verschuift de balans van immuuncellen rond de laesies. In het begin domineren “aanvallende” macrofagen en T‑helpercellen en geven agressieve signalen af die ontsteking bevorderen. Naarmate laesies groter worden en herhaaldelijk bloeden, beginnen ze een andere samenstelling van immuuncellen aan te trekken en te herprogrammeren — cellen die reacties kalmeren en schade beperken. Anti‑inflammatoire macrofagen, regulatorische T‑cellen en andere verzachtende celtypen nemen in aantal toe, aangetrokken door chemokinen en “alarmin”-moleculen die vrijkomen tijdens herhaald bloeden. Bloedplaatjes en lokale hormonen, zoals oestrogeen, duwen het systeem ook richting een rustiger, anti‑inflammatoir verblijf. Hoewel deze rustigere omgeving het omliggende weefsel beschermt tegen chronische, ongecontroleerde ontsteking, beschermt ze tegelijkertijd de laesies, bevordert ze de vorming van nieuwe bloedvaten en stimuleert ze de ophoping van littekenachtig vezelig weefsel.
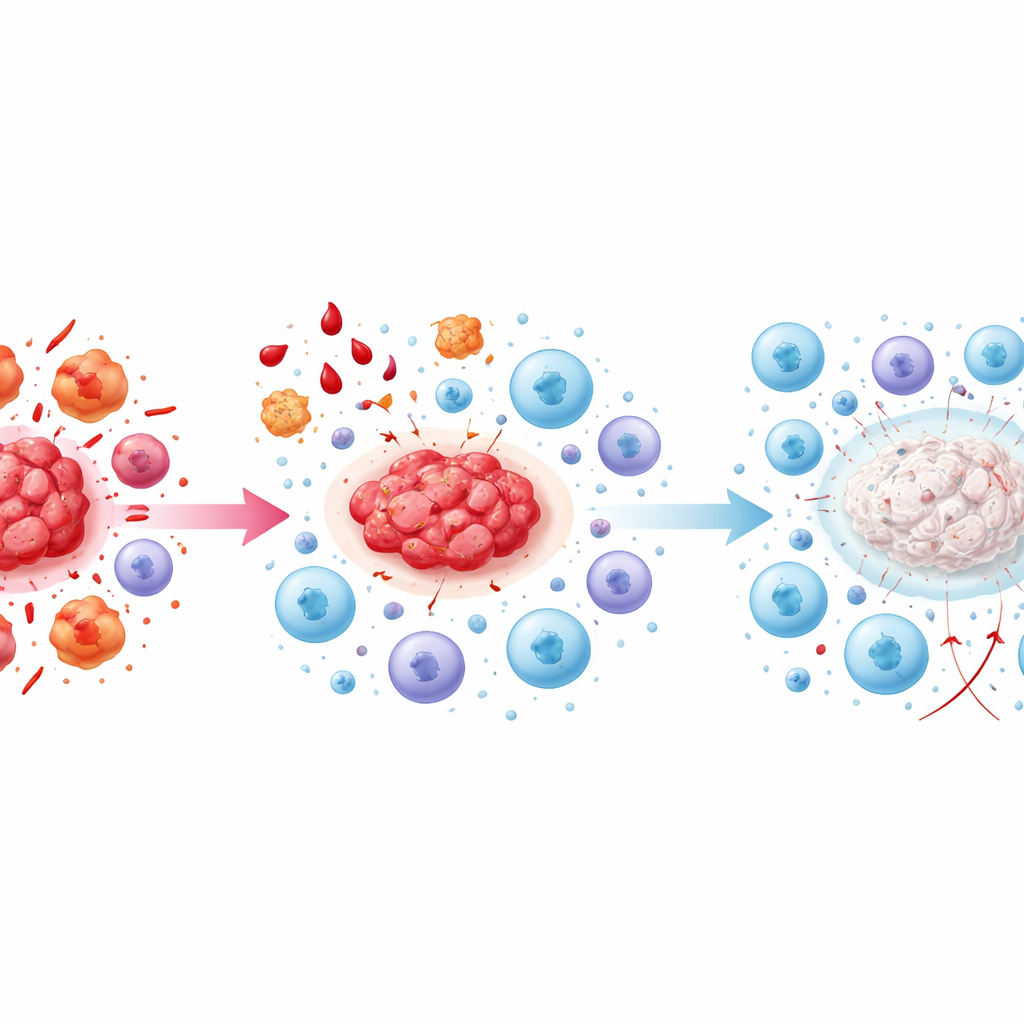
Als de killers hun energie opmaken
In de late stadia beschrijft het artikel een toestand van “immuunuitputting.” Killer-cellen die in principe laesies hadden kunnen aanvallen, zijn nu chronisch overstimuleerd en voortdurend onderdrukt door anti‑inflammatoire signalen. Ze beginnen oppervlaktemerkers te uiten die kenmerkend zijn voor vermoeide, ineffectieve cellen, en hun productie van cruciale aanvalsmoleculen neemt af. Signalen zoals TGF‑beta en IL‑10, geproduceerd door anti‑inflammatoire cellen en bloedplaatjes, versterken deze uitputting. Ondertussen raken checkpoints op immuuncellen — moleculaire remmen die normaal overreacties voorkomen — in toenemende mate geactiveerd, waardoor de respons verder wordt stilgelegd. Het resultaat is een zichzelf in stand houdende situatie waarin laesies blijven bestaan, rijkelijk van bloed voorzien zijn en fibrerend worden, terwijl de cellen die ze zouden moeten controleren wel aanwezig zijn maar grotendeels machteloos.
Wat dit betekent voor toekomstige behandelingen
Voor een niet‑specialist is de kernboodschap dat endometriose niet alleen een probleem is van weggelopen weefsel, maar van timing en balans in de afweer van het lichaam. De review stelt dat de ziekte vier immuunfasen doorloopt: ontsnapping, vroege ontsteking, latere anti‑ontsteking en uiteindelijk immuunuitputting. Omdat elke fase verschillende mengsels van cellen en signalen kent, kunnen behandelingen die op een bepaald moment werken, op een ander moment falen. Strategieën die zorgvuldig de activiteit van killer‑cellen stimuleren, het juiste soort ontsteking aanmoedigen, of de schadelijke samenwerking tussen bloedplaatjes, hormonen en kalmerende immuuncellen onderbreken, zouden de groei van laesies mogelijk kunnen vertragen of zelfs omkeren. Door deze immuun-tijdlijn in kaart te brengen, willen de auteurs meer precieze, op het ziekte‑stadium afgestemde therapieën sturen en uitleggen waarom het eenvoudig verwijderen van laesies vaak op zichzelf niet voldoende is.
Bronvermelding: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
Trefwoorden: endometriose, immuunmicroomgeving, chronische ontsteking, immuunuitputting, vrouwengezondheid