Clear Sky Science · de
Verschiebungen im immunologischen Mikromilieu bei Endometriose: vom Immunentkommen zur Immunerschöpfung
Warum die Abwehr des Körpers bei Endometriose wichtig ist
Endometriose ist eine schmerzhafte Erkrankung, bei der Gewebe, das dem Gebärmutterschleimhaut ähnelt, an falschen Stellen wächst und häufig starke Krämpfe, anhaltende Beckenschmerzen und Schwierigkeiten beim Schwangerwerden verursacht. Dieser Artikel beleuchtet eine weniger bekannte Facette der Krankheit: wie das körpereigene Abwehrsystem, das Immunsystem, zunächst versagt, diese fehlplatzierten Zellen zu beseitigen, und dann im Laufe der Zeit erschöpft wird. Das Verständnis dieser sich verändernden „immunologischen Landschaft“ könnte erklären, warum Endometriose persistiert, sich verschlechtert und oft selbst nach Operationen zurückkehrt.
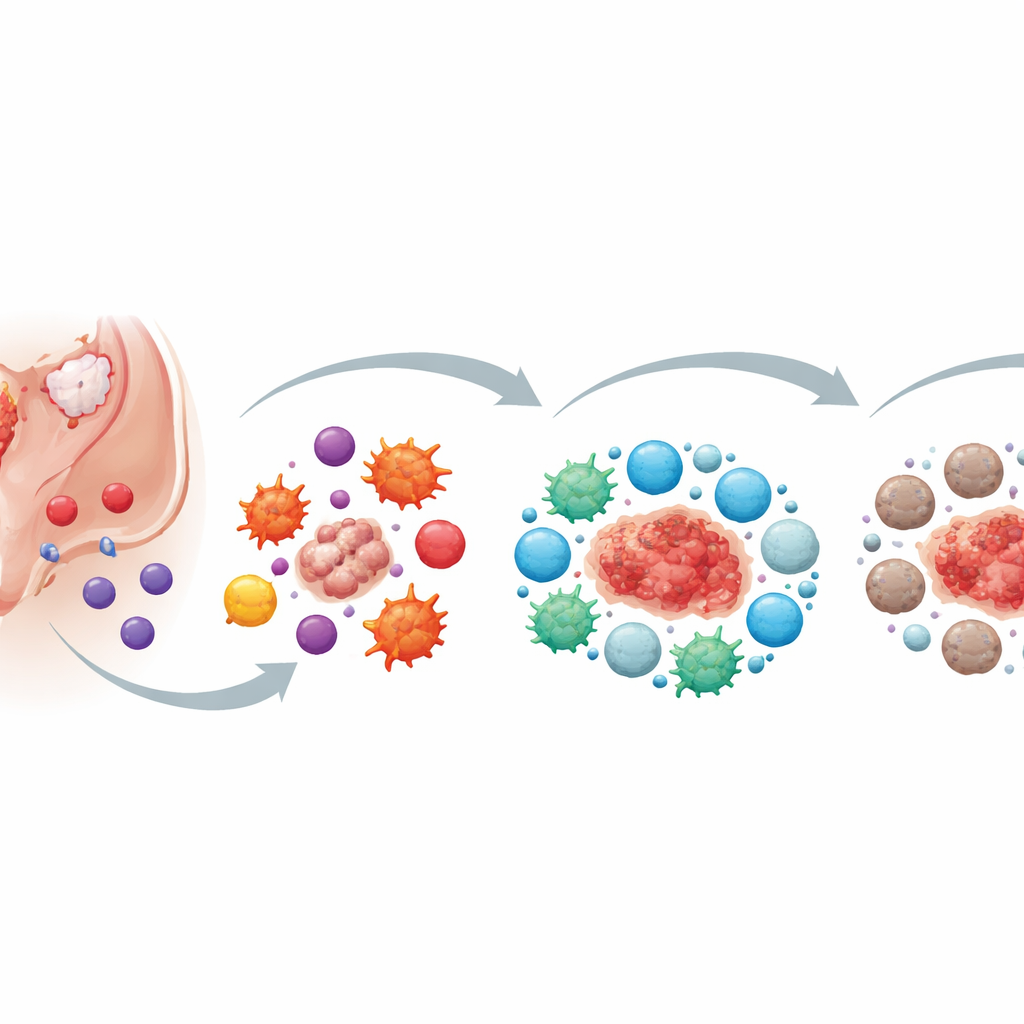
Erste Schritte: Wie problematische Zellen an der Abwehr vorbeischlüpfen
Die Autoren beschreiben die früheste Phase als „Immunentkommen“. Normalerweise patrouillieren spezialisierte weiße Blutzellen im Körper und beseitigen abnorme Zellen. Bei Endometriose gelangen ektopische Endometriumzellen (EECs) in die Bauchhöhle, doch wichtige „Killer“-Zellen — natürliche Killerzellen (NK-Zellen), bestimmte T-Zellen und Makrophagen — entfernen sie nicht wirksam. Diese Killerzellen sind zwar vorhanden, aber ihre Angriffsleistung ist abgeschwächt. Ihre aktivierenden Schalter sind heruntergeregelt, hemmende Schalter hochgeregelt, und sie sind weniger in der Lage, sich zur richtigen Zeit an den richtigen Ort zu bewegen. EECs tragen aktiv zu diesem Versagen bei, indem sie Botenstoffe und winzige Membranpakete (Exosomen) freisetzen, die die Aktivität der Killerzellen dämpfen und die Fähigkeit der Makrophagen reduzieren, unerwünschte Zellen „aufzufressen“.
Monatliche Zyklen, hilfreiche Mitspieler und ein Sturm der Entzündung
Wenn Menstruationsblut und Gewebe rückwärts in die Bauchhöhle fließen, kommen weitere Komponenten der Periode ins Spiel. Thrombozyten und Abbauprodukte roter Blutkörperchen schwächen die Tötungskraft von NK-Zellen und Makrophagen zusätzlich ab. Anstatt das fehlgeleitete Gewebe zu beseitigen, helfen sie ihm, sich festzusetzen, einzudringen und zu wachsen. Zu diesem Zeitpunkt ist das immunologische Umfeld stark entzündlich: viele Zellen setzen Alarmsignale frei, die theoretisch helfen sollten, das abnorme Gewebe zu bekämpfen. Diese Signale fördern jedoch gleichzeitig die Gefäßneubildung, Zellteilung und das Eindringen der Endometrioseherde. Entzündung wird so zum zweischneidigen Schwert — zu schwach, um die Herde zu eliminieren, aber stark genug, ihr Wachstum und die verursachten Schmerzen anzutreiben.
Von heißer Entzündung zu einer beruhigenden, aber schädlichen Ruhe
Im Laufe der Zeit verschiebt sich das Gleichgewicht der Immunzellen um die Herde. Anfänglich dominieren „angreifende“ Makrophagen und T-Helferzellen und setzen aggressive Signale frei, die Entzündungen fördern. Wenn Herde wachsen und wiederholt bluten, ziehen sie jedoch zunehmend andere Immunzellen an und formen diese um — solche, die Reaktionen beruhigen und Schäden begrenzen. Anti-inflammatorische Makrophagen, regulatorische T-Zellen und andere dämpfende Zelltypen nehmen an Zahl zu, angelockt von Chemokinen und „Alarmin“-Molekülen, die bei wiederholtem Bluten freigesetzt werden. Thrombozyten und lokale Hormone, etwa Östrogen, treiben das System zusätzlich in einen ruhigeren, anti-entzündlichen Zustand. Obwohl dieses ruhigere Umfeld das umliegende Gewebe vor chronischer, unkontrollierter Entzündung schützt, schirmt es gleichzeitig die Herde ab, fördert die Neubildung von Blutgefäßen und begünstigt die Ablagerung narbenähnlichen Bindegewebes.
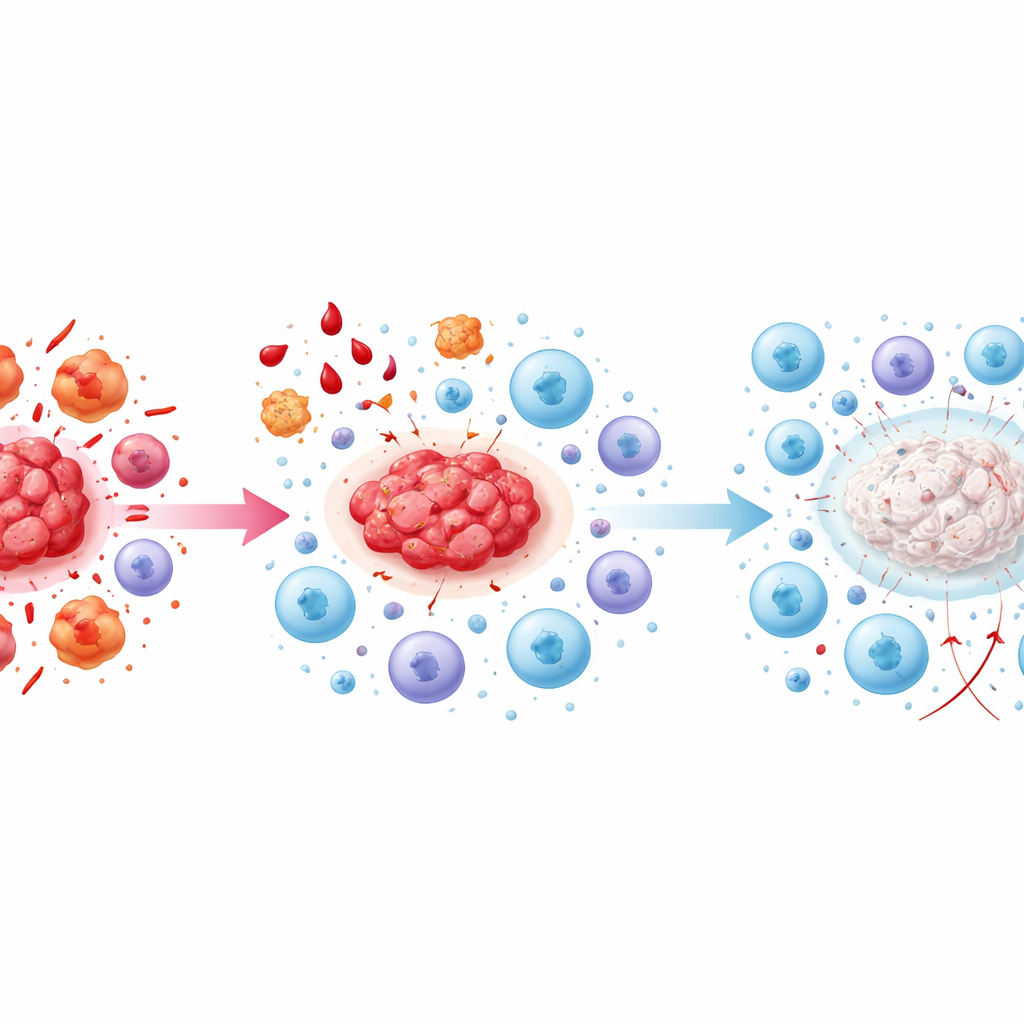
Wenn den Killern die Energie ausgeht
In späten Stadien beschreiben die Autoren einen Zustand der „Immunerschöpfung“. Killerzellen, die einst prinzipiell die Herde angreifen konnten, sind nun chronisch überstimuliert und dauerhaft durch anti-entzündliche Signale unterdrückt. Sie beginnen, Oberflächenmarker zu exprimieren, die für müde, unwirksame Zellen typisch sind, und ihre Produktion wichtiger Angriffsmediatoren nimmt ab. Signale wie TGF-beta und IL-10, erzeugt von anti-entzündlichen Zellen und Thrombozyten, verstärken diese Erschöpfung. Gleichzeitig werden Checkpoints auf Immunzellen — molekulare Bremsen, die normalerweise übermäßige Reaktionen verhindern — zunehmend aktiviert und dämpfen die Antwort weiter. Das Ergebnis ist eine sich selbst erhaltende Lage, in der Herde persistieren, gut durchblutet sind und fibrotisch werden, während die Zellen, die sie kontrollieren sollten, zwar vorhanden, aber weitgehend machtlos sind.
Was das für künftige Behandlungen bedeutet
Für nicht Fachkundige lautet die Botschaft: Endometriose ist nicht nur ein Problem fehlgeleiteten Gewebes, sondern eine Frage von Timing und Gleichgewicht in der körpereigenen Abwehr. Die Übersichtsarbeit schlägt vor, dass die Krankheit vier immunologische Phasen durchläuft: Entkommen, frühe Entzündung, spätere Anti-Entzündung und schließlich Immunerschöpfung. Da jede Phase unterschiedliche Zell- und Signalmischungen umfasst, können Behandlungen, die in einem Moment wirken, zu einem anderen Zeitpunkt versagen. Strategien, die gezielt Killerzellen stärken, die richtige Form der Entzündung fördern oder die schädliche Kooperation von Thrombozyten, Hormonen und dämpfenden Immunzellen unterbrechen, könnten eines Tages das Herdwachstum verlangsamen oder sogar rückgängig machen. Durch die Kartierung dieser immunologischen Zeitachse wollen die Autoren präzisere, phasengerechte Therapien leiten und verdeutlichen, warum das einfache Entfernen von Herden oft allein nicht ausreicht.
Zitation: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
Schlüsselwörter: Endometriose, immunologisches Mikromilieu, chronische Entzündung, Immunerschöpfung, Frauengesundheit