Clear Sky Science · pt
Alterações temporais do microambiente imune na endometriose: da evasão imune ao esgotamento imunológico
Por que as defesas do corpo importam na endometriose
A endometriose é uma condição dolorosa na qual tecido semelhante ao revestimento uterino cresce onde não deveria, frequentemente causando cólicas intensas, dor pélvica persistente e dificuldade para engravidar. Este artigo explora um lado menos familiar da doença: como o próprio sistema de defesa do corpo, o sistema imunológico, primeiro falha em eliminar essas células deslocadas e depois gradualmente se esgota. Compreender essa “paisagem imune” em mudança pode ajudar a explicar por que a endometriose persiste, piora com o tempo e muitas vezes retorna mesmo após cirurgia.
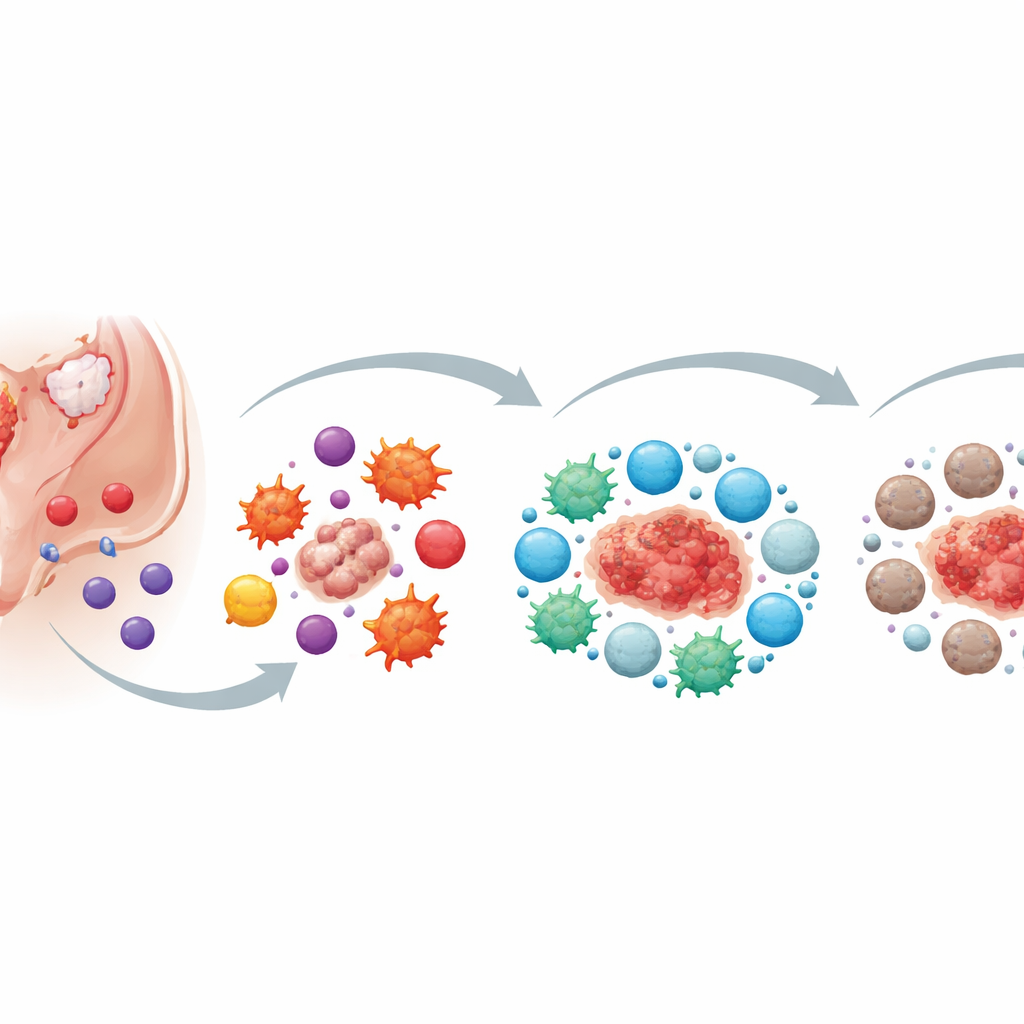
Primeiros passos: como as células problemáticas escapam da defesa
Os autores descrevem o estágio inicial como “evasão imune”. Normalmente, glóbulos brancos especializados patrulham o corpo e removem células anormais. Na endometriose, células endometriais ectópicas (CEE) acabam na cavidade abdominal, mas células “assassinas”-chave — células natural killer (NK), certos linfócitos T e macrófagos — não as removem de forma eficaz. Essas células assassinas estão presentes, mas sua capacidade de atacar está enfraquecida. Seus interruptores de ativação estão reduzidos, os de inibição estão aumentados e elas têm menos capacidade de migrar para o local certo no momento certo. As CEE contribuem ativamente para essa falha ao liberar mensageiros químicos e pequenas vesículas de membrana (exossomos) que atenuam a atividade das células assassinas e reduzem a habilidade dos macrófagos de “engolir” células indesejadas.
Ciclos mensais, ajudantes aparentes e uma tempestade de inflamação
À medida que sangue menstrual e tecido refluem para a cavidade abdominal, outros componentes do período entram em cena. Plaquetas e os produtos da degradação dos glóbulos vermelhos reduzem ainda mais o poder de eliminação das células NK e dos macrófagos. Em vez de limpar o tecido disperso, eles ajudam-no a aderir, invadir e crescer. Neste ponto, o ambiente imune é fortemente inflamatório: muitas células liberam sinais de alarme que, em tese, deveriam ajudar a combater o tecido anormal. No entanto, esses mesmos sinais também estimulam o crescimento de vasos sanguíneos, a divisão celular e a invasão pelas lesões de endometriose. A inflamação torna-se uma espada de dois gumes — fraca para eliminar as lesões, mas suficientemente forte para alimentar sua expansão e a dor que causam.
De uma inflamação “quente” para uma calma apaziguadora, porém prejudicial
Com o tempo, o equilíbrio das células imunes ao redor das lesões muda. No início, macrófagos “de ataque” e células T helper dominam, liberando sinais agressivos que promovem inflamação. À medida que as lesões aumentam e sangram repetidamente, começam a atrair e reprogramar um elenco diferente de células imunes — aquelas que acalmam respostas e limitam danos. Macrófagos anti-inflamatórios, células T reguladoras e outros tipos celulares apaziguadores aumentam em número, atraídos por quimiocinas e moléculas “alarminas” liberadas durante os sangramentos recorrentes. Plaquetas e hormônios locais, como o estrogênio, também empurram o sistema para um estado mais silencioso e anti-inflamatório. Embora esse ambiente mais calmo proteja os tecidos circundantes da inflamação crônica descontrolada, ele simultaneamente protege as lesões, favorece a formação de novos vasos sanguíneos e encoraja o acúmulo de tecido fibroso semelhante a cicatriz.
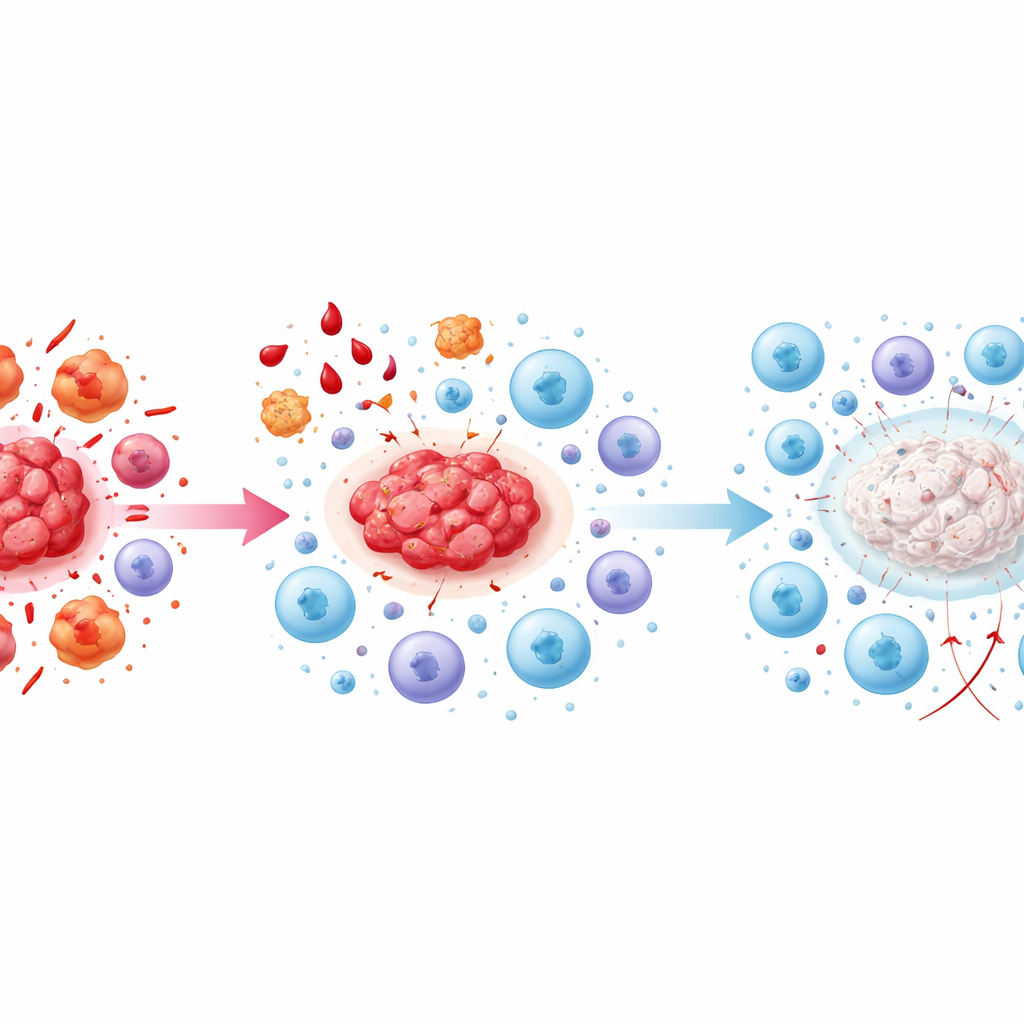
Quando as células assassinas ficam sem energia
Nos estágios avançados, o artigo descreve um estado de “esgotamento imunológico”. Células assassinas que antes, em princípio, poderiam atacar as lesões agora estão cronicamente superestimuladas e continuamente suprimidas por sinais anti-inflamatórios. Elas começam a expressar marcadores de superfície típicos de células cansadas e ineficazes, e sua produção de moléculas-chave de ataque diminui. Sinais como TGF-beta e IL-10, produzidos por células anti-inflamatórias e plaquetas, reforçam esse esgotamento. Enquanto isso, pontos de controle nas células imunes — freios moleculares que normalmente impedem reações excessivas — tornam-se cada vez mais ativos, silenciando ainda mais a resposta. O resultado é uma situação auto-sustentada em que as lesões persistem, são ricamente vascularizadas e tornam-se fibróticas, enquanto as próprias células que deveriam controlá-las estão presentes, mas em grande parte impotentes.
O que isso significa para tratamentos futuros
Para um não especialista, a mensagem é que a endometriose não é apenas um problema de tecido deslocado, mas de tempo e equilíbrio nas defesas do corpo. A revisão propõe que a doença progride por quatro fases imunes: evasão, inflamação inicial, anti-inflamação posterior e, finalmente, esgotamento imunológico. Como cada fase envolve diferentes combinações de células e sinais, tratamentos que funcionam em um momento podem falhar em outro. Estratégias que estimulem com cuidado a atividade das células assassinas, incentivem o tipo certo de inflamação ou interrompam a parceria prejudicial entre plaquetas, hormônios e células imunes apaziguadoras podem, um dia, desacelerar ou mesmo reverter o crescimento das lesões. Ao mapear essa linha do tempo imune, os autores pretendem orientar terapias mais precisas e ajustadas ao estágio e destacar por que a simples remoção das lesões muitas vezes não é suficiente por si só.
Citação: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
Palavras-chave: endometriose, microambiente imune, inflamação crônica, esgotamento imunológico, saúde da mulher