Clear Sky Science · it
I cambiamenti temporali del microambiente immunitario nell’endometriosi: dalla fuga immunitaria all’esaurimento immunitario
Perché le difese dell’organismo contano nell’endometriosi
L’endometriosi è una condizione dolorosa in cui tessuto simile al rivestimento uterino cresce dove non dovrebbe, causando spesso crampi molto intensi, dolore pelvico persistente e difficoltà a concepire. Questo articolo esplora un aspetto meno noto della malattia: come il sistema di difesa dell’organismo, il sistema immunitario, prima non riesca a eliminare queste cellule spostate e poi si esaurisca gradualmente. Comprendere questo «paesaggio immunitario» in evoluzione potrebbe aiutare a spiegare perché l’endometriosi persiste, peggiora nel tempo e spesso ricompare anche dopo l’intervento chirurgico.
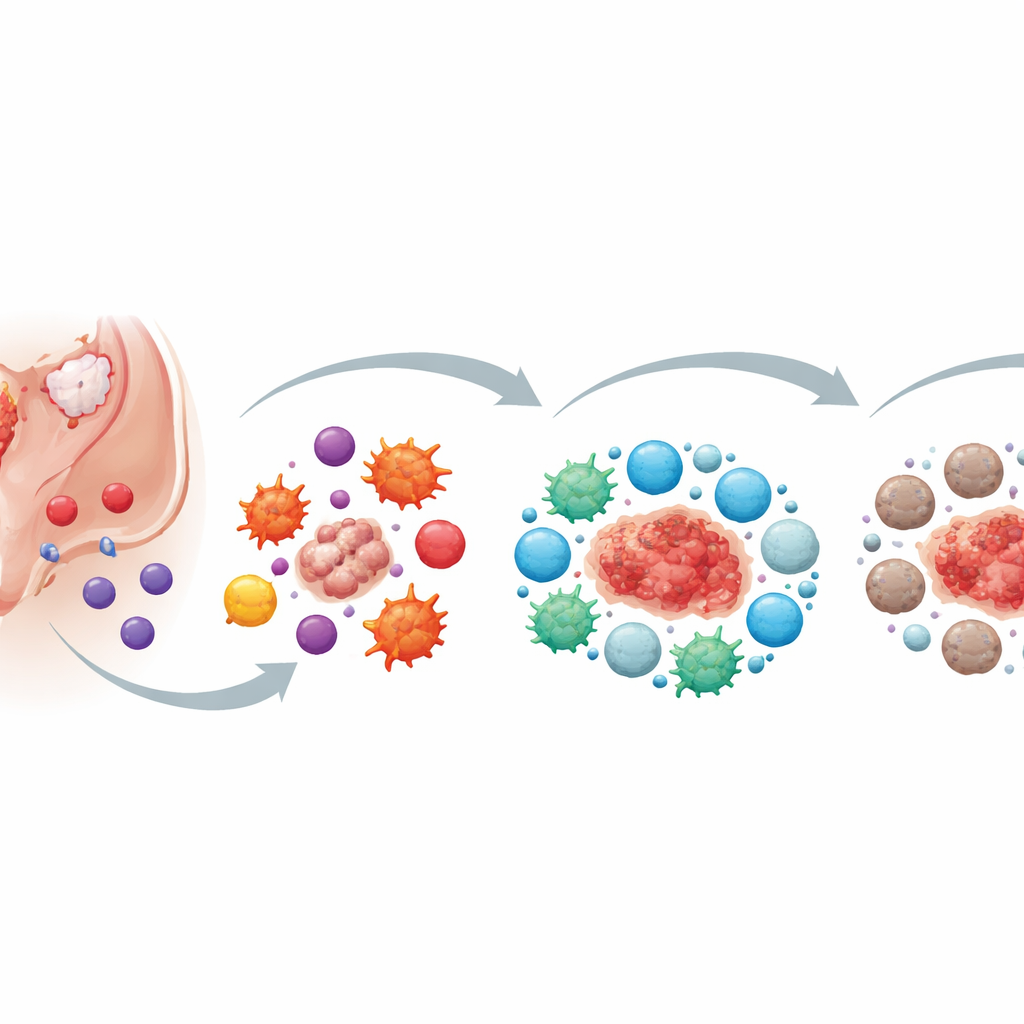
I primi passi: come le cellule problematiche sfuggono alle difese
Gli autori descrivono lo stadio iniziale come «fuga immunitaria». Normalmente, cellule bianche specializzate perlustrano l’organismo ed eliminano le cellule anomale. Nell’endometriosi, cellule endometriali ectopiche (EEC) finiscono nella cavità addominale, ma le cellule “assassine” chiave—le naturali killer (NK), alcuni linfociti T e i macrofagi—non le rimuovono efficacemente. Queste cellule citotossiche sono presenti, ma la loro capacità di attaccare è indebolita. I loro interruttori di attivazione sono abbassati, quelli inibitori sono aumentati e sono meno in grado di raggiungere il posto giusto al momento giusto. Le EEC contribuiscono attivamente a questo fallimento rilasciando messaggeri chimici e piccole vescicole di membrana (esosomi) che attenuano l’attività delle cellule killer e riducono la capacità dei macrofagi di “ingerire” le cellule indesiderate.
Cicli mensili, aiutanti compiacenti e una tempesta infiammatoria
Man mano che sangue mestruale e tessuto refluiscono nella cavità addominale, altri componenti del flusso mestruale entrano in gioco. Le piastrine e i prodotti di degradazione dei globuli rossi attenuano ulteriormente il potere uccidente di NK e macrofagi. Invece di eliminare il tessuto smarrito, lo aiutano ad aderire, invadere e crescere. A questo punto, l’ambiente immunitario è fortemente infiammatorio: molte cellule rilasciano segnali di allarme che, in teoria, dovrebbero favorire la lotta contro il tessuto anomalo. Tuttavia gli stessi segnali promuovono anche la crescita dei vasi sanguigni, la proliferazione cellulare e l’invasione da parte delle lesioni endometriosiche. L’infiammazione diventa un’arma a doppio taglio—troppo debole per eliminare le lesioni, ma abbastanza intensa da alimentarne l’espansione e il dolore che provocano.
Dall’infiammazione acuta a una calma apparentemente benefica ma dannosa
Con il tempo, l’equilibrio delle cellule immunitarie intorno alle lesioni cambia. Nelle fasi iniziali dominano macrofagi “attaccanti” e linfociti T helper, che rilasciano segnali aggressivi che favoriscono l’infiammazione. Man mano che le lesioni si ingrandiscono e sanguinano ripetutamente, iniziano ad attrarre e rimodellare un diverso repertorio di cellule immunitarie—quelle che placano le risposte e limitano i danni. Macrofa gi anti-infiammatori, cellule T regolatorie e altri tipi cellulari “calmanti” aumentano di numero, richiamati da chemochine e molecole di allarme rilasciate durante il sanguinamento ripetuto. Le piastrine e ormoni locali, come gli estrogeni, spingono anch’essi il sistema verso uno stato più tranquillo e anti-infiammatorio. Sebbene questo ambiente più calmo protegga i tessuti circostanti da un’infiammazione cronica incontrollata, al contempo protegge le lesioni, favorisce la formazione di nuovi vasi e incoraggia l’accumulo di tessuto fibrotico simile a una cicatrice.
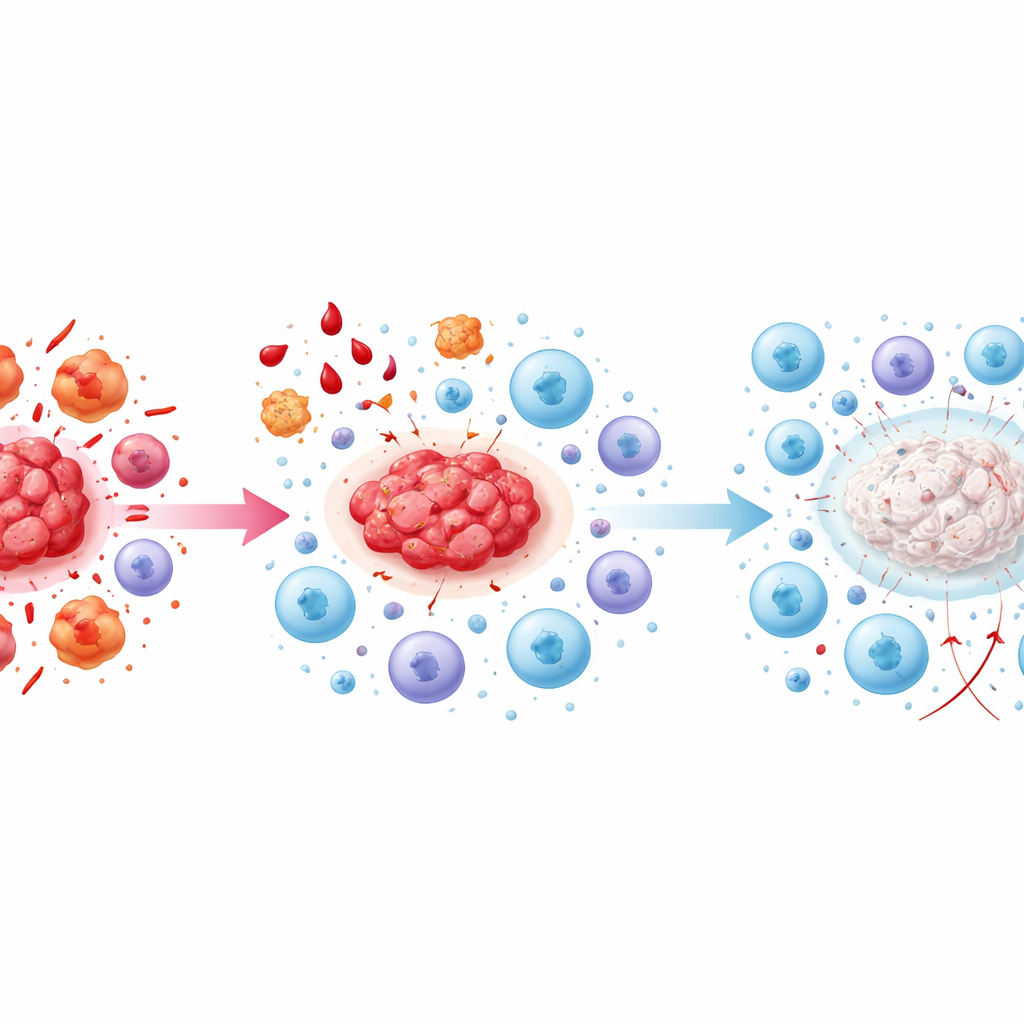
Quando le cellule “assassine” esauriscono l’energia
Nelle fasi avanzate, l’articolo descrive uno stato di «esaurimento immunitario». Le cellule killer che una volta avrebbero potuto attaccare le lesioni sono ora cronicamente sovra-stimolate e costantemente soppresse da segnali anti-infiammatori. Cominciano a esprimere marcatori di superficie tipici di cellule stanche e inefficaci, e la loro produzione di molecole d’attacco chiave diminuisce. Segnali come TGF-beta e IL-10, prodotti da cellule anti-infiammatorie e dalle piastrine, rinforzano questo esaurimento. Nel frattempo, checkpoint immunitari—freni molecolari che normalmente prevengono reazioni eccessive—sono sempre più attivi, silenziando ulteriormente la risposta. Il risultato è una situazione auto-sostenuta in cui le lesioni persistono, sono ben vascolarizzate e diventano fibrotiche, mentre le stesse cellule che dovrebbero controllarle sono presenti ma in gran parte impotenti.
Cosa significa questo per i trattamenti futuri
Per il non specialista, il messaggio è che l’endometriosi non è solo un problema di tessuto errante, ma di tempistica ed equilibrio nelle difese dell’organismo. La revisione propone che la malattia attraversi quattro fasi immunitarie: fuga, infiammazione iniziale, successiva anti-infiammazione e infine esaurimento immunitario. Poiché ogni fase coinvolge miscele diverse di cellule e segnali, trattamenti efficaci in un momento possono fallire in un altro. Strategie che potenzino con attenzione l’attività delle cellule killer, favoriscano il tipo giusto di infiammazione o interrompano la collaborazione dannosa tra piastrine, ormoni e cellule immunitarie calmanti potrebbero un giorno rallentare o persino invertire la crescita delle lesioni. Mappando questa linea temporale immunitaria, gli autori mirano a guidare terapie più precise e adeguate allo stadio della malattia e a spiegare perché la semplice rimozione delle lesioni spesso non è sufficiente da sola.
Citazione: Fan, W., Fengting, Z. & Ruihua, Z. Endometriosis immune microenvironment timing shifts: from immune escape to immune exhaustion. Cell Death Discov. 12, 125 (2026). https://doi.org/10.1038/s41420-026-02965-8
Parole chiave: endometriosi, microambiente immunitario, infiammazione cronica, esaurimento immunitario, salute femminile